Clear Sky Science · sv
Kombinera 5-ALA-PDT med berbamin som en in vitro multimodal behandlingsstrategi mot blåscancerceller
Varför denna forskning är viktig
Blåscancer är vanligt, kostsamt att behandla och återkommer ofta även efter aggressiv terapi. Många tumörer slutar så småningom svara på standardkemoterapi som cisplatin, delvis eftersom en liten population svårslagna ”start”-celler kan överleva behandlingen och återbilda cancern. Denna studie undersöker i laboratoriet en behandlingskombination som parar en ljusaktiverad cancerterapi med en naturlig växtförening för att avgöra om duon bättre kan slå ut envisa blåscancerceller, inklusive dem som är resistenta mot kemoterapi och beter sig som stamceller.
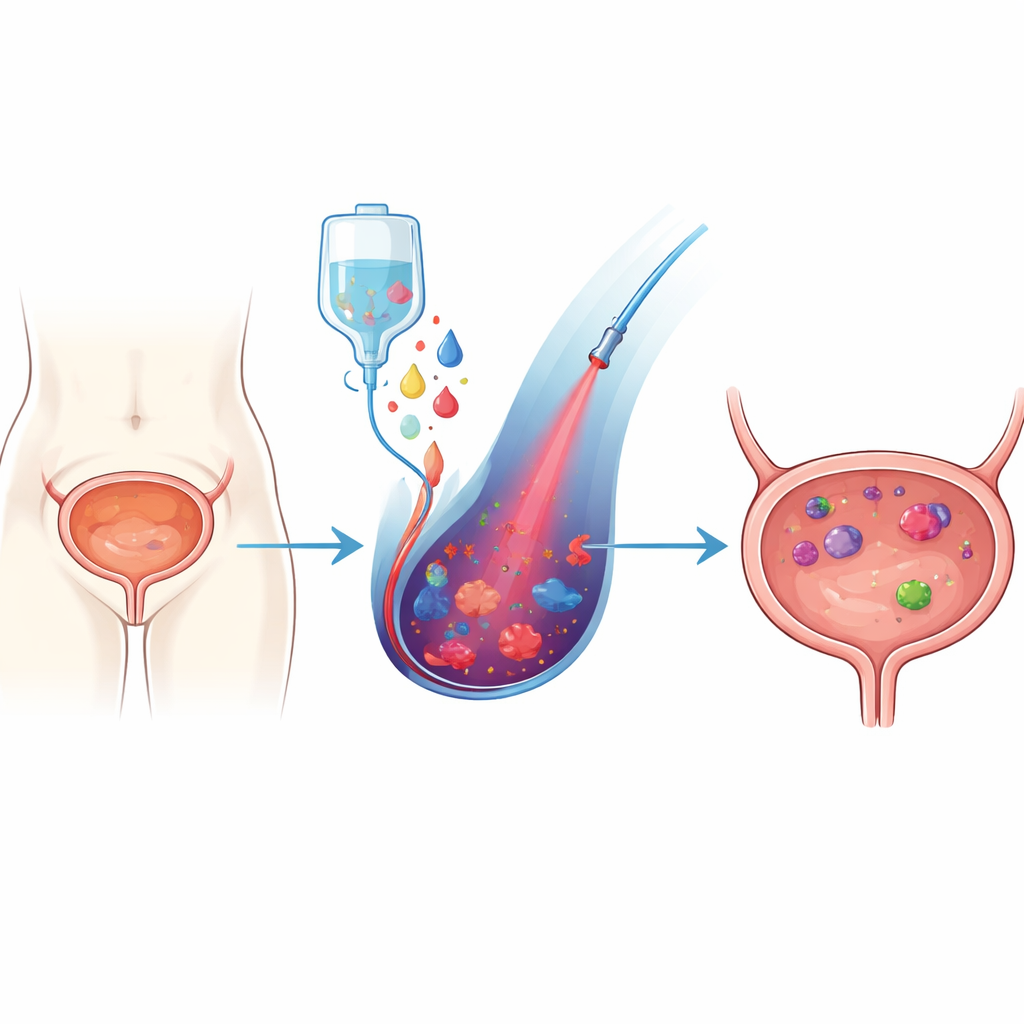
En ljusburen metod för att angripa tumörer
Den första delen av behandlingen kallas 5-aminolevulinsyra–medierad fotodynamisk terapi, eller 5-ALA-PDT. 5-ALA är en byggsten som celler använder för att tillverka hem, den röda pigmenten i blod. När extra 5-ALA tillförs externt tenderar tumörceller att lagra en intermediär molekyl som kallas protoporfyrin IX. Denna molekyl fungerar som en ljusfångare: när rött laserljus lyser på den bildas mycket reaktiva syremolekyler som kan skapa hål i cellstrukturer och utlösa olika former av celldöd. Eftersom cancerceller ofta ackumulerar mer av denna ljusfångare än normala celler kan 5-ALA-PDT i viss mån skada tumörer föredraget samtidigt som frisk vävnad skonas. Metoden har redan visat lovande resultat i tidiga studier av blåscancer, men dess effekt begränsas av cellernas interna försvarssystem som rensar upp reaktiva syrearter.
En växtförening med anticancerpotential
Den andra delen av strategin är berbamin, ett naturligt alkaloid utvunnet ur växten Berberis amurensis. Tidigare arbeten har antytt att berbamin kan bromsa tumörtillväxt, minska cellrörelse och invasion samt främja cancercelldöd samtidigt som det är mindre skadligt för normala celler. Det kan också störa flera överlevnadsbanor i cancerceller, inklusive en nyckelomkopplare som kallas NF-κB och andra signaler kopplade till läkemedelsresistens och cellmigration. Författarna studerade berbamin i två humana blåscancercellinjer (RT112 och J82), deras cisplatinresistenta motsvarigheter och versioner odlade under särskilda förhållanden för att berika för tumörstamcells-liknande sfärer. De mätte först hur snabbt varje celltyp förökade sig och hur mycket berbamin som krävdes för att halvera cellöverlevnaden, och använde sedan dessa värden för att bestämma doser i kombinationsexperimenten.
Hur kombinationen testades i laboratorium
För att se hur de två behandlingarna samverkar exponerade teamet celler för olika mängder 5-ALA, tillsatte varierande doser berbamin och belyste dem sedan med rött laserljus vid kontrollerade energinivåer. De mätte hur mycket av den ljusfångande protoporfyrin IX som byggdes upp i varje celltyp, hur många reaktiva syremolekyler som genererades och hur många celler som förblev levande efteråt. I samtliga blåscancercellinjer ledde mer 5-ALA till mer protoporfyrin IX, upp till en mättnadspunkt. Tillsats av berbamin ökade denna ansamling ytterligare, i vissa fall mer än åttafaldigt, och ökade generellt skadan när cellerna utsattes för ljus. Berbamin ensam minskade också celltillväxt, begränsade migration och invasion samt inducerade celldöd, där cisplatinresistenta celler ofta visade särskild sårbarhet.
Olika tumörceller, olika svar
Kombinationen uppförde sig inte identiskt i alla celltyper, vilket understryker hur varierande blåscancer kan vara. I de cisplatinresistenta J82 LTT-cellerna förstärkte högre berbamindoser stadigt 5-ALA-PDT:s dödande effekt och utplånade nästan levande celler under de starkaste förhållandena. I kontrast svarade vissa föräldra-J82-celler och deras stamcells‑lika motsvarigheter bäst vid måttliga berbamindoser; att höja dosen ytterligare verkade dämpa den extra nyttan av ljusterapi, möjligen eftersom överlevande celler ökade sina försvar. För RT112-celler förbättrade berbamin 5-ALA-PDT främst vid vissa 5-ALA-doser, medan i den cisplatinresistenta RT112 LTT-linjen var 5-ALA-PDT redan så effektiv att ytterligare berbamin inte gav mycket mer nytta. Mest anmärkningsvärt var att RT112 tumörstamcells-liknande sfärer var mycket känsliga för kombinationen: måttliga doser 5-ALA och berbamin tillsammans med ljus räckte för att sänka överlevnaden till nästan bakgrundsnivåer, vilket tyder på att dessa annars motståndskraftiga startceller kan träffas selektivt.
Vad detta kan innebära för framtida behandling
Förenklat visar studien att parning av ett ljusaktiverat läkemedel med en växtbaserad förening kan göra blåscancerceller, inklusive kemoterapiresistenta och stamcells‑lika celler, lättare att förstöra i laboratoriet. Berbamin skadar inte bara tumörceller på egen hand utan hjälper dem också att ladda upp mer av den ljusfångande molekylen som driver fotodynamisk terapi, vilket tippar balansen mot dödlig oxidativ skada när rött ljus appliceras. Den exakta dosblandningen spelar roll och beror på varje tumörs biologi, men konceptet att ”finjustera” ljusterapi med en lågkostnadssensitiserare är lovande. Arbetet utfördes i cellodlingar, inte på patienter, så det bevisar ännu inte nytta hos människor. Det pekar dock mot en framtid där blåstumörer, särskilt sådana som överlistat standardläkemedel, kan screenas för känslighet mot 5-ALA-PDT plus berbamin och sedan behandlas med en skräddarsydd kombination som även riktar sig mot de hårdaste cancerfröna.
Citering: Kabus, M., Aumiller, M., Rühm, A. et al. Combining 5-ALA-PDT with berbamine as an in vitro multimodal therapy approach against bladder cancer cells. Sci Rep 16, 11228 (2026). https://doi.org/10.1038/s41598-026-46092-x
Nyckelord: blåscancer, fotodynamisk terapi, berbamin, cisplatinresistens, cancerstamceller