Clear Sky Science · pl
Połączenie 5-ALA-PDT z berbaminą jako in vitro multimodalne podejście terapeutyczne przeciw komórkom raka pęcherza
Dlaczego te badania są istotne
Rak pęcherza jest powszechny, kosztowny w leczeniu i często nawraca nawet po agresywnej terapii. Wiele guzów z czasem przestaje reagować na standardowe leki chemioterapeutyczne, takie jak cisplatyna, częściowo dlatego, że niewielka pula trudnych do zabicia „komórek startowych” może przetrwać leczenie i odtworzyć nowotwór. W tym badaniu sprawdzono w warunkach laboratoryjnych połączenie terapii przeciwnowotworowej aktywowanej światłem z naturalnym związkiem roślinnym, pytając, czy duet ten może skuteczniej eliminować oporne komórki raka pęcherza, w tym te zachowujące się jak komórki macierzyste.
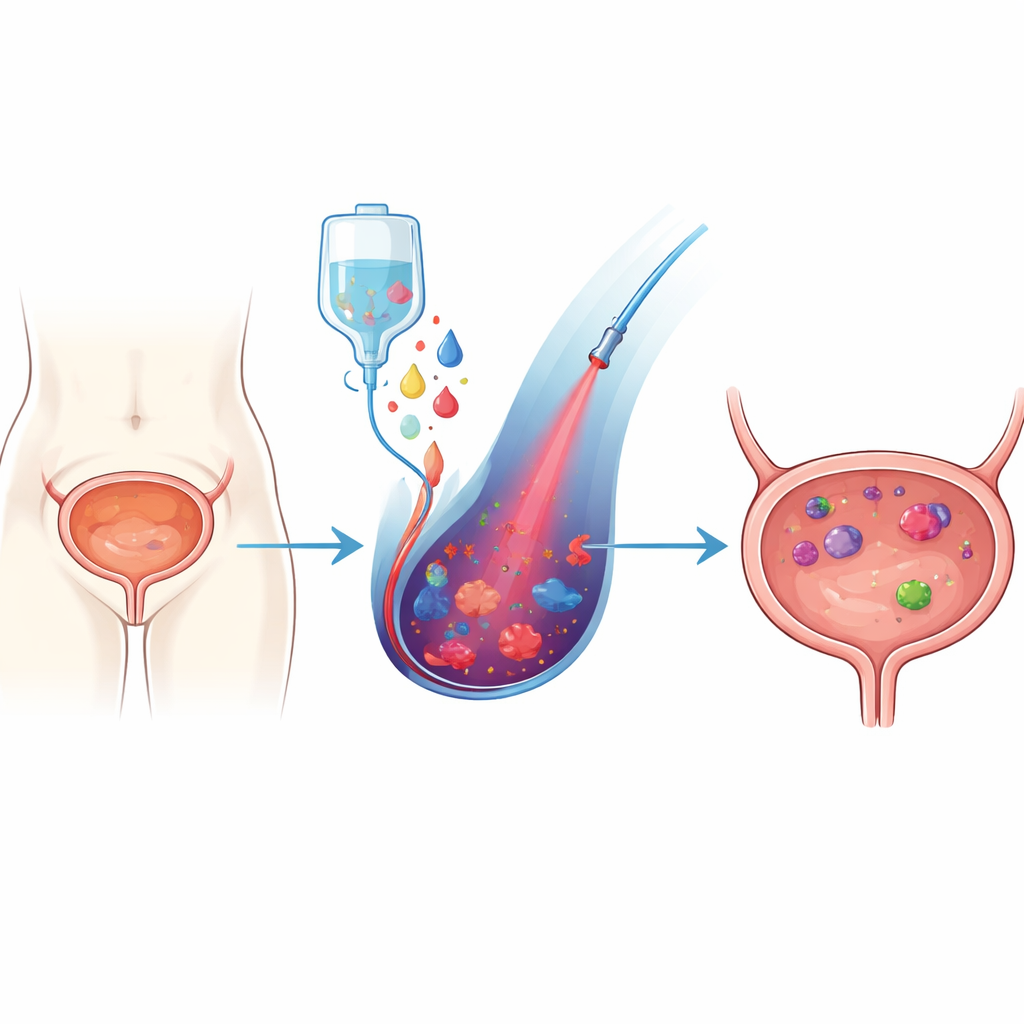
Metoda oparta na świetle do ataku na guzy
Pierwsza część leczenia to fotodynamiczna terapia z wykorzystaniem kwasu 5‑aminolewulinowego, czyli 5‑ALA‑PDT. 5‑ALA jest składnikiem, którego komórki używają do syntezy hemu, czerwonego barwnika we krwi. Gdy podaje się dodatkowe 5‑ALA z zewnątrz, komórki nowotworowe mają tendencję do gromadzenia pośredniego związku zwanego protoporfiryną IX. Ten związek działa jak „łapacz światła”: kiedy naświetla się go czerwonym światłem lasera, wytwarza silnie reaktywne cząsteczki tlenu, które mogą uszkadzać struktury komórkowe i wywoływać różne formy śmierci komórki. Ponieważ komórki nowotworowe często akumulują więcej tego „łapacza światła” niż komórki normalne, 5‑ALA‑PDT może preferencyjnie uszkadzać guzy, oszczędzając zdrowe tkanki. Metoda ta wykazała już obiecujące wyniki w wczesnych badaniach raka pęcherza, ale jej skuteczność jest ograniczana przez wewnętrzne systemy obronne komórek, które neutralizują reaktywne formy tlenu.
Związek roślinny o potencjale przeciwnowotworowym
Drugą część strategii stanowi berbamina, naturalny alkaloid wyizolowany z rośliny Berberis amurensis. Wcześniejsze badania sugerowały, że berbamina może spowalniać wzrost guza, ograniczać ruchliwość i inwazję komórek oraz promować ich śmierć, przy mniejszej toksyczności wobec komórek prawidłowych. Może także zakłócać kilka szlaków przetrwania w komórkach nowotworowych, w tym kluczowy czynnik przełączający znany jako NF‑κB oraz inne sygnały związane z opornością na leki i migracją komórek. Autorzy badali berbaminę w dwóch ludzkich liniach komórek raka pęcherza (RT112 i J82), ich odpowiednikach opornych na cisplatynę oraz w wariantach hodowanych w specjalnych warunkach, które wzbogacają populacje przypominające kuliste komórki macierzyste. Najpierw zmierzyli tempo namnażania każdej linii komórkowej i dawkę berbaminy konieczną do zmniejszenia przeżywalności o połowę, a następnie użyli tych wartości do ustalenia dawek w eksperymentach łączonych.
Jak kombinację testowano w laboratorium
Aby sprawdzić, jak obie terapie wchodzą ze sobą w interakcję, zespół eksponował komórki na różne ilości 5‑ALA, dodawał zmienne dawki berbaminy, a następnie naświetlał je czerwonym światłem lasera przy kontrolowanym poziomie energii. Mierzono, ile protoporfiryny IX gromadziło się w każdym typie komórek, ile reaktywnych form tlenu zostało wygenerowanych oraz ile komórek pozostało przy życiu po zabiegu. We wszystkich badanych liniach raka pęcherza więcej 5‑ALA powodowało większe nagromadzenie protoporfiryny IX aż do punktu nasycenia. Dodanie berbaminy dalsze zwiększało to nagromadzenie, w niektórych przypadkach ponad ośmiokrotnie, i zwykle zwiększało uszkodzenia wywołane przez naświetlanie. Sama berbamina również ograniczała wzrost komórek, zmniejszała migrację i inwazję oraz indukowała śmierć komórek, przy czym komórki oporne na cisplatynę często wykazywały szczególną wrażliwość.
Różne komórki nowotworowe, różne odpowiedzi
Kombinacja nie zachowywała się identycznie we wszystkich typach komórek, co podkreśla zróżnicowanie raków pęcherza. W komórkach J82 LTT opornych na cisplatynę wyższe stężenia berbaminy stopniowo wzmacniały efekt zabijania 5‑ALA‑PDT, niemal eliminując żywe komórki przy najsilniejszych warunkach. W przeciwieństwie do tego, niektóre komórki rodzicielskie J82 i ich odpowiedniki przypominające komórki macierzyste najlepiej reagowały przy umiarkowanych poziomach berbaminy; dalsze podnoszenie dawki wydawało się osłabiać dodatkową korzyść z naświetlania, być może dlatego, że pozostałe przy życiu komórki zwiększały swoje mechanizmy obronne. W komórkach RT112 berbamina poprawiała skuteczność 5‑ALA‑PDT głównie przy określonych dawkach 5‑ALA, podczas gdy w linii RT112 LTT opornej na cisplatynę 5‑ALA‑PDT było już tak skuteczne, że dodatkowa berbamina nie przynosiła znaczącego wzrostu efektu. Najbardziej uderzające było to, że kuliste, przypominające komórki macierzyste struktury RT112 były bardzo wrażliwe na kombinację: umiarkowane dawki 5‑ALA i berbaminy razem z naświetlaniem wystarczyły, by obniżyć przeżywalność niemal do tła, co sugeruje, że te zazwyczaj odporne „komórki startowe” można selektywnie zaatakować.
Co to może oznaczać dla przyszłego leczenia
Mówiąc najprościej, badanie pokazuje, że połączenie leku aktywowanego światłem z pochodnym roślinnym może uczynić komórki raka pęcherza, w tym komórki oporne na chemioterapię i te przypominające komórki macierzyste, łatwiejszymi do zniszczenia w laboratorium. Berbamina nie tylko sama szkodzi komórkom nowotworowym, lecz także pomaga im gromadzić więcej „łapacza światła”, który napędza terapię fotodynamiczną, przechylając równowagę w stronę śmiertelnych uszkodzeń oksydacyjnych po zastosowaniu czerwonego światła. Dokładne proporcje dawek mają znaczenie i zależą od biologii danego guza, ale koncepcja „strojenia” terapii opartej na świetle za pomocą niedrogiego sensitizatora jest obiecująca. Prace przeprowadzono na hodowlach komórkowych, a nie u pacjentów, więc nie dowodzą jeszcze korzyści u ludzi. Mimo to wskazują na przyszłość, w której guzy pęcherza, zwłaszcza te, które przechytrzyły standardowe leki, mogłyby być badane pod kątem wrażliwości na 5‑ALA‑PDT plus berbaminę, a następnie leczone dobraną kombinacją ukierunkowaną nawet na najbardziej oporne „nasiona” nowotworu.
Cytowanie: Kabus, M., Aumiller, M., Rühm, A. et al. Combining 5-ALA-PDT with berbamine as an in vitro multimodal therapy approach against bladder cancer cells. Sci Rep 16, 11228 (2026). https://doi.org/10.1038/s41598-026-46092-x
Słowa kluczowe: rak pęcherza, terapia fotodynamiczna, berbamina, oporność na cisplatynę, komórki macierzyste nowotworu