Clear Sky Science · ar
دمج العلاج الضوئي 5-ALA-PDT مع البربامين كنهج علاج متعدد الوسائط في المختبر ضد خلايا سرطان المثانة
لماذا يهم هذا البحث
سرطان المثانة شائع وتكلفة علاجه مرتفعة، وغالبًا ما يعود حتى بعد علاجات قاسية. الكثير من الأورام تتوقف في النهاية عن الاستجابة للأدوية الكيميائية القياسية مثل السيسبلاتين، جزئياً لأن هناك مجموعة صغيرة من الخلايا «المبدئية» الصعبة القتل التي قد تبقى على قيد الحياة بعد العلاج وتعيد نمو السرطان. تستكشف هذه الدراسة زوجًا من العلاجات المختبرية يجمعان علاجًا ضوئيًا منشطًا للسرطان ومركبًا نباتيًا طبيعيًا، وتسأل ما إذا كان هذا الزوج قادرًا على القضاء بصورة أفضل على خلايا سرطان المثانة العنيدة، بما في ذلك تلك المقاومة للعلاج الكيميائي والتي تتصرف مثل الخلايا الجذعية.
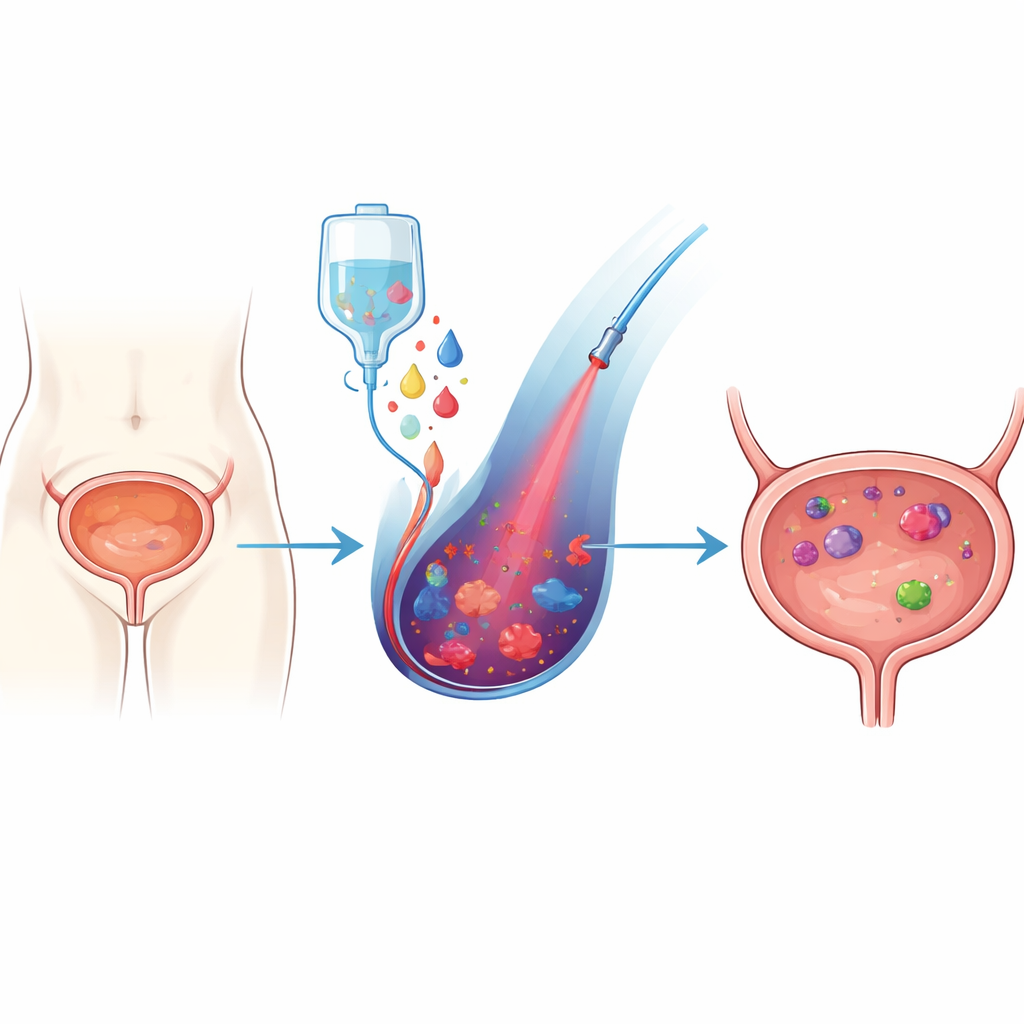
طريقة تعتمد على الضوء لمهاجمة الأورام
الجزء الأول من العلاج يسمى العلاج الضوئي الديناميكي بوساطة حمض 5-أمينوليفولينك، أو 5-ALA-PDT. 5-ALA هو لبنة يستخدمها الخلايا لصنع الهيم، الصبغة الحمراء في الدم. عندما يُزوَّد الخلايا بكمية إضافية من 5-ALA من الخارج، تميل الخلايا الورمية إلى تراكم جزيء وسيط يُدعى بروتوبورفيرين IX. يعمل هذا الجزيء كـمُمسك للضوء: عندما يُسقط عليه ضوء ليزر أحمر، ينتج جزيئات أكسجين تفاعلية للغاية يمكنها إحداث ثقوب في هياكل الخلية وتحفيز أشكال مختلفة من موت الخلية. وبما أن خلايا السرطان غالبًا ما تجمع مزيدًا من هذا الممسك الضوئي مقارنة بالخلايا الطبيعية، فإن 5-ALA-PDT يمكن أن يُلحق أضرارًا تفضيلية بالأورام مع الحفاظ على الأنسجة السليمة. لقد أظهر بالفعل نتائج واعدة في تجارب مبكرة على سرطان المثانة، لكن قوته محدودة بآليات الدفاع الداخلية للخلايا التي تزيل الجذور الحرة.
مركب نباتي ذي إمكانات مضادة للسرطان
الجزء الثاني من الاستراتيجية هو البربامين، وهو قلويد طبيعي مُستخلص من نبات Berberis amurensis. أشارت أعمال سابقة إلى أن البربامين يمكن أن يبطئ نمو الأورام، ويقلل من حركة الخلايا وغزوها، ويعزز موت الخلايا السرطانية مع إحداث ضرر أقل للخلايا السليمة. كما يمكن أن يتداخل مع عدة مسارات بقاء داخل الخلايا السرطانية، بما في ذلك مفتاح تحكمي معروف باسم NF-κB وإشارات أخرى مرتبطة بمقاومة الأدوية وهجرة الخلايا. درس المؤلفون البربامين في سلايلتين بشريتين من سرطان المثانة (RT112 وJ82)، ونظائرهما المقاومة للسيسبلاتين، ونسخًا نمت تحت ظروف خاصة لإغناء الكرات الشبيهة بالخلايا الجذعية السرطانية. قاسوا أولًا مدى سرعة تكاثر كل نوع من الخلايا وكمية البربامين اللازمة لخفض بقاء الخلايا إلى النصف، ثم استخدموا هذه القيم لتحديد الجرعات لتجارب التوليف.
كيف تم اختبار التوليفة في المختبر
لمعرفة كيفية تفاعل العلاجين، عرض الفريق الخلايا لكميات مختلفة من 5-ALA، وأضافوا جرعات متباينة من البربامين، ثم أضاءوها بضوء ليزر أحمر عند مستويات طاقة محكومة. قاسوا مقدار تراكم البروتوبورفيرين IX في كل نوع من الخلايا، وكمية الجزيئات الأكسجينية التفاعلية التي تُنتَج، وعدد الخلايا التي بقيت حية بعد ذلك. في جميع خطوط خلايا سرطان المثانة، أدت كميات أكبر من 5-ALA إلى مزيد من البروتوبورفيرين IX حتى نقطة التشبع. عزز إضافة البربامين هذا التراكم أكثر، وفي بعض الحالات بما يصل إلى أكثر من ثمانية أضعاف، وعموماً زاد الضرر الحاصل عند تعريض الخلايا للضوء. كما أن البربامين وحده خفّض أيضًا نمو الخلايا، وقيّد الهجرة والغزو، وحفّز موت الخلايا، مع إظهار الخلايا المقاومة للسيسبلاتين قابلية خاصة في كثير من الحالات.
خلايا ورمية مختلفة، استجابات مختلفة
لم تتصرف التوليفة بنفس الشكل في كل نوع من الخلايا، مما يبرز مدى تنوّع سرطانات المثانة. في خلايا J82 LTT المقاومة للسيسبلاتين، زادت تراكيز البربامين الأعلى من قوة القتل بواسطة 5-ALA-PDT بشكل مطرد، وكادت تقضي على الخلايا الحية في أقوى الظروف. على النقيض من ذلك، استجابت بعض خلايا J82 الأصلية ونظيراتها الشبيهة بالخلايا الجذعية بأفضل شكل عند مستويات بربامين متوسطة؛ فرفع الجرعة قد أضعف الفائدة المضافة للعلاج الضوئي، ربما لأن الخلايا الناجية رفعت من آليات دفاعها. بالنسبة لخلايا RT112، حسّن البربامين 5-ALA-PDT بشكل رئيسي عند جرعات معينة من 5-ALA، بينما في خط RT112 LTT المقاوم للسيسبلاتين كان 5-ALA-PDT فعالًا بما فيه الكفاية لدرجة أن إضافة البربامين لم تضف كثيرًا. والأكثر بروزًا، كانت كرات RT112 الشبيهة بالخلايا الجذعية شديدة الحساسية للتوليفة: جرعات متواضعة من 5-ALA والبربامين مع الضوء كانت كافية لخفض البقاء إلى مستويات تكاد تكون خلفية، مما يشير إلى أن هذه الخلايا المبدئية الصامدة يمكن استهدافها بشكل انتقائي.
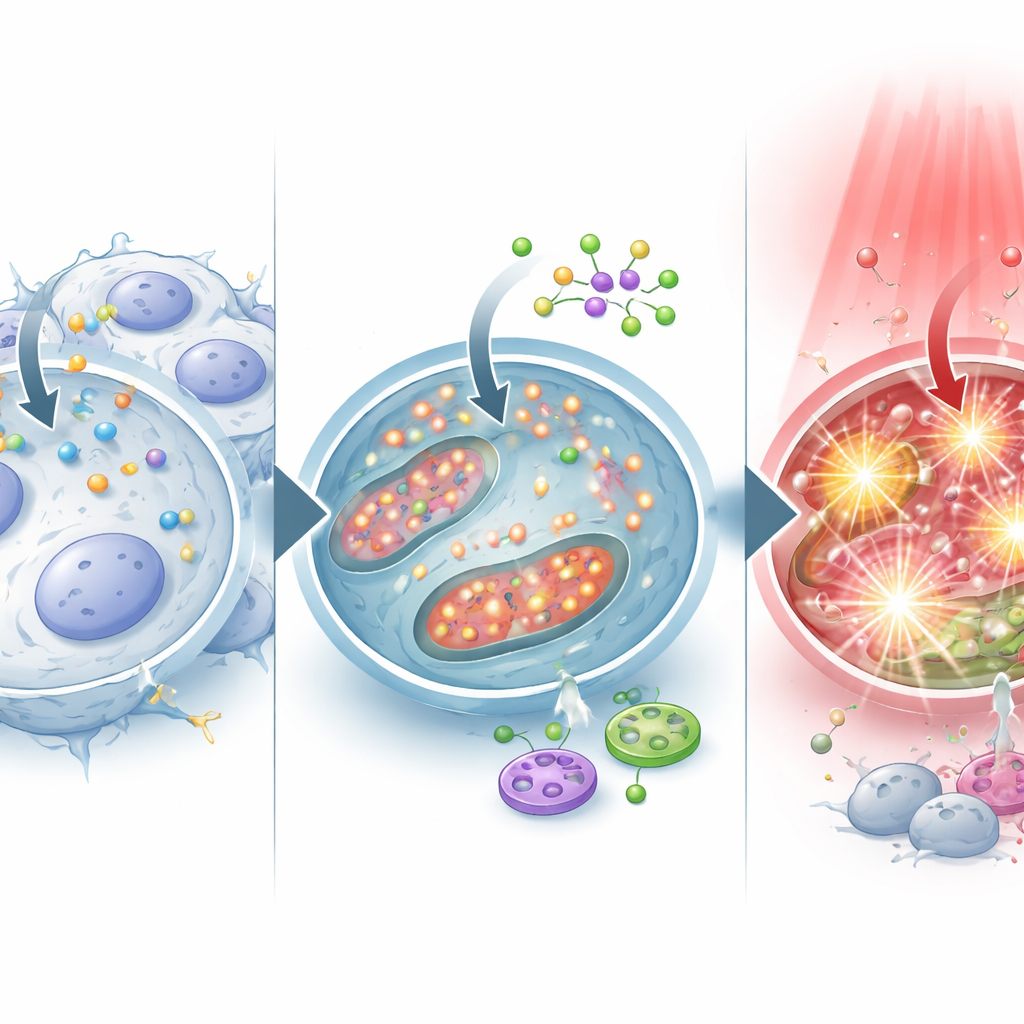
ماذا قد يعني هذا للعلاج في المستقبل
بعبارة مبسطة، تُظهر الدراسة أن إقران دواء منشط بالضوء بمركب نباتي يمكن أن يجعل خلايا سرطان المثانة، بما في ذلك الخلايا المقاومة للعلاج الكيميائي والخلايا الشبيهة بالجذعية، أسهل في التدمير في المختبر. البربامين لا يضر الخلايا الورمية بمفرده فحسب، بل يساعدها أيضًا على تحميل مزيد من الممسك الضوئي الذي يغذي العلاج الضوئي الديناميكي، ما يميل بالميزان نحو ضرر أكسدي مميت عند تطبيق الضوء الأحمر. تركيبة الجرعات الدقيقة مهمة وتعتمد على بيولوجيا كل ورم، لكن مفهوم "ضبط" العلاج الضوئي بمساعد حساس منخفض التكلفة واعد. العمل أُجري في أطباق خلوية وليس على مرضى، لذا فهو لا يثبت بعد فائدة سريرية لدى البشر. ومع ذلك، يشير إلى مستقبل قد تُفَحَص فيه أورام المثانة، خصوصًا التي تفوقت على الأدوية القياسية، من حيث حساسيتها لـ5-ALA-PDT مع البربامين ثم تُعالج بتوليفة مصممة تستهدف حتى أصعب بذور السرطان.
الاستشهاد: Kabus, M., Aumiller, M., Rühm, A. et al. Combining 5-ALA-PDT with berbamine as an in vitro multimodal therapy approach against bladder cancer cells. Sci Rep 16, 11228 (2026). https://doi.org/10.1038/s41598-026-46092-x
الكلمات المفتاحية: سرطان المثانة, العلاج الضوئي الديناميكي, البربامين, مقاومة السيسبلاتين, خلايا جذعية سرطانية