Clear Sky Science · sv
Förutsägelse av kirurgiskt utfall vid läkemedelsresistent epilepsi genom att kombinera interiktala biomarkörer inom ett maskininlärningsramverk
Varför denna forskning är viktig för familjer med epilepsi
För barn vars anfall inte svarar på läkemedel kan hjärnkirurgi erbjuda hopp om ett liv fritt från anfall. Kirurger måste ändå fatta ett avgörande beslut: vilka små hjärnområden som ska tas bort samtidigt som friska delar sparas. Denna studie undersöker hur datoralgoritmer kan sålla i rutinmässiga hjärnregistreringar tagna mellan anfall för att bättre vägleda det valet och hjälpa till att förutsäga vilka barn som sannolikt får mest nytta av operationen.
Letar efter ledtrådar mellan anfall
Traditionellt förlitar sig läkare på hjärnaktivitet registrerad under ett verkligt anfall för att uppskatta den epileptogena zonen, det område som antas utlösa anfall. Att fånga tillräckligt många anfall kan dock kräva dagars sjukhusövervakning och kan ändå missa avgörande regioner. Författarna fokuserar istället på interiktala data, de elektriska signaler som registreras när inget anfall pågår. Dessa tysta intervall innehåller korta onormala händelser kallade spikar och ripplar som kan ge en fingervisning om var anfallen börjar, men varje typ för sig är ofta för oprecis för att vägleda kirurgi. Teamet ville se om kombinationen av många egenskaper hos spikar och ripplar tillsammans med maskininlärning kunde skärpa bilden.
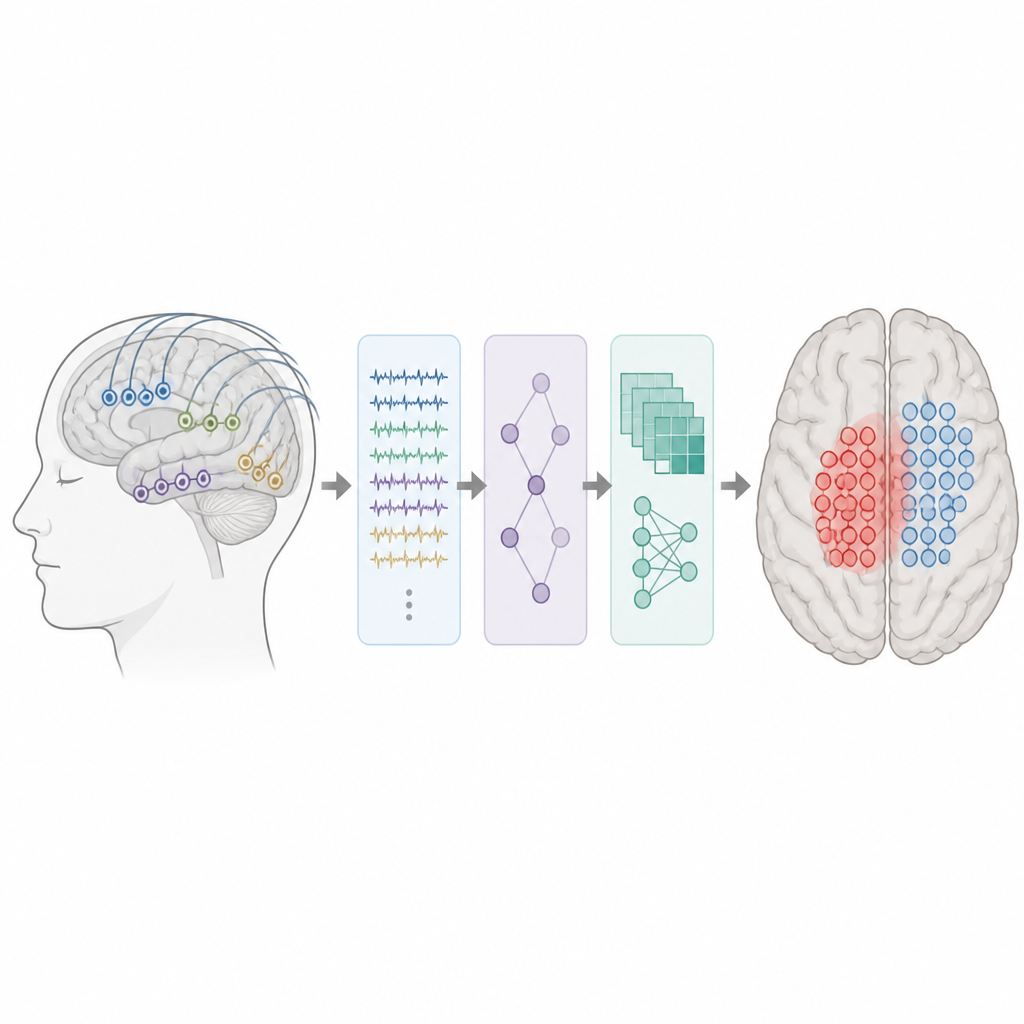
Omvandla komplexa hjärnsignaler till användbara egenskaper
Forskarna analyserade hjärnregistreringar från 62 barn och unga vuxna med läkemedelsresistent fokal epilepsi som genomgick invasiv övervakning med elektroder placerade direkt på eller i hjärnan. Alla hade minst fem minuter ren, interiktal data och minst ett års uppföljning efter operation. Automatiska detektorer skannade först registreringarna efter spikar och ripplar. För varje elektrod mätte teamet sedan hur ofta dessa händelser inträffade, hur kraftfulla de var, hur de spreds över närliggande elektroder och hur nära varje kontakt låg till händelseinkomster och hotspots. Totalt skapade de en uppsättning temporala, spektrala och spatiala egenskaper som beskriver lokal excitabilitet och hur onormal aktivitet propagerar genom hjärnan.
Träna maskiner på framgångsrika operationer
För att lära sitt system hur verkligt epileptogent vävnad ser ut använde författarna endast patienter som blev anfallsfria efter operation. För dessa barn innehöll troligen den vävnad som avlägsnats eller ablaterats den kritiska anfallsframkallande zonen. Varje elektrod inom denna resektion märktes som epileptogen, och de utanför som icke-epileptogena. Med dessa etiketter tränade teamet Random Forest-klassificerare, en typ av maskininlärningsmodell, på tre olika indata: endast spikbaserade egenskaper, endast ripple-baserade egenskaper eller en kombination av alla spik- och ripple-egenskaper. Modellerna lärde sig mönster som särskiljer epileptogena kontakter från övriga och producerade sedan en förutsagd epileptogen zon för varje patient.
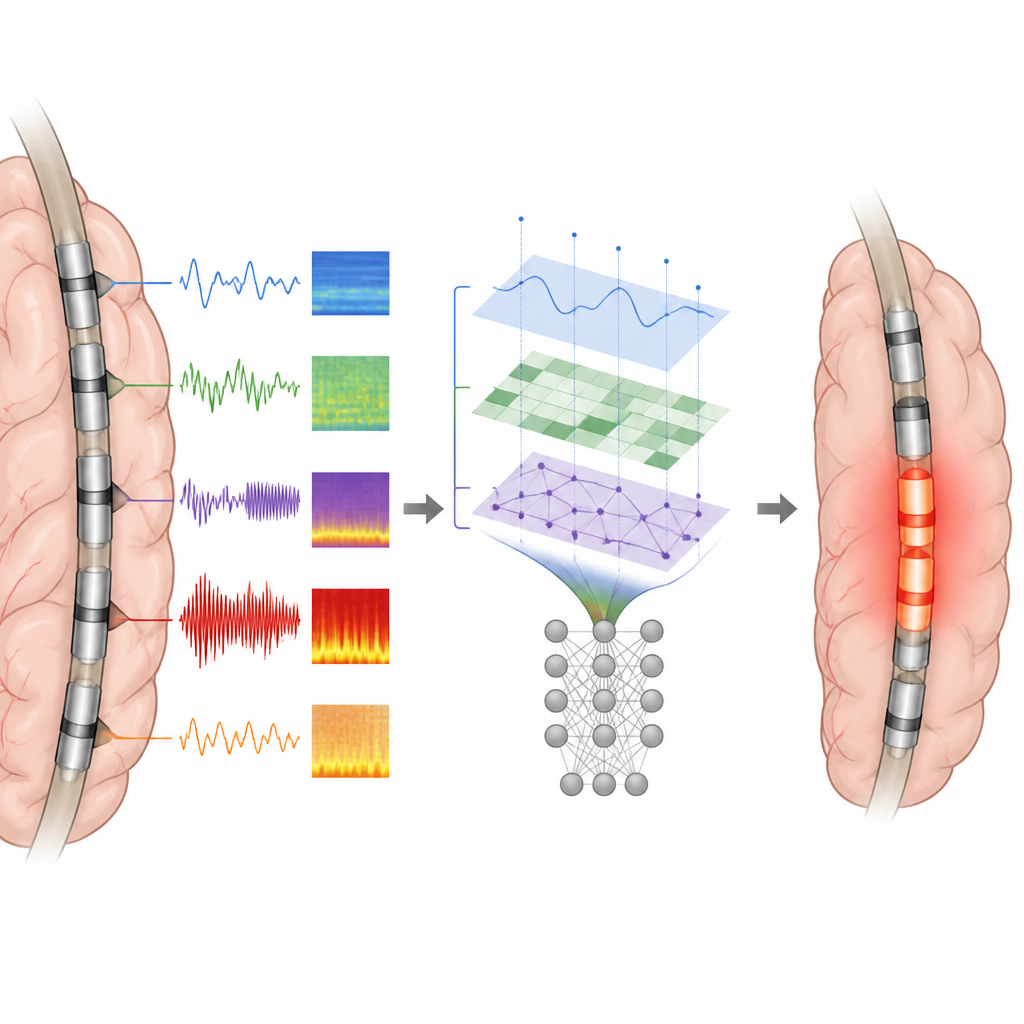
Hur väl modellerna överensstämde med verkliga operationer
När de testades presterade modeller baserade på spike-egenskaper och på kombinerade spike plus ripple-egenskaper bäst. De skiljde korrekt mellan epileptogena och icke-epileptogena kontakter med hög noggrannhet, och deras predicerade zoner överlappade ungefär tre fjärdedelar av den faktiska resektionen hos de anfallsfria patienterna. Däremot var de flesta enskilda mått, såsom enbart spike-frekvens, mindre pålitliga. En viktig slutsats var att den exakta spatiala fördelningen av spikar, särskilt hur nära en elektrod låg till den tidigaste eller starkaste aktiviteten, gav rikare information än att bara räkna händelser. Ripple-egenskaper bidrog endast med måttliga förbättringar utöver spikar, möjligen eftersom ripplar också kan förekomma i friska hjärnområden.
Koppla förutsägelser till verkliga utfall
Teamet ställde sedan en praktisk fråga: om åtminstone hälften av den predicerade epileptogena zonen låg inom den vävnad som en kirurg avlägsnat, tenderade patienten då att klara sig bra? Med hjälp av den kombinerade egenskapsmodellen identifierade denna enkla regel anfallsfria barn med en sensitivitet på 88 procent och en specificitet på 68 procent, vilket överträffade den traditionella anfallstartszonen definierad av specialister. Hos patienter som fortsatte att ha anfall låg den predicerade zonen ofta delvis eller till stor del utanför det resecerade området, vilket tyder på att viktig epileptogen vävnad hade missats eller inte kunde avlägsnas säkert.
Vad detta kan innebära för framtida epilepsivård
För familjer som står inför epilepsikirurgi antyder detta arbete att några minuters hjärnregistrering mellan anfall en dag kan hjälpa kirurger att planera operationer mer precist och uppskatta chanserna för framgång. Metoden behöver fortfarande prospektiv testning i större och mer homogena patientgrupper, men visar att kombinationen av flera subtila egenskaper hos hjärnaktivitet med maskininlärning kan ge en klarare, mer objektiv bild av var anfall uppstår och hur fullständigt operationen riktat in sig på dessa regioner.
Citering: Partamian, H., Jahromi, S., Perry, M.S. et al. Predicting surgical outcome in drug-resistant epilepsy by combining interictal biomarkers within a machine learning framework. Sci Rep 16, 15166 (2026). https://doi.org/10.1038/s41598-026-45177-x
Nyckelord: epilepsikirurgi, interiktal EEG, maskininlärning, pediatrisk epilepsi, epileptogen zon