Clear Sky Science · es
Predicción del resultado quirúrgico en epilepsia farmacorresistente combinando biomarcadores interictales mediante aprendizaje automático
Por qué esta investigación importa para las familias con epilepsia
Para los niños cuyas crisis no responden a la medicación, la cirugía cerebral puede ofrecer la esperanza de una vida sin convulsiones. Sin embargo, los cirujanos deben tomar una decisión crítica: qué pequeñas regiones de tejido cerebral eliminar preservando al mismo tiempo las áreas sanas. Este estudio explora cómo los algoritmos informáticos pueden procesar las grabaciones cerebrales de rutina tomadas entre crisis para orientar mejor esa decisión y ayudar a predecir qué niños tienen más probabilidades de beneficiarse de la cirugía.
Buscando pistas entre las crisis
Tradicionalmente, los médicos se basan en la actividad cerebral registrada durante una crisis para estimar la zona epileptógena, el área que se piensa que desencadena las convulsiones. Sin embargo, captar suficientes crisis puede requerir días de monitorización hospitalaria y aun así pasar por alto regiones cruciales. Los autores se centran en cambio en los datos interictales, las señales eléctricas registradas cuando no hay una crisis en curso. Estos intervalos silenciosos contienen eventos breves y anormales llamados picos y ráfagas que pueden indicar dónde comienzan las convulsiones, pero cada tipo por sí solo suele ser demasiado impreciso para guiar la cirugía. El equipo se propuso averiguar si combinar muchas propiedades de picos y ráfagas con aprendizaje automático podía aclarar mejor este panorama.
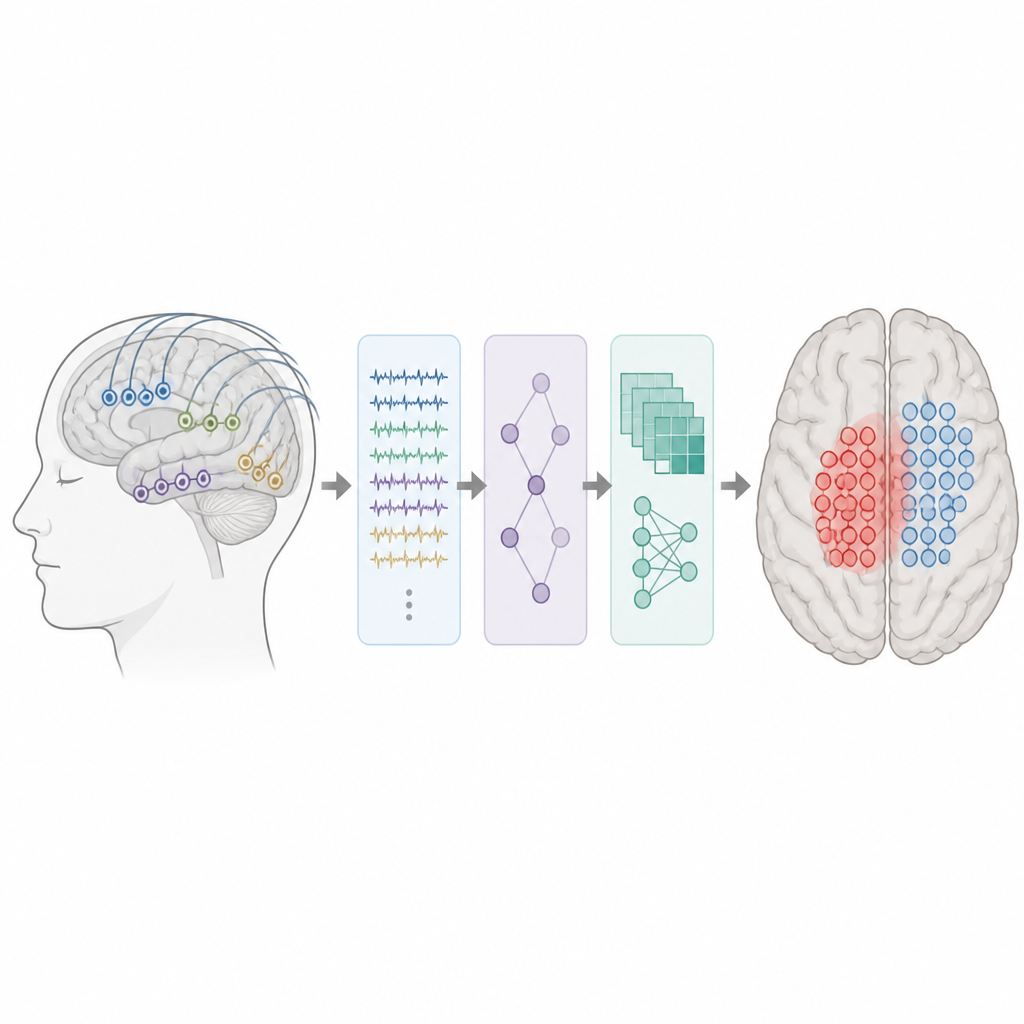
Convertir señales cerebrales complejas en características útiles
Los investigadores analizaron grabaciones cerebrales de 62 niños y jóvenes adultos con epilepsia focal farmacorresistente que se sometieron a monitorización invasiva con electrodos colocados directamente sobre o dentro del cerebro. Todos disponían de al menos cinco minutos de datos interictales limpios y al menos un año de seguimiento tras la cirugía. Detectores automatizados escanearon primero las grabaciones en busca de picos y ráfagas. Para cada electrodo, el equipo midió luego con qué frecuencia ocurrían estos eventos, cuán intensos eran, cómo se propagaban por electrodos vecinos y qué tan cerca estaba cada contacto de los inicios de los eventos y de los puntos calientes. En total, crearon un conjunto de características temporales, espectrales y espaciales que describen la excitabilidad local y cómo la actividad anómala se propaga por el cerebro.
Entrenar máquinas con cirugías exitosas
Para enseñar a su sistema cómo es realmente el tejido epileptógeno, los autores utilizaron únicamente pacientes que quedaron libres de crisis tras la cirugía. Para estos niños, el tejido que se había extirpado o ablacionado contenía muy probablemente la zona crítica generadora de convulsiones. Cada electrodo dentro de esta resección se etiquetó como epileptógeno, y los situados fuera como no epileptógenos. Con estas etiquetas, el equipo entrenó clasificadores Random Forest, un tipo de modelo de aprendizaje automático, con tres entradas diferentes: características basadas solo en picos, características basadas solo en ráfagas, o una combinación de todas las características de picos y ráfagas. Los modelos aprendieron patrones que distinguen los contactos epileptógenos del resto y luego produjeron una zona epileptógena predicha para cada paciente.
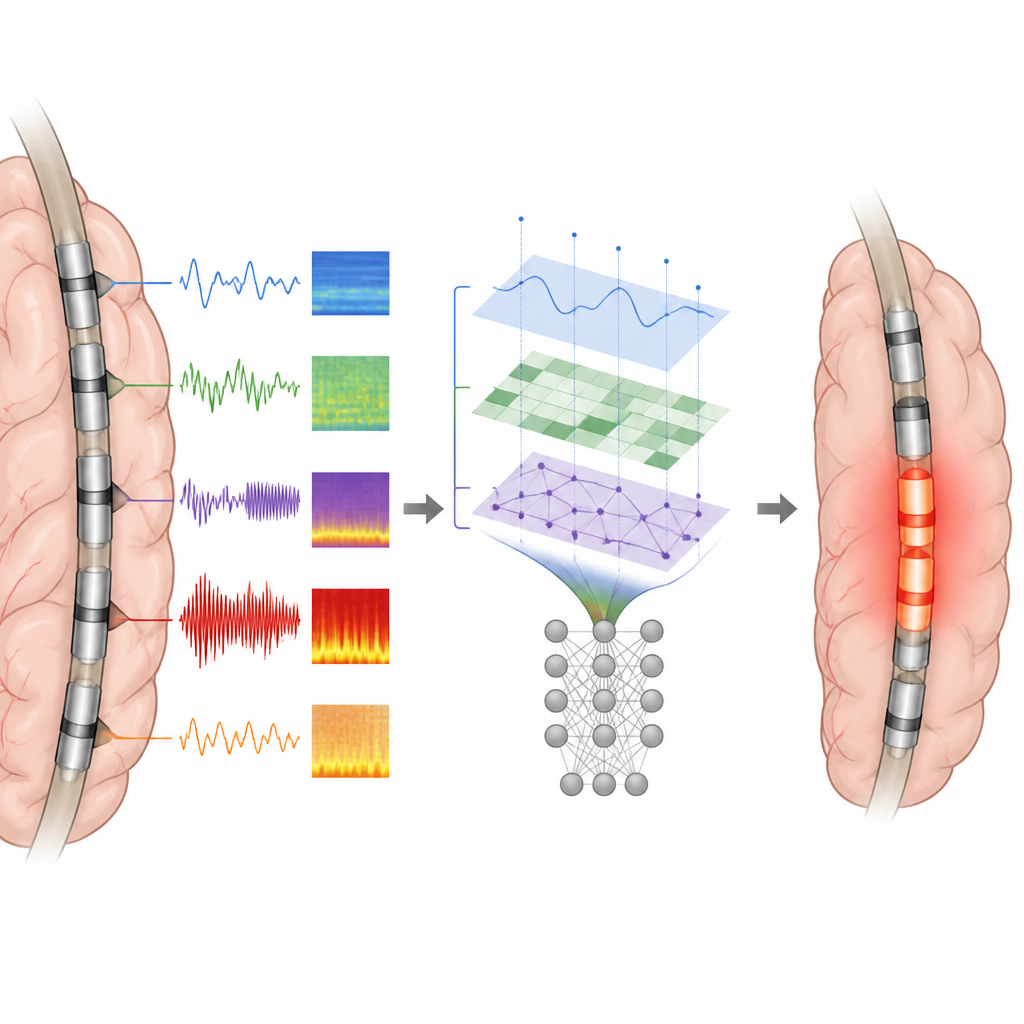
Qué tan bien coincidieron los modelos con las cirugías reales
Al evaluarlos, los modelos basados en características de picos y los que combinaban picos y ráfagas fueron los que mejor funcionaron. Separaron correctamente los contactos epileptógenos de los no epileptógenos con alta precisión, y sus zonas predichas se solaparon con aproximadamente tres cuartas partes de la resección real en los pacientes libres de crisis. En contraste, la mayoría de las mediciones individuales, como la tasa de picos por sí sola, fueron menos fiables. Un hallazgo importante fue que la disposición espacial exacta de los picos, especialmente qué tan cerca estaba un electrodo de la actividad más temprana o más intensa, proporcionó información más rica que el mero recuento de eventos. Las características de las ráfagas añadieron solo ganancias modestas más allá de los picos, quizá porque las ráfagas también pueden aparecer en regiones cerebrales sanas.
Conectar las predicciones con los resultados reales
El equipo planteó entonces una pregunta práctica: si al menos la mitad de la zona epileptógena predicha estaba dentro del tejido que el cirujano extirpó, ¿tendía el paciente a evolucionar bien? Usando el modelo de características combinadas, esta regla simple identificó a niños libres de crisis con una sensibilidad del 88 por ciento y una especificidad del 68 por ciento, superando a la zona de inicio de crisis tradicional definida por especialistas. En los pacientes que siguieron teniendo convulsiones, la zona predicha a menudo se encontraba parcial o mayoritariamente fuera de la región resecada, lo que sugiere que se había pasado por alto tejido epileptógeno importante o que no pudo extirparse de forma segura.
Qué podría significar esto para la futura atención de la epilepsia
Para las familias que enfrentan la posibilidad de una cirugía de epilepsia, este trabajo sugiere que unos pocos minutos de registro cerebral entre crisis podrían algún día ayudar a los cirujanos a planificar operaciones con mayor precisión y a estimar las probabilidades de éxito. Aunque el enfoque aún requiere ensayos prospectivos en grupos de pacientes más grandes y homogéneos, demuestra que combinar múltiples características sutiles de la actividad cerebral con aprendizaje automático puede ofrecer una visión más clara y objetiva de dónde se originan las crisis y de cuánto ha abordado la cirugía esas regiones.
Cita: Partamian, H., Jahromi, S., Perry, M.S. et al. Predicting surgical outcome in drug-resistant epilepsy by combining interictal biomarkers within a machine learning framework. Sci Rep 16, 15166 (2026). https://doi.org/10.1038/s41598-026-45177-x
Palabras clave: cirugía de epilepsia, EEG interictal, aprendizaje automático, epilepsia pediátrica, zona epileptógena