Clear Sky Science · de
Vorhersage des Operationsergebnisses bei medikamentenresistenter Epilepsie durch Kombination interiktaler Biomarker in einem maschinellen Lernrahmen
Warum diese Forschung für Familien mit Epilepsie wichtig ist
Für Kinder, deren Anfälle nicht auf Medikamente ansprechen, kann eine Gehirnoperation die Hoffnung auf ein anfallsfreies Leben bieten. Chirurgen stehen dabei jedoch vor einer entscheidenden Frage: Welche kleinen Hirnareale sollen entfernt werden, während gesundes Gewebe geschont wird. In dieser Studie wird untersucht, wie Computeralgorithmen routinemäßige Hirnaufzeichnungen zwischen Anfällen durchsuchen können, um diese Entscheidung besser zu unterstützen und vorherzusagen, welche Kinder am ehesten von einer Operation profitieren.
Auf der Suche nach Hinweisen zwischen Anfällen
Traditionell verlassen sich Ärzte auf die Hirnaktivität, die während eines tatsächlichen Anfalls aufgezeichnet wird, um die epileptogene Zone zu schätzen — das Gebiet, das Anfälle auszulösen scheint. Ausreichend viele Anfälle zu erfassen kann jedoch Tage der Überwachung im Krankenhaus erfordern und dennoch wichtige Regionen übersehen. Die Autoren konzentrieren sich stattdessen auf interiktale Daten, also elektrische Signale, die aufgezeichnet werden, wenn kein Anfall stattfindet. Diese ruhigen Intervalle enthalten kurze abnorme Ereignisse, sogenannte Spikes und Ripples, die einen Hinweis darauf geben können, wo Anfälle beginnen. Allein sind diese Signale jedoch oft zu ungenau, um als Operationsleitsatz zu dienen. Das Team prüfte, ob die Kombination vieler Eigenschaften von Spikes und Ripples zusammen mit maschinellem Lernen dieses Bild schärfen kann.
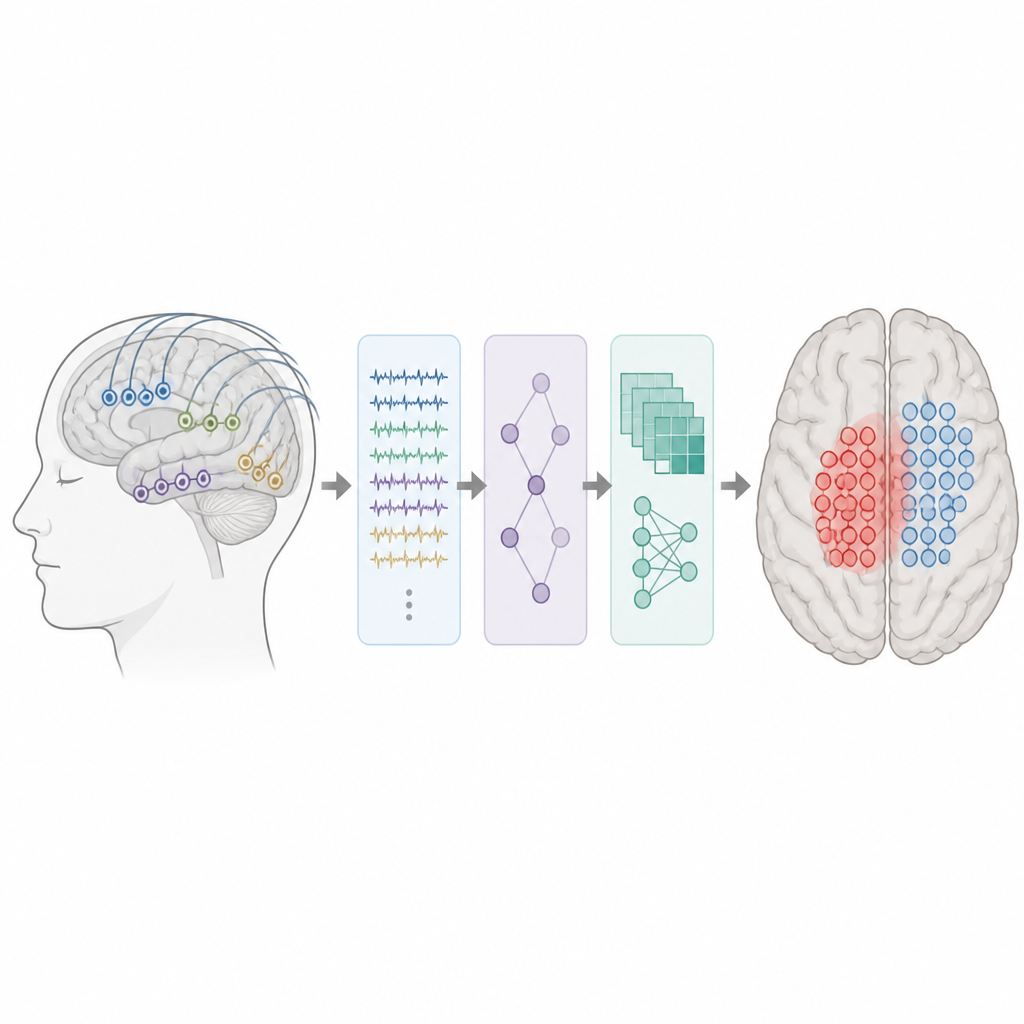
Komplexe Hirnsignale in nutzbare Merkmale verwandeln
Die Forscher analysierten Hirnaufzeichnungen von 62 Kindern und jungen Erwachsenen mit medikamentenresistenter fokaler Epilepsie, die eine invasive Überwachung mit direkt auf oder im Gehirn platzierten Elektroden erhielten. Alle verfügten über mindestens fünf Minuten sauberer interiktaler Daten und mindestens ein Jahr Nachbeobachtung nach der Operation. Automatisierte Detektoren durchsuchten zunächst die Aufzeichnungen nach Spikes und Ripples. Für jede Elektrode maß das Team dann, wie häufig diese Ereignisse auftraten, wie stark sie waren, wie sie sich über benachbarte Elektroden ausbreiteten und wie nah jeder Kontakt an Ereignisbeginn und Hotspots lag. Insgesamt erstellten sie einen Satz zeitlicher, spektraler und räumlicher Merkmale, die die lokale Erregbarkeit und die Ausbreitung abnormer Aktivität im Gehirn beschreiben.
Maschinen auf erfolgreiche Operationen trainieren
Um dem System beizubringen, wie tatsächlich epileptogenes Gewebe aussieht, verwendeten die Autoren nur Patienten, die nach der Operation anfallsfrei wurden. Bei diesen Kindern enthielt das entfernte oder ablatierte Gewebe sehr wahrscheinlich die kritische Anfalls erzeugende Zone. Jede Elektrode innerhalb dieser Resektion wurde als epileptogen etikettiert, und solche außerhalb als nicht epileptogen. Mit diesen Labels trainierte das Team Random-Forest-Klassifikatoren, eine Art Modell des maschinellen Lernens, anhand von drei verschiedenen Eingaben: nur spike-basierte Merkmale, nur ripple-basierte Merkmale oder eine Kombination aller Spike- und Ripple-Merkmale. Die Modelle lernten Muster, die epileptogene Kontakte von anderen unterscheiden, und erstellten anschließend für jeden Patienten eine vorhergesagte epileptogene Zone.
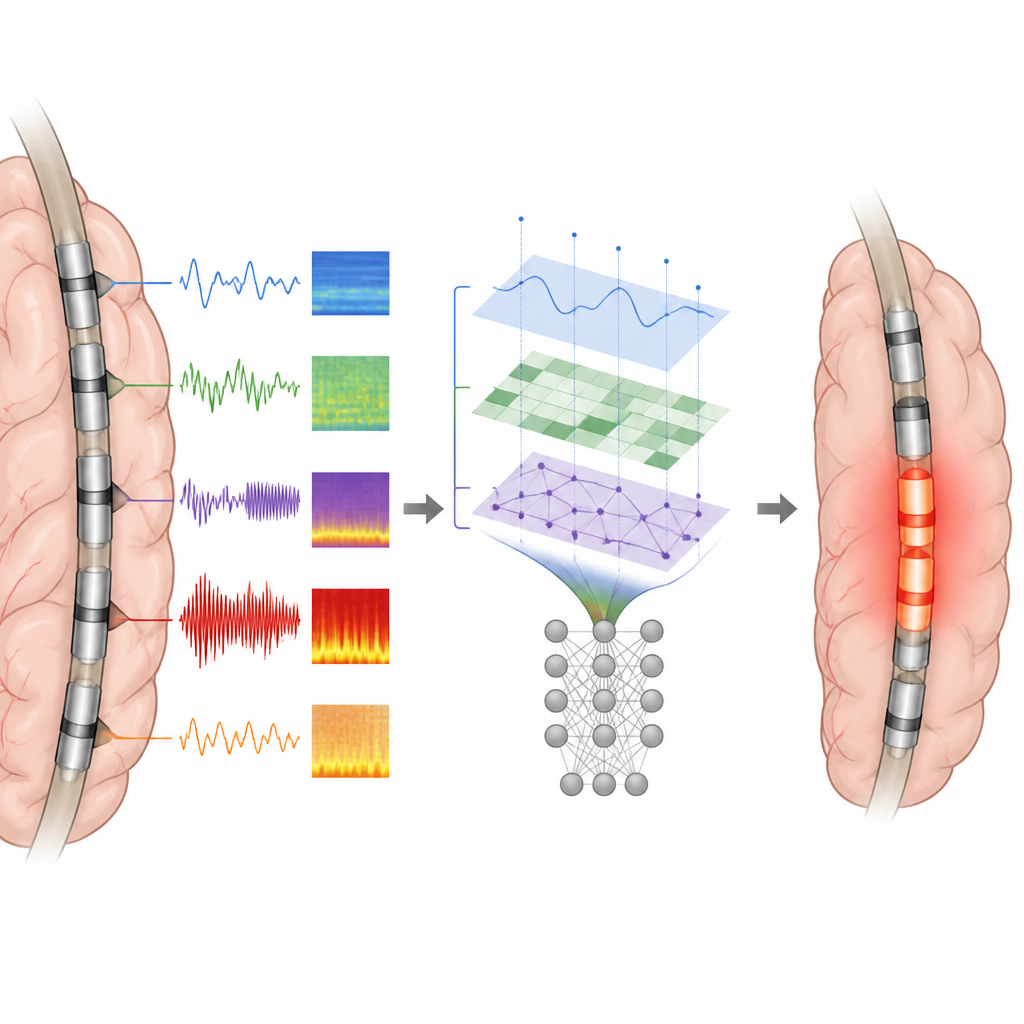
Wie gut die Modelle mit realen Operationen übereinstimmten
Bei Tests erzielten Modelle, die auf Spike-Merkmalen bzw. auf kombinierten Spike‑plus‑Ripple‑Merkmalen basierten, die besten Ergebnisse. Sie trennten epileptogene von nicht epileptogenen Kontakten mit hoher Genauigkeit, und ihre vorhergesagten Zonen überlappten etwa drei Viertel der tatsächlichen Resektion bei anfallsfreien Patienten. Im Gegensatz dazu waren die meisten Einzelmessungen, wie etwa die reine Spikerate, weniger zuverlässig. Eine wichtige Erkenntnis war, dass die genaue räumliche Anordnung der Spikes — insbesondere wie nahe eine Elektrode an der frühesten oder stärksten Aktivität lag — reichere Informationen lieferte als bloße Ereigniszahlen. Ripple-Merkmale brachten nur bescheidene zusätzliche Verbesserungen gegenüber Spikes, möglicherweise weil Ripples auch in gesunden Hirnregionen auftreten können.
Verbindung von Vorhersagen mit klinischen Ergebnissen
Die Forscher stellten dann eine praktische Frage: Wenn mindestens die Hälfte der vorhergesagten epileptogenen Zone innerhalb des vom Chirurgen entfernten Gewebes lag, ging es dem Patienten dann tendenziell gut? Mithilfe des kombinierten Merkmalsmodells identifizierte diese einfache Regel anfallsfreie Kinder mit einer Sensitivität von 88 Prozent und einer Spezifität von 68 Prozent und übertraf damit die traditionelle, von Spezialisten definierte Anfallsausgangszone. Bei Patienten, die weiterhin Anfälle hatten, lag die vorhergesagte Zone häufig teilweise oder überwiegend außerhalb des resezierten Bereichs, was darauf hindeutet, dass wichtiges epileptogenes Gewebe übersehen oder nicht sicher entfernt werden konnte.
Was dies für die zukünftige Epilepsieversorgung bedeuten könnte
Für Familien, die sich mit der Aussicht auf eine Epilepsieoperation konfrontiert sehen, deutet diese Arbeit darauf hin, dass wenige Minuten Hirnaufzeichnung zwischen Anfällen eines Tages Chirurgen helfen könnten, Operationen präziser zu planen und die Erfolgsaussichten besser einzuschätzen. Obwohl der Ansatz noch prospektive Tests in größeren und homogeneren Patientengruppen benötigt, zeigt er, dass die Kombination mehrerer subtiler Merkmale der Hirnaktivität mit maschinellem Lernen ein klareres, objektiveres Bild davon liefern kann, wo Anfälle entstehen und wie vollständig die Operation diese Regionen erfasst hat.
Zitation: Partamian, H., Jahromi, S., Perry, M.S. et al. Predicting surgical outcome in drug-resistant epilepsy by combining interictal biomarkers within a machine learning framework. Sci Rep 16, 15166 (2026). https://doi.org/10.1038/s41598-026-45177-x
Schlüsselwörter: Epilepsiechirurgie, interiktales EEG, maschinelles Lernen, pädiatrische Epilepsie, epileptogene Zone