Clear Sky Science · pt
Previsão do resultado cirúrgico na epilepsia farmacorresistente combinando biomarcadores interictais em um framework de aprendizado de máquina
Por que esta pesquisa importa para famílias com epilepsia
Para crianças cujas crises não respondem a medicamentos, a cirurgia cerebral pode oferecer a esperança de uma vida sem convulsões. Ainda assim, os cirurgiões enfrentam uma decisão crítica: quais pequenas regiões de tecido cerebral remover preservando as áreas saudáveis. Este estudo explora como algoritmos computacionais podem analisar gravações cerebrais rotineiras feitas entre crises para orientar melhor essa escolha e ajudar a prever quais crianças têm maior probabilidade de se beneficiar da cirurgia.
Procurando pistas entre as crises
Tradicionalmente, os médicos dependem da atividade cerebral registrada durante uma crise para estimar a zona epileptogênica, a área considerada responsável por desencadear as crises. Capturar crises suficientes, porém, pode exigir dias de monitoramento hospitalar e ainda assim deixar de identificar regiões cruciais. Os autores, em vez disso, focam em dados interictais, os sinais elétricos registrados quando não há uma crise em curso. Esses intervalos silenciosos contêm eventos breves e anormais chamados picos e ripples que podem indicar onde as crises começam, mas cada tipo isolado costuma ser impreciso para orientar a cirurgia. A equipe investigou se combinar muitas propriedades de picos e ripples com aprendizado de máquina poderia afinar esse quadro.
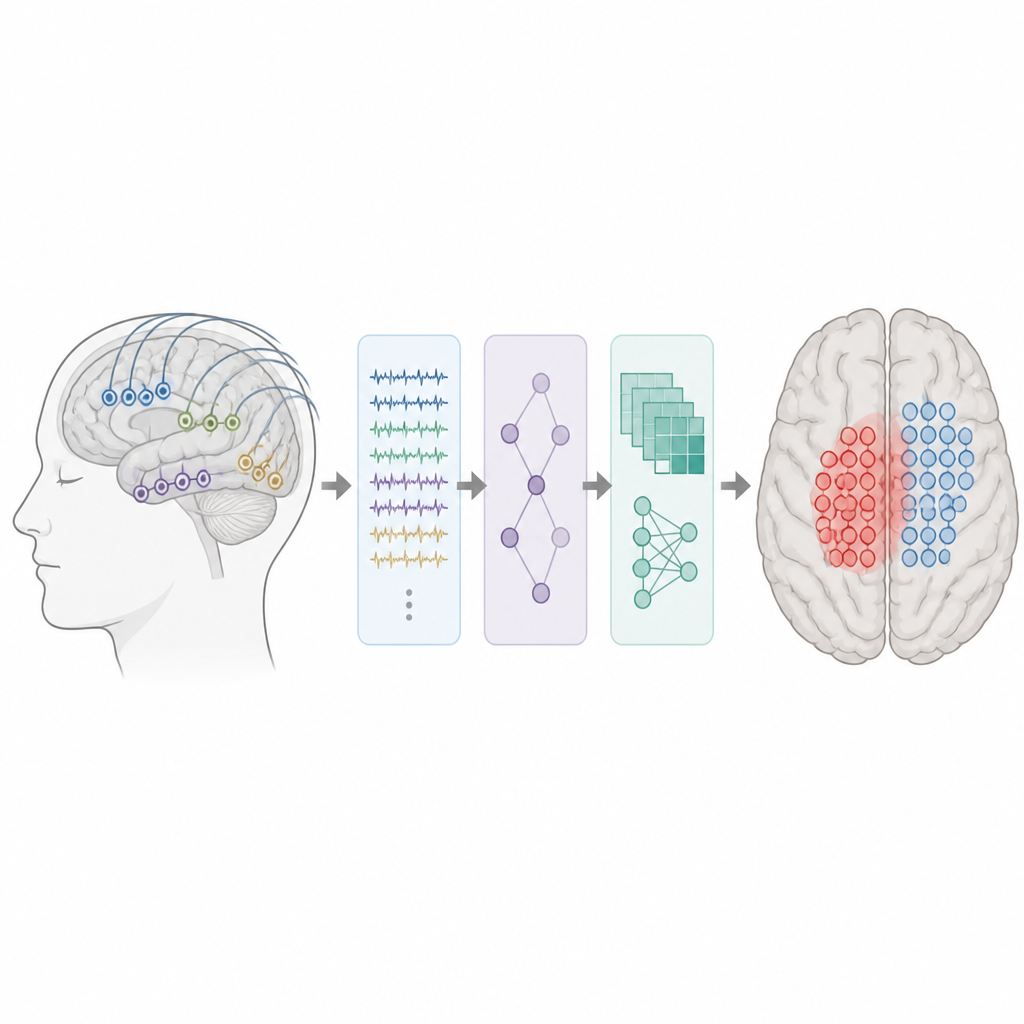
Transformando sinais cerebrais complexos em características úteis
Os pesquisadores analisaram gravações cerebrais de 62 crianças e jovens adultos com epilepsia focal farmacorresistente submetidos a monitoramento invasivo com eletrodos colocados diretamente sobre ou dentro do cérebro. Todos tinham pelo menos cinco minutos de dados interictais limpos e pelo menos um ano de acompanhamento pós‑operatório. Detectores automatizados primeiro vasculharam as gravações em busca de picos e ripples. Para cada eletrodo, a equipe então mediu com que frequência esses eventos ocorriam, quão fortes eram, como se espalhavam para eletrodos vizinhos e quão próximo cada contato estava dos inícios de evento e de hotspots. No total, criaram um conjunto de características temporais, espectrais e espaciais descrevendo a excitabilidade local e como a atividade anormal se propagava pelo cérebro.
Treinando máquinas com cirurgias bem‑sucedidas
Para ensinar ao sistema como é o tecido realmente epileptogênico, os autores utilizaram apenas pacientes que ficaram livres de crises após a cirurgia. Para essas crianças, o tecido removido ou ablacionado provavelmente continha a zona geradora crítica das crises. Cada eletrodo dentro dessa ressecção foi rotulado como epileptogênico, e os fora dela como não epileptogênicos. Usando esses rótulos, a equipe treinou classificadores Random Forest, um tipo de modelo de aprendizado de máquina, com três entradas diferentes: características baseadas apenas em picos, características baseadas apenas em ripples, ou uma combinação de todas as características de picos e ripples. Os modelos aprenderam padrões que distinguem contatos epileptogênicos dos demais e então produziram uma zona epileptogênica prevista para cada paciente.
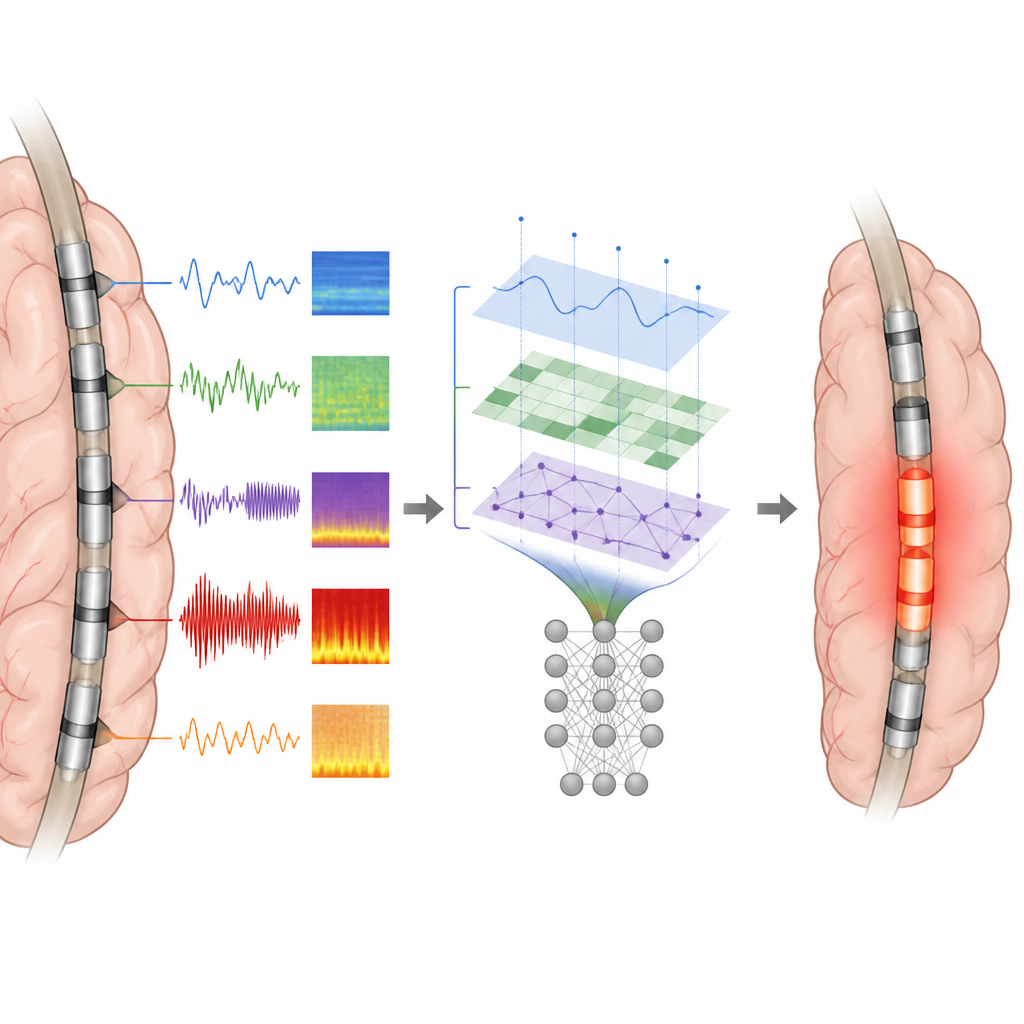
Quão bem os modelos corresponderam às cirurgias reais
Ao serem testados, os modelos baseados em características de picos e os modelos combinados de picos mais ripples foram os melhores. Eles separaram corretamente contatos epileptogênicos de não epileptogênicos com alta precisão, e suas zonas previstas sobrepuseram cerca de três quartos da ressecção real em pacientes livres de crises. Em contraste, a maioria das medidas isoladas, como taxa de picos sozinha, foi menos confiável. Um achado importante foi que a disposição espacial exata dos picos, especialmente a proximidade de um eletrodo em relação à atividade mais precoce ou mais forte, forneceu informações mais ricas do que a simples contagem de eventos. As características de ripple acrescentaram apenas ganhos modestos além dos picos, possivelmente porque ripples também podem aparecer em regiões cerebrais saudáveis.
Conectando previsões a desfechos na vida real
A equipe então fez uma pergunta prática: se pelo menos metade da zona epileptogênica prevista estivesse dentro do tecido removido pelo cirurgião, o paciente tendia a evoluir bem? Usando o modelo de características combinadas, essa regra simples identificou crianças livres de crises com sensibilidade de 88 por cento e especificidade de 68 por cento, superando a zona de início de crise tradicionalmente definida por especialistas. Em pacientes que continuaram a ter crises, a zona prevista frequentemente encontrava‑se em parte ou largamente fora da região ressecada, sugerindo que tecido epileptogênico importante havia sido omitido ou não pôde ser removido com segurança.
O que isso pode significar para o futuro do cuidado da epilepsia
Para famílias diante da perspectiva de cirurgia para epilepsia, este trabalho sugere que alguns minutos de gravação cerebral entre crises podem, um dia, ajudar cirurgiões a planejar operações com mais precisão e estimar as chances de sucesso. Embora a abordagem ainda precise de testes prospectivos em grupos maiores e mais homogêneos de pacientes, ela demonstra que combinar múltiplas características sutis da atividade cerebral com aprendizado de máquina pode oferecer uma visão mais clara e objetiva de onde as crises surgem e de quão completamente a cirurgia atingiu essas regiões.
Citação: Partamian, H., Jahromi, S., Perry, M.S. et al. Predicting surgical outcome in drug-resistant epilepsy by combining interictal biomarkers within a machine learning framework. Sci Rep 16, 15166 (2026). https://doi.org/10.1038/s41598-026-45177-x
Palavras-chave: cirurgia de epilepsia, EEG interictal, aprendizado de máquina, epilepsia pediátrica, zona epileptogênica