Clear Sky Science · pl
Przewidywanie wyników operacji u pacjentów z lekooporną padaczką poprzez łączenie międzynapadowych biomarkerów w ramach uczenia maszynowego
Dlaczego to badanie ma znaczenie dla rodzin dzieci z padaczką
Dla dzieci, u których napady nie reagują na leki, operacja mózgu może dać nadzieję na życie bez napadów. Chirurdzy muszą jednak podjąć kluczową decyzję: które drobne obszary tkanki mózgowej usunąć, jednocześnie oszczędzając zdrowe okolice. W tym badaniu sprawdzono, jak algorytmy komputerowe mogą przesiać rutynowe zapisy mózgu wykonywane między napadami, by lepiej poprowadzić ten wybór i pomóc przewidzieć, które dzieci najprawdopodobniej skorzystają z operacji.
Poszukiwanie wskazówek między napadami
Tradycyjnie lekarze polegają na aktywności mózgu zarejestrowanej podczas rzeczywistego napadu, aby oszacować strefę epileptogenną — obszar uważany za inicjujący napady. Zarejestrowanie wystarczającej liczby napadów może jednak wymagać dni monitorowania szpitalnego i nadal nie uchwycić kluczowych regionów. Autorzy skupili się zamiast tego na danych międzynapadowych, czyli sygnałach elektrycznych rejestrowanych, gdy napad nie występuje. Te spokojne odstępy zawierają krótkie nieprawidłowe zdarzenia zwane skokami (spikes) i riple’ami, które mogą wskazywać, gdzie zaczynają się napady, ale każdy z tych typów sam w sobie często jest zbyt nieprecyzyjny, by kierować operacją. Zespół postanowił sprawdzić, czy połączenie wielu właściwości skoków i riple’ów z uczeniem maszynowym może wyostrzyć ten obraz.
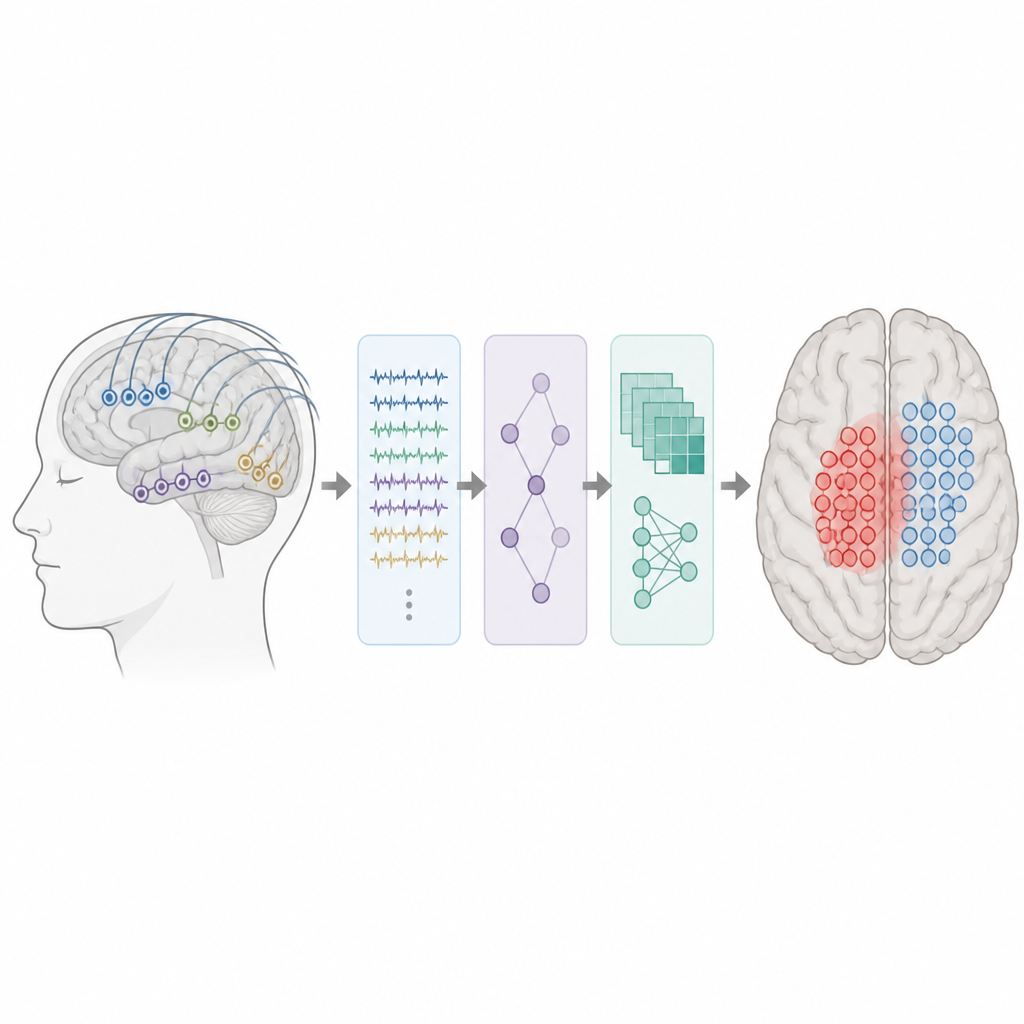
Przekształcanie złożonych sygnałów mózgowych w użyteczne cechy
Naukowcy przeanalizowali zapisy mózgowe od 62 dzieci i młodych dorosłych z lekooporną padaczką ogniskową, którzy przeszli inwazyjne monitorowanie z elektrodami umieszczonymi bezpośrednio na lub w mózgu. Wszyscy mieli co najmniej pięć minut czystych danych międzynapadowych i co najmniej roczny okres obserwacji po operacji. Automatyczne detektory najpierw przeszukały zapisy w poszukiwaniu skoków i riple’ów. Dla każdej elektrody zespół zmierzył, jak często występowały te zdarzenia, jak silne były, jak rozprzestrzeniały się na sąsiednie elektrody oraz jak blisko każdy kontakt leżał względem początku zdarzeń i tzw. gorących punktów. W sumie stworzono zestaw cech czasowych, spektralnych i przestrzennych opisujących lokalną pobudliwość oraz to, jak nieprawidłowa aktywność rozprzestrzenia się przez mózg.
Szkolenie algorytmów na podstawie udanych operacji
Aby nauczyć system, jak wygląda rzeczywiście epileptogenna tkanka, autorzy użyli tylko pacjentów, którzy po operacji pozostali bez napadów. U tych dzieci tkanka, która została usunięta lub zniszczona termicznie, najprawdopodobniej zawierała krytyczną strefę generującą napady. Każdą elektrodę wewnątrz tego resekcji oznaczono jako epileptogenną, a te na zewnątrz jako nieepileptogenne. Korzystając z tych oznaczeń, zespół wytrenował klasyfikatory Random Forest, rodzaj modelu uczenia maszynowego, na trzech różnych wejściach: tylko cechy oparte na skokach, tylko cechy riple’ów lub kombinację wszystkich cech skoków i riple’ów. Modele nauczyły się wzorców odróżniających kontakty epileptogenne od pozostałych, a następnie wygenerowały przewidywaną strefę epileptogenną dla każdego pacjenta.
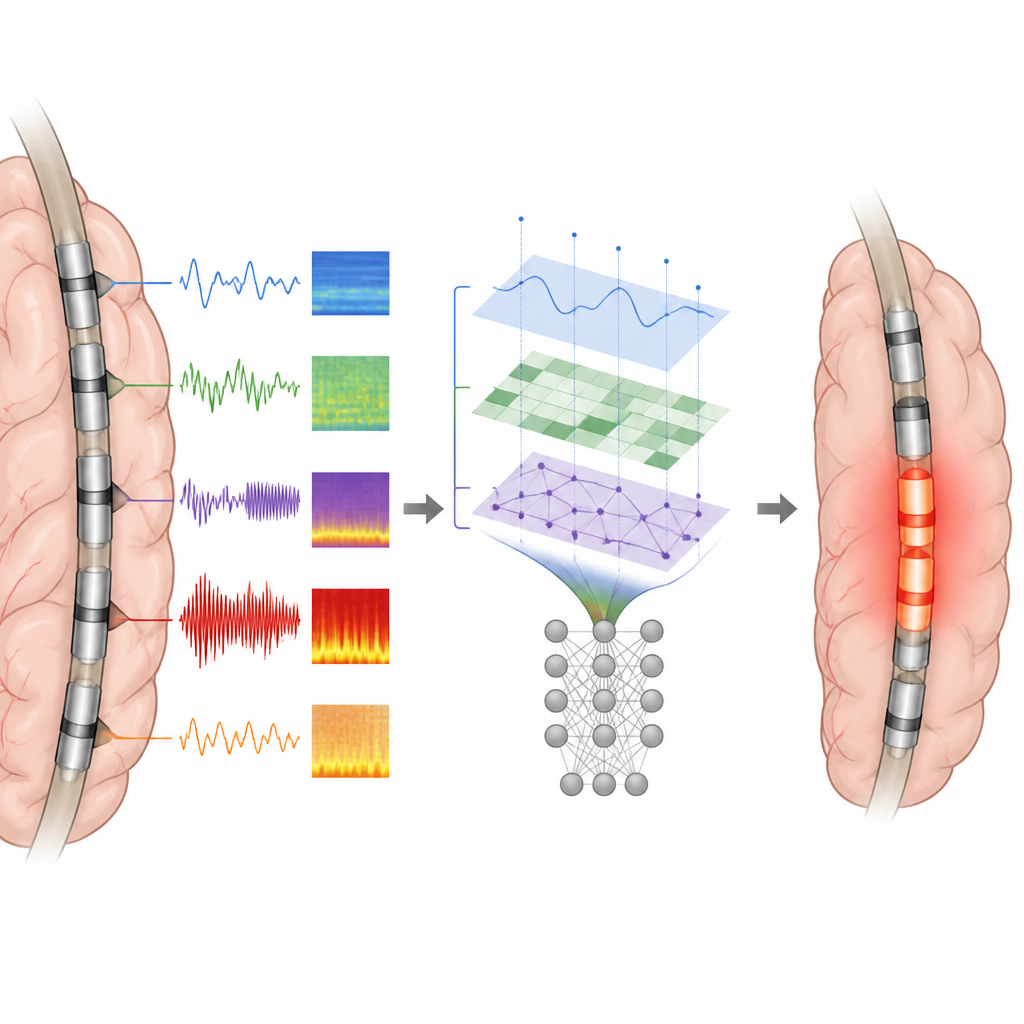
Jak dobrze modele odpowiadały rzeczywistym operacjom
W testach najlepiej wypadły modele oparte na cechach skoków oraz na połączonych cechach skoków i riple’ów. Poprawnie oddzielały kontakty epileptogenne od nieepileptogennych z wysoką dokładnością, a ich przewidywane strefy pokrywały około trzech czwartych faktycznej resekcji u pacjentów bez napadów. W przeciwieństwie do tego większość pojedynczych miar, takich jak sama częstość skoków, była mniej wiarygodna. Ważnym ustaleniem było to, że dokładne ułożenie przestrzenne skoków, szczególnie jak blisko elektroda znajdowała się do najwcześniejszej lub najsilniejszej aktywności, dostarczało bogatszych informacji niż same zliczenia zdarzeń. Cechy riple’ów dodały jedynie umiarkowane korzyści ponad skoki, prawdopodobnie dlatego, że riple mogą też pojawiać się w zdrowych rejonach mózgu.
Łączenie przewidywań z rzeczywistymi wynikami
Zespół postawił następnie praktyczne pytanie: czy jeśli co najmniej połowa przewidywanej strefy epileptogennej znajdowała się w tkance usuniętej przez chirurga, pacjent miał tendencję do dobrego wyniku? Korzystając z modelu łączącego cechy, ta prosta reguła zidentyfikowała dzieci bez napadów z czułością 88 procent i specyficznością 68 procent, przewyższając tradycyjnie definiowaną przez specjalistów strefę początku napadu. U pacjentów, którzy dalej doświadczali napadów, przewidywana strefa często leżała częściowo lub w dużej mierze poza resekcją, co sugeruje, że istotna tkanka epileptogenna została pominięta lub nie mogła być bezpiecznie usunięta.
Co to może oznaczać dla przyszłej opieki nad chorymi z padaczką
Dla rodzin stojących przed perspektywą operacji padaczki praca ta sugeruje, że kilka minut zapisu mózgu między napadami może pewnego dnia pomóc chirurgom precyzyjniej planować operacje i oszacować szanse powodzenia. Chociaż podejście wymaga jeszcze testów prospektywnych w większych i bardziej jednorodnych grupach pacjentów, pokazuje, że łączenie wielu subtelnych cech aktywności mózgowej z uczeniem maszynowym może dostarczyć jaśniejszego, bardziej obiektywnego obrazu miejsca, gdzie powstają napady, oraz tego, jak w pełni operacja objęła te obszary.
Cytowanie: Partamian, H., Jahromi, S., Perry, M.S. et al. Predicting surgical outcome in drug-resistant epilepsy by combining interictal biomarkers within a machine learning framework. Sci Rep 16, 15166 (2026). https://doi.org/10.1038/s41598-026-45177-x
Słowa kluczowe: operacja padaczki, międzynapadowe EEG, uczenie maszynowe, padaczka pediatryczna, strefa epileptogenna