Clear Sky Science · sv
Temperaturberoende öppningsvägar i TRPV3
Hur vår hud känner värme och kyla
Vår hud kan skilja ett varmt kärl från ett iskallt glas på ett ögonblick, tack vare små proteingatede porer i cellmembran som öppnar och stänger med temperaturen. En sådan port, kallad TRPV3, hjälper till att upptäcka värme och deltar i hudens biologiska funktioner. Denna studie ställer en enkel men djup fråga: förklarar samma grundläggande regler hur detta protein känner både värme och kyla, även när dess aktivitet senare slås av?
Två temperaturvägar till en sensor
TRPV3 är en fyrdelad proteinkanalen som sitter i cellmembranet och släpper igenom laddade atomer när den öppnas. Tidigare arbete har föreslagit att dess svar på värme kan beskrivas av en klassisk termodynamisk ekvation som kopplar temperaturförändringar till skiften i energi och värmekapacitet. Den ekvationen förutsäger att under rätt förhållanden bör samma kanal också reagera på nedkylning. TRPV3 är dock svårhanterlig eftersom den, när den aktiverats, kan inaktiveras — det vill säga kanalen slutar leda trots att stimulansen kvarstår. Författaren ville ta reda på om både de initiala varma och kalla svaren fortfarande följer samma energi- regel, trots dessa senare förändringar.
Att se kanalen byta form
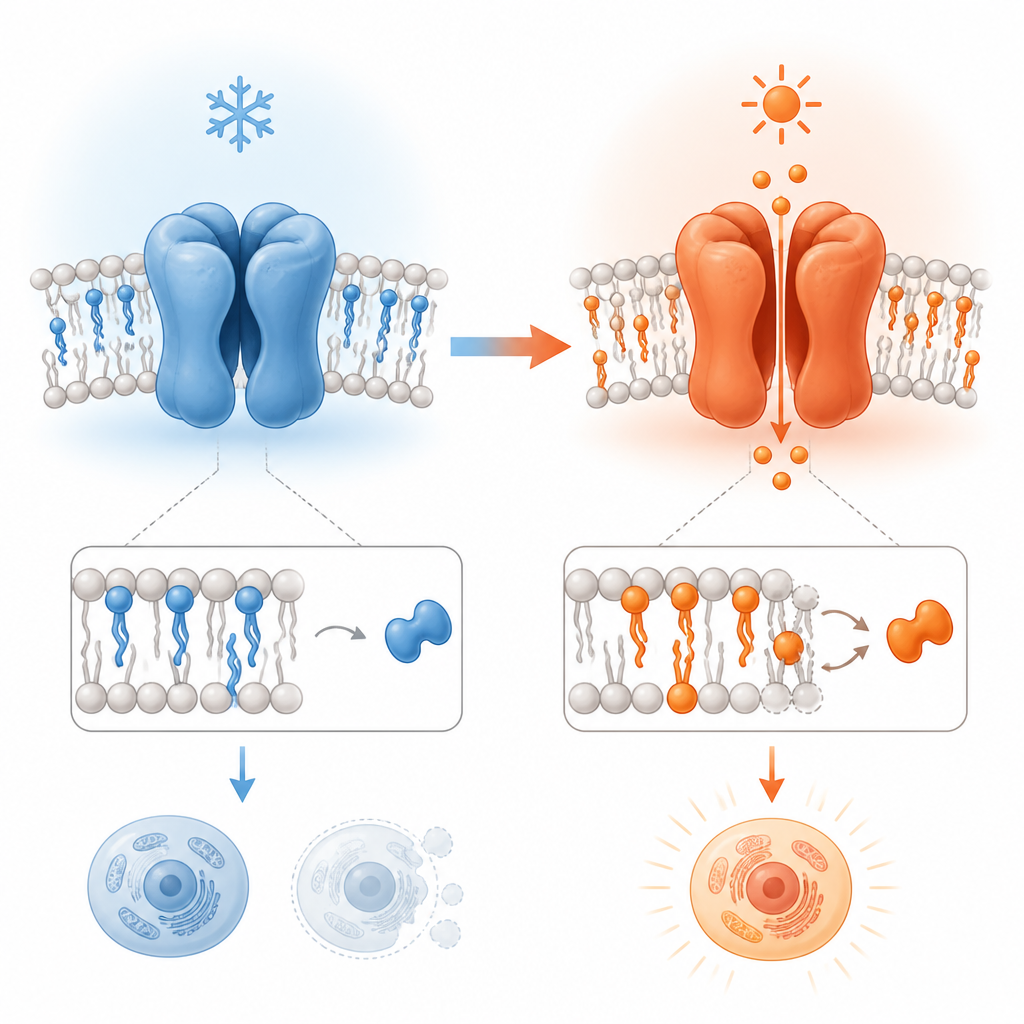
För att undersöka detta jämförde studien högupplösta kryo-elektronmikroskopistrukturer av TRPV3 från möss och människor vid olika temperaturer. Kanalen undersöktes i membranliknande skivor som innehåller naturliga fetter och en speciell växtderived molekyl, tetrahydrokannabivarin (THCV), som kan binda på en plats som normalt upptas av ett lipid. Genom att studera TRPV3 med och utan THCV vid kalla temperaturer, och jämföra dessa strukturer med en värmeaktiverad form, kartlade arbetet de stegvisa strukturella förändringarna som följer öppning, inaktivering och ett ovanligt ”por-dilaterat” tillstånd där kanalen vidgas och ändrar sin sammankoppling.
Gömda värmeregler i ett kallt svar
Den centrala analysen behandlar proteinet som ett nätverk av små icke-kovalenta länkar mellan aminosyror. Dessa länkar bildar slingor, eller ”termoringar”, vars storlek och styrka speglar hur stabil varje del av strukturen är. Den minst stabila länken i den största ringen fungerar som en termisk svag punkt som bestämmer temperaturen då en större omarrangering inträffar. Genom att följa hur dessa svaga punkter och slingor skiftar mellan stängt, öppet och inaktiverat tillstånd kunde författaren uppskatta temperaturtrösklarna för varje övergång. Viktigt är att när ett membranlipid vid vanilloidstället förskjuts av THCV visade den initiala kylinducerade öppningen en strukturell temperatursensitivitet som nära matchade den kända värmesensitiviteten som mätts för TRPV3 vid uppvärmning. Detta speglade beteende stöder idén att en enda förändring i värmekapacitet kan ligga bakom både varm- och kallsinne.
Varför inaktivering ser så annorlunda ut
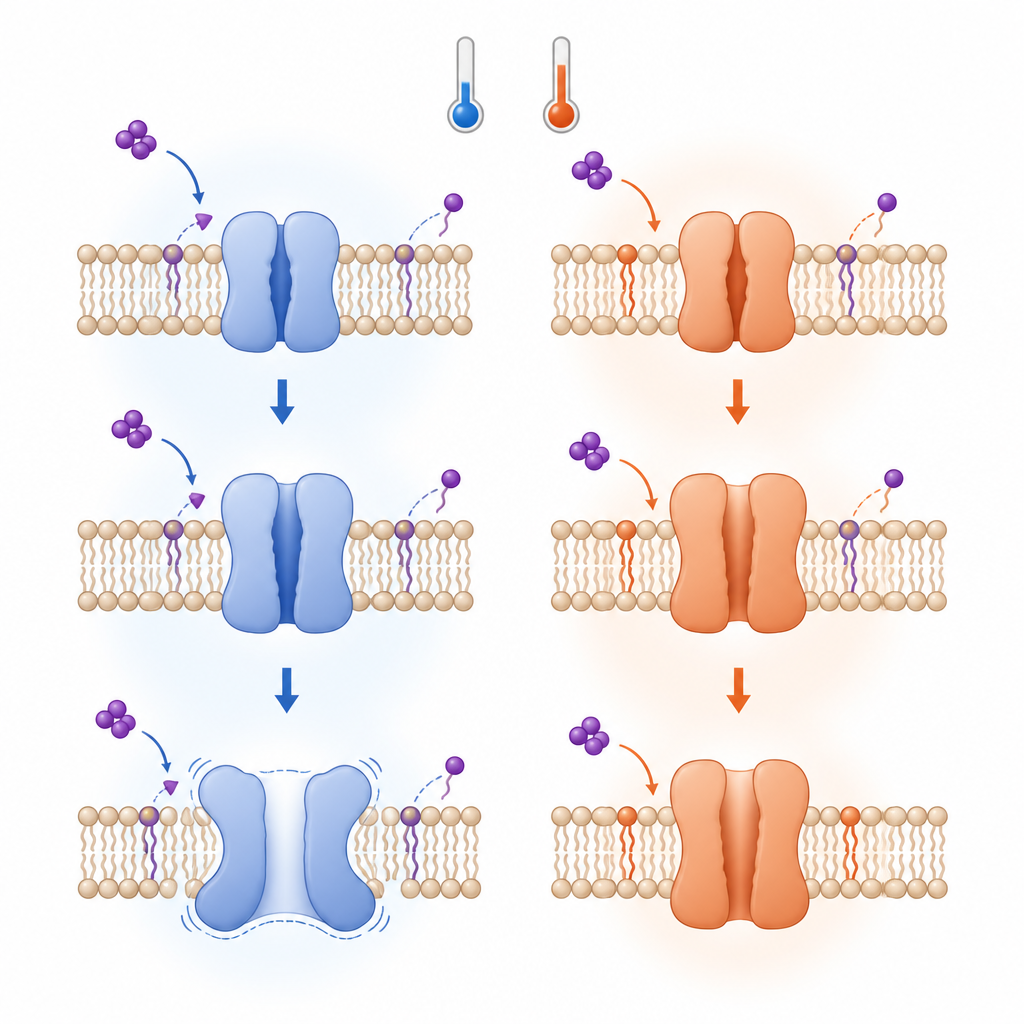
Även om de tidiga stegen i varm- och kaldaktivering följer samma termodynamiska regel, avviker de senare stegen. Vid låga temperaturer, efter att TRPV3 öppnats, stabiliserar ytterligare omarrangemang ett inaktiverat tillstånd och kan till och med driva en övergång från den vanliga fyrdelade uppbyggnaden till en femdelad, por-dilaterad form med en vidgad öppning. Dessa förändringar involverar brott i specifika kontakter som normalt kopplar ihop olika segment av kanalen, vilket gör strukturen mer stabil i vissa avseenden men också mindre förutsägbar. Över ungefär 30 grader Celsius, däremot, tenderar kanalen, efter att lipiden förskjutits och kanalen öppnats, att förbli öppen utan att gå genom samma inaktiveringsväg.
Vad detta betyder för att känna värme och kyla
För en icke-specialist är huvudbudskapet att TRPV3 uppför sig som en termisk apparat vars första reaktion på värme och kyla styrs av samma underliggande energiregel, även om dess senare beteende kan dela sig i olika strukturella banor. Arbetet visar att både uppvärmning och nedkylning kan starta från samma molekylära ”startpunkt” vid ett lipidbindningsställe och producera öppningar med liknande temperaturkänslighet. Därefter kan kanalen, särskilt vid lägre temperaturer, stänga av sig själv eller till och med omforma sig till en annan sammansättning. Detta stöder en generell modell där ett enda termodynamiskt ramverk kan förklara hur ett sensorsprotein bidrar till både varma och kalla upplevelser, samtidigt som det belyser hur ytterligare lager av strukturella förändringar formar vad våra celler slutligen gör med den signalen.
Citering: Wang, G. Temperature-dependent gating pathways in TRPV3. Sci Rep 16, 15030 (2026). https://doi.org/10.1038/s41598-026-44194-0
Nyckelord: TRPV3, temperaturkänslighet, jonkanaler, termodynamik, kryoelektronmikroskopi