Clear Sky Science · nl
Temperatuurafhankelijke poortroutes in TRPV3
Hoe onze huid heet en koud voelt
Onze huid kan in één oogopslag een warme mok van een ijskoud glas onderscheiden, dankzij kleine proteïnepoorten in celmembranen die bij temperatuur openen en sluiten. Eén zo’n poort, TRPV3 genaamd, helpt warmte te detecteren en speelt een rol in huidbiologie. Deze studie stelt een eenvoudig maar fundamenteel vraagstuk: leggen dezelfde basisregels uit hoe dit eiwit zowel warmte als kou waarneemt, zelfs wanneer zijn activiteit later afslaat?
Twee temperatuurroutes naar één sensor
TRPV3 is een vierledig proteïnekanaal dat in het celmembraan zit en geladen deeltjes doorlaat wanneer het opent. Eerder werk suggereerde dat de reactie op warmte beschreven kan worden met een klassieke thermodynamische vergelijking die temperatuurschommelingen koppelt aan veranderingen in energie en warmtecapaciteit. Die vergelijking voorspelt dat, onder de juiste voorwaarden, hetzelfde kanaal ook op afkoeling zou moeten reageren. TRPV3 is echter lastig omdat het, eenmaal geactiveerd, kan inactivëren — het kanaal stopt met geleiden zelfs als de prikkel blijft bestaan. De auteur wilde nagaan of zowel de initiële warme als koude respons nog steeds volgens dezelfde energetische regel verlopen, ondanks die latere veranderingen.
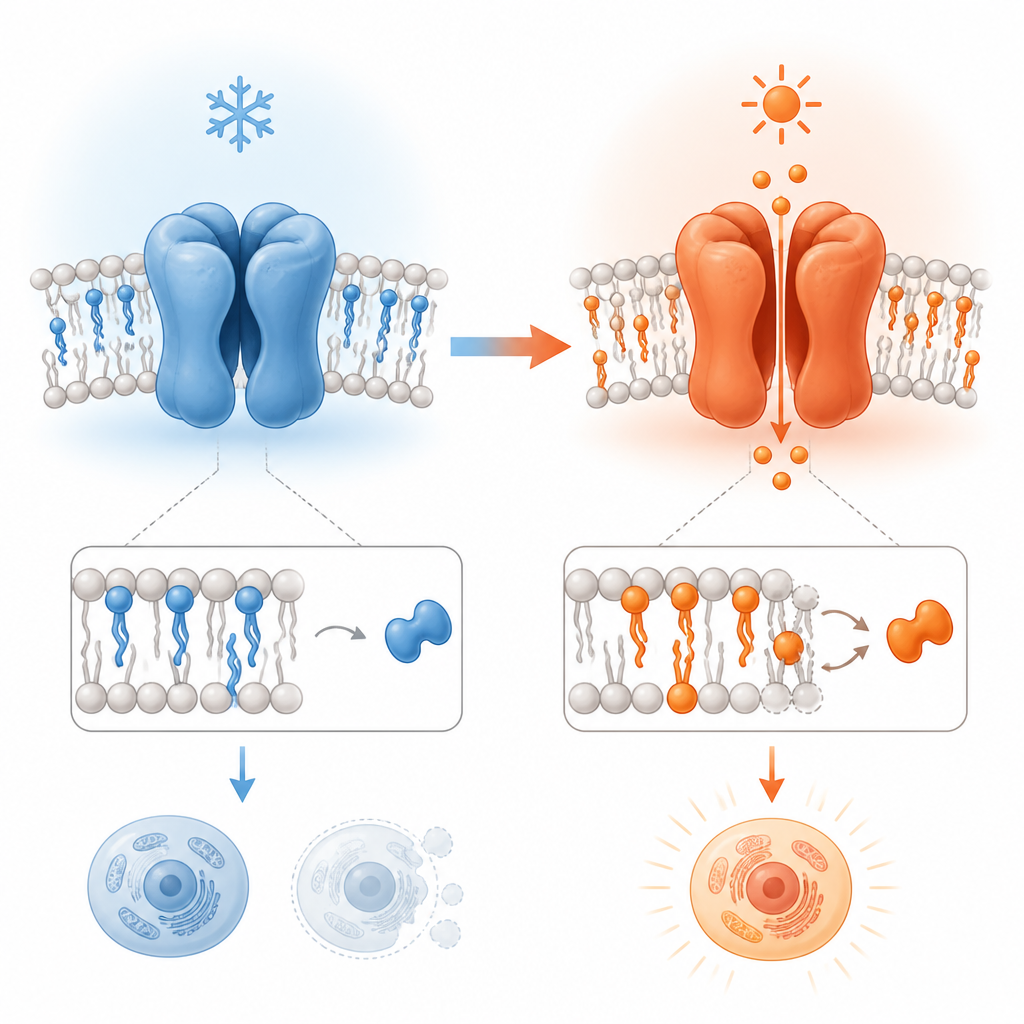
Het kanaal in vormverandering volgen
Om dit te onderzoeken vergeleek de studie hoge-resolutie kryo-elektronenmicroscopie-structuren van TRPV3 uit muis- en menselijke monsters bij verschillende temperaturen. Het kanaal werd bekeken in membraanachtige schijven die natuurlijke vetten en een speciale plantafgeleide molecule, tetrahydrocannabivarin (THCV), bevatten, die kan binden op een plaats die normaal door een lipid wordt bezet. Door TRPV3 met en zonder THCV bij koude temperaturen te bekijken en die structuren te vergelijken met een hitte-geactiveerde vorm, bracht het werk de stapsgewijze structurele veranderingen in kaart die samengaan met openen, inactivatie en een ongewone “porie-verwijdende” toestand waarin het kanaal wijder wordt en zijn samenstelling verandert.
Verborgen hitte-regels in een koude respons
De kernanalyse behandelt het proteïne als een netwerk van kleine niet-covalente verbindingen tussen aminozuren. Deze verbindingen vormen lussen, of “thermoringen”, waarvan grootte en sterkte weergeven hoe stabiel elk deel van de structuur is. De minst stabiele schakel in de grootste ring werkt als een thermisch zwak punt dat de temperatuur bepaalt waarop een grote herschikking plaatsvindt. Door te volgen hoe deze zwakke schakels en lussen verschuiven tussen gesloten, open en geïnactiveerde toestanden, kon de auteur de temperatuurgrenzen voor elke overgang schatten. Belangrijk is dat, wanneer een membraanlipid op de vanilloïdeplaats door THCV werd verdrongen, de aanvankelijke koude-geïnduceerde opening een structurele temperatuursensitiviteit toonde die nauw overeenkwam met de bekende hittegevoeligheid van TRPV3 bij verwarming. Dit weerspiegelende gedrag ondersteunt het idee dat één verandering in warmtecapaciteit zowel warme als koude detectie kan onderbouwen.
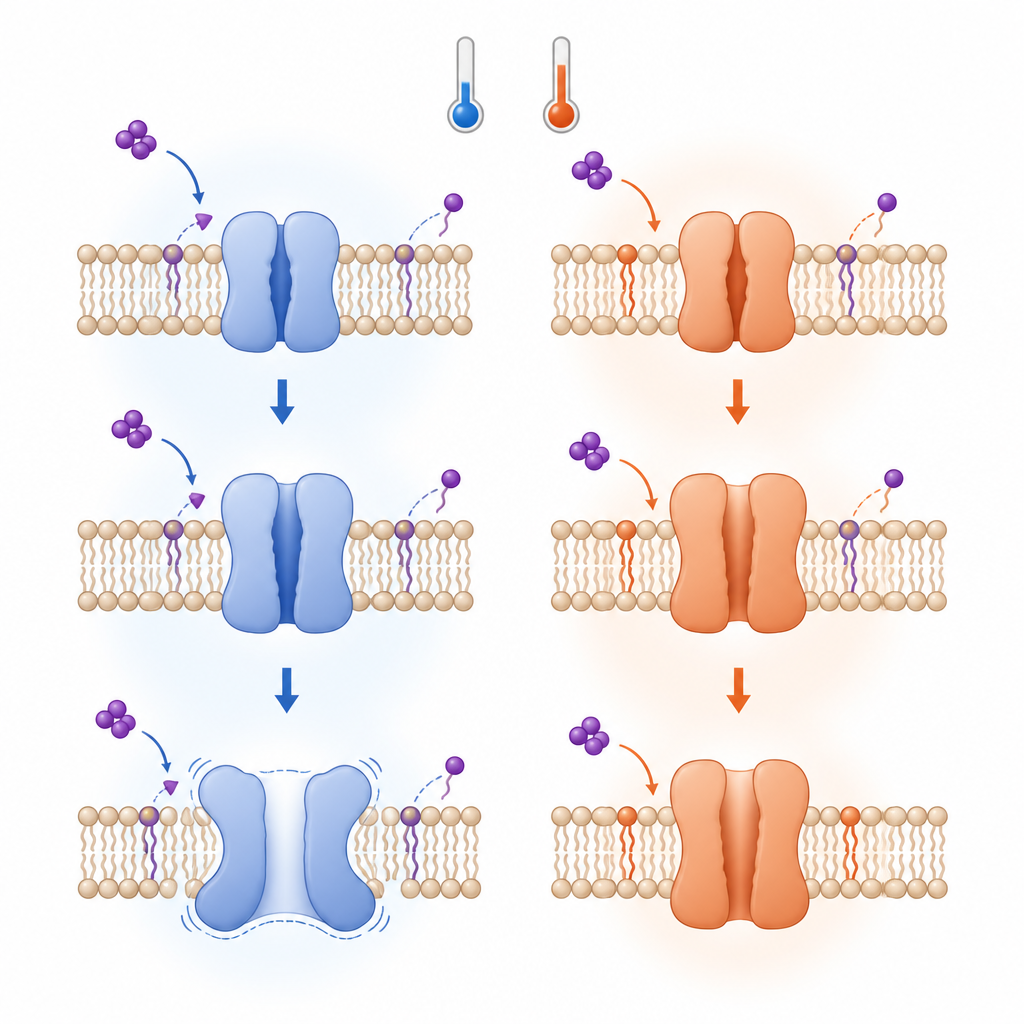
Waarom inactivatie er zo anders uitziet
Hoewel de vroege stappen van warme en koude activatie dezelfde thermodynamische regel volgen, lopen de latere stappen uiteen. Bij lage temperaturen, nadat TRPV3 opent, stabiliseren verdere herschikkingen een geïnactiveerde toestand en kunnen ze zelfs een verschuiving teweegbrengen van de gebruikelijke vierdelige samenstelling naar een vijfdelige, porie-verwijdende vorm met een verruimde opening. Deze veranderingen houden in dat specifieke contacten breken die normaal verschillende segmenten van het kanaal koppelen, waardoor de structuur in sommige opzichten stabieler maar ook minder voorspelbaar wordt. Daarentegen blijft het kanaal boven ongeveer 30 graden Celsius, nadat het lipid is verdrongen en het kanaal opent, geneigd open te blijven zonder door hetzelfde inactivatiepad te gaan.
Wat dit betekent voor het waarnemen van warmte en koude
Voor de niet-specialist is de kernboodschap dat TRPV3 zich gedraagt als een thermisch instrument waarvan de eerste reactie op warm en koud door dezelfde onderliggende energieregel wordt bepaald, ook al kan het latere gedrag in verschillende structurele richtingen afbuigen. Het werk laat zien dat zowel verwarming als afkoeling kunnen beginnen vanaf hetzelfde moleculaire "startpunt" bij een lipidbindende plaats en openingen kunnen veroorzaken met vergelijkbare temperatuursgevoeligheid. Daarna kan het kanaal, vooral bij lagere temperaturen, zichzelf uitschakelen of zelfs herinrichten tot een andere samenstelling. Dit ondersteunt een algemeen model waarin één thermodynamisch kader verklaart hoe één sensorproteïne bijdraagt aan zowel warme als koude gewaarwording, terwijl het ook toont hoe extra lagen van structurele verandering bepalen wat onze cellen uiteindelijk met dat signaal doen.
Bronvermelding: Wang, G. Temperature-dependent gating pathways in TRPV3. Sci Rep 16, 15030 (2026). https://doi.org/10.1038/s41598-026-44194-0
Trefwoorden: TRPV3, temperatuursensing, ionkanalen, thermodynamica, kryo-elektronenmicroscopie