Clear Sky Science · pt
Vias de ativação dependentes de temperatura em TRPV3
Como nossa pele sente calor e frio
Nossa pele consegue distinguir instantaneamente uma caneca morna de um copo gelado graças a minúsculas portas proteicas nas membranas celulares que se abrem e fecham com a temperatura. Uma dessas portas, chamada TRPV3, ajuda a detectar calor e participa da biologia da pele. Este estudo faz uma pergunta simples, porém profunda: as mesmas regras básicas explicam como essa proteína percebe tanto calor quanto frio, mesmo quando sua atividade depois se desliga?
Dois caminhos térmicos para um mesmo sensor
O TRPV3 é um canal proteico em quatro partes que fica na membrana celular e permite que íons carregados fluam quando se abre. Trabalhos anteriores sugeriram que sua resposta ao calor pode ser descrita por uma equação termodinâmica clássica que relaciona variações de temperatura a mudanças na energia e na capacidade térmica. Essa equação prevê que, sob condições adequadas, o mesmo canal também deveria responder ao resfriamento. Contudo, o TRPV3 é complicado porque, uma vez ativado, pode se inativar — ou seja, o canal para de conduzir mesmo se o estímulo permanecer. O autor procurou verificar se tanto as respostas iniciais ao calor quanto ao frio seguem a mesma regra energética, apesar dessas mudanças posteriores.
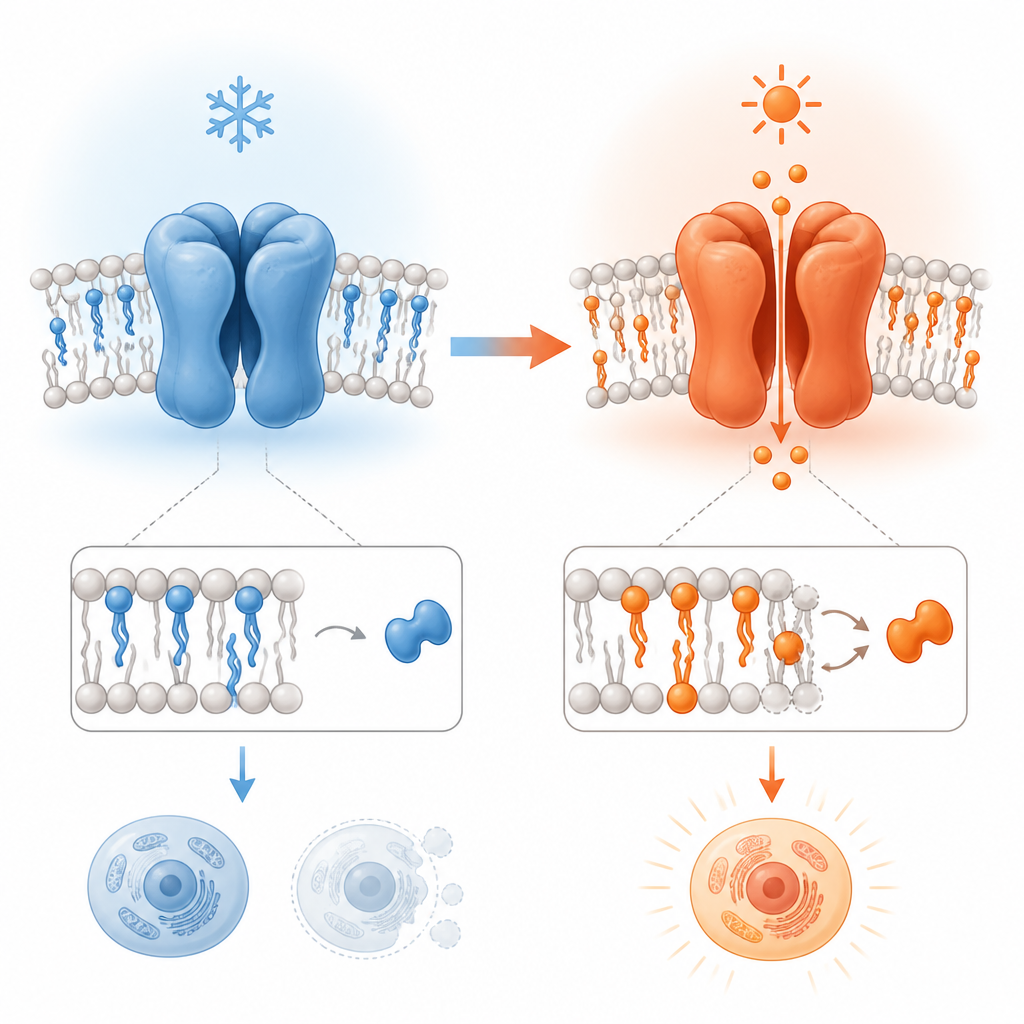
Observando o canal mudar de forma
Para investigar isso, o estudo comparou estruturas de alta resolução de TRPV3 de camundongo e humano obtidas por crio-microscopia eletrônica em diferentes temperaturas. O canal foi examinado em discos semelhantes à membrana que incluem gorduras naturais e uma molécula derivada de planta especial, a tetrahidrocanabivarina (THCV), que pode ligar-se em um sítio normalmente ocupado por um lipídio. Ao analisar o TRPV3 com e sem THCV em temperaturas frias e comparar essas estruturas com uma forma ativada pelo calor, o trabalho mapeou as mudanças estruturais passo a passo que acompanham a abertura, a inativação e um estado incomum de “dilatação do poro” no qual o canal se alarga e muda seu arranjo.
Regras térmicas ocultas em uma resposta ao frio
A análise central trata a proteína como uma rede de pequenas ligações não covalentes entre aminoácidos. Essas ligações formam anéis, ou “termoringues”, cujo tamanho e força refletem o quão estável cada parte da estrutura é. A ligação menos estável no maior anel atua como um ponto térmico fraco que define a temperatura na qual uma reorganização importante ocorre. Ao acompanhar como esses pontos fracos e anéis mudam entre estados fechado, aberto e inativado, o autor pôde estimar os limiares de temperatura para cada transição. Importante: quando um lipídio de membrana no sítio vaniloide foi deslocado pela THCV, a abertura inicial induzida pelo frio mostrou uma sensibilidade estrutural à temperatura que coincidia estreitamente com a sensibilidade ao calor conhecida para o TRPV3 sob aquecimento. Esse comportamento espelhado apoia a ideia de que uma única mudança na capacidade térmica pode fundamentar tanto a detecção de calor quanto de frio.
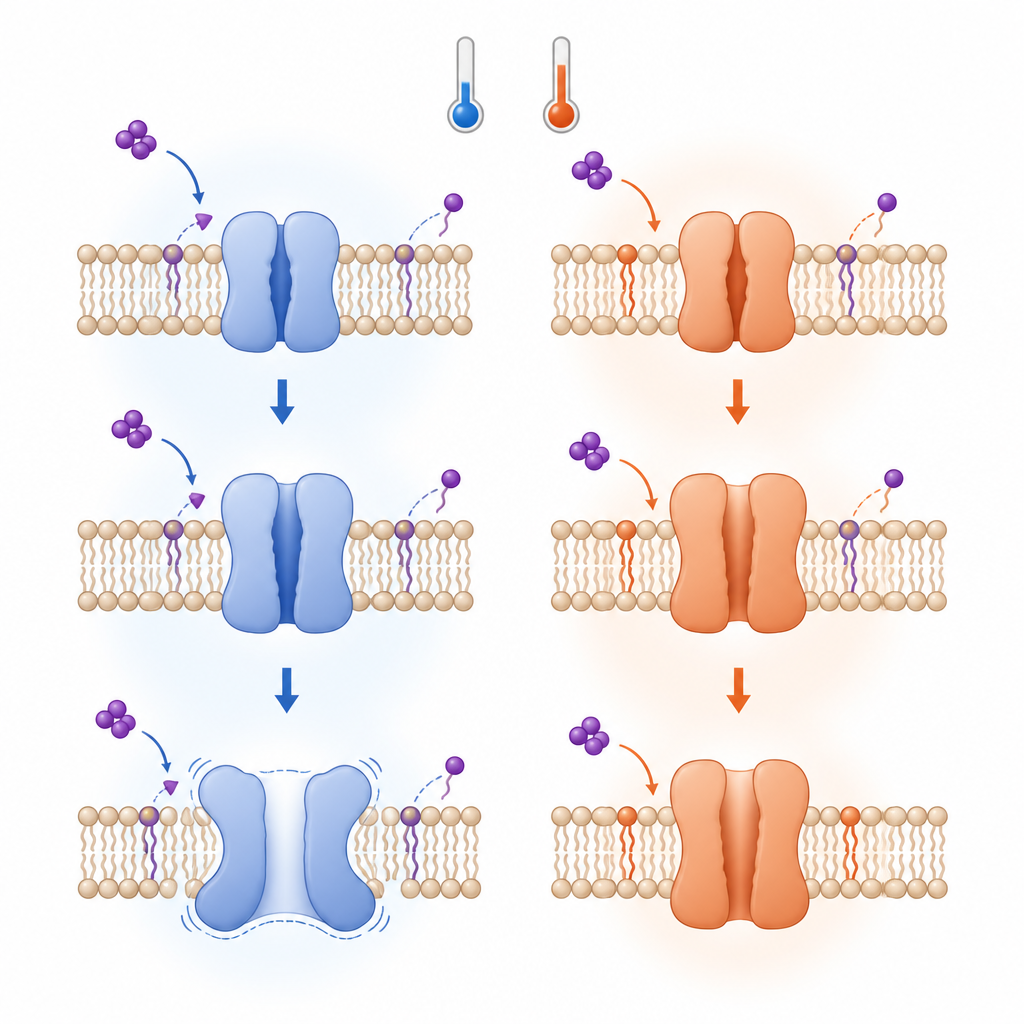
Por que a inativação parece tão diferente
Embora os primeiros passos da ativação por calor e por frio obedeçam à mesma regra termodinâmica, os passos posteriores divergem. Em baixas temperaturas, após o TRPV3 se abrir, rearranjos adicionais estabilizam um estado inativado e podem até promover uma mudança do arranjo usual em quatro partes para uma forma em cinco partes, com poro dilatado e abertura ampliada. Essas mudanças envolvem a ruptura de contatos específicos que normalmente acoplam diferentes segmentos do canal, tornando a estrutura mais estável em certos aspectos, mas também menos previsível. Acima de cerca de 30 graus Celsius, por outro lado, uma vez que o lipídio foi deslocado e o canal se abre, ele tende a permanecer aberto sem passar pelo mesmo caminho de inativação.
O que isso significa para a detecção de calor e frio
Para um público não especializado, a mensagem central é que o TRPV3 se comporta como um mecanismo térmico cuja primeira reação ao calor e ao frio é regida pela mesma regra energética subjacente, embora seu comportamento posterior possa seguir rotas estruturais diferentes. O estudo mostra que tanto o aquecimento quanto o resfriamento podem partir do mesmo “gatilho” molecular em um sítio de ligação a lipídio e produzir aberturas com sensibilidade à temperatura semelhante. Depois disso, especialmente em temperaturas mais baixas, o canal pode se desligar sozinho ou mesmo remodelar-se em um arranjo diferente. Isso sustenta um modelo geral no qual uma única estrutura termodinâmica pode explicar como uma proteína sensora contribui para a sensação de calor e frio, ao mesmo tempo em que destaca como camadas adicionais de mudanças estruturais moldam o que nossas células fazem, em última instância, com esse sinal.
Citação: Wang, G. Temperature-dependent gating pathways in TRPV3. Sci Rep 16, 15030 (2026). https://doi.org/10.1038/s41598-026-44194-0
Palavras-chave: TRPV3, detecção de temperatura, canais iônicos, termodinâmica, crio-microscopia eletrônica