Clear Sky Science · es
Vías de apertura dependientes de la temperatura en TRPV3
Cómo nuestra piel percibe calor y frío
Nuestra piel distingue al instante una taza tibia de un vaso helado gracias a diminutas compuertas proteicas en las membranas celulares que se abren y cierran con la temperatura. Una de esas compuertas, llamada TRPV3, ayuda a detectar el calor y participa en la biología cutánea. Este estudio plantea una pregunta sencilla pero profunda: ¿explican las mismas reglas básicas cómo esta proteína detecta tanto el calor como el frío, incluso cuando su actividad después se apaga por inactivación?
Dos caminos térmicos hacia un solo sensor
TRPV3 es un canal proteico formado por cuatro subunidades que se sitúa en la membrana celular y permite el paso de iones cuando se abre. Estudios previos sugirieron que su respuesta al calor puede describirse con una ecuación termodinámica clásica que vincula cambios de temperatura con variaciones en la energía y la capacidad calorífica. Esa ecuación predice que, en las condiciones adecuadas, el mismo canal también debería responder al enfriamiento. Sin embargo, TRPV3 es complejo porque una vez activado puede inactivarse, es decir, dejar de conducir aunque el estímulo persista. El autor se propuso comprobar si tanto las respuestas iniciales al calor como al frío siguen la misma regla energética, pese a esos cambios posteriores.
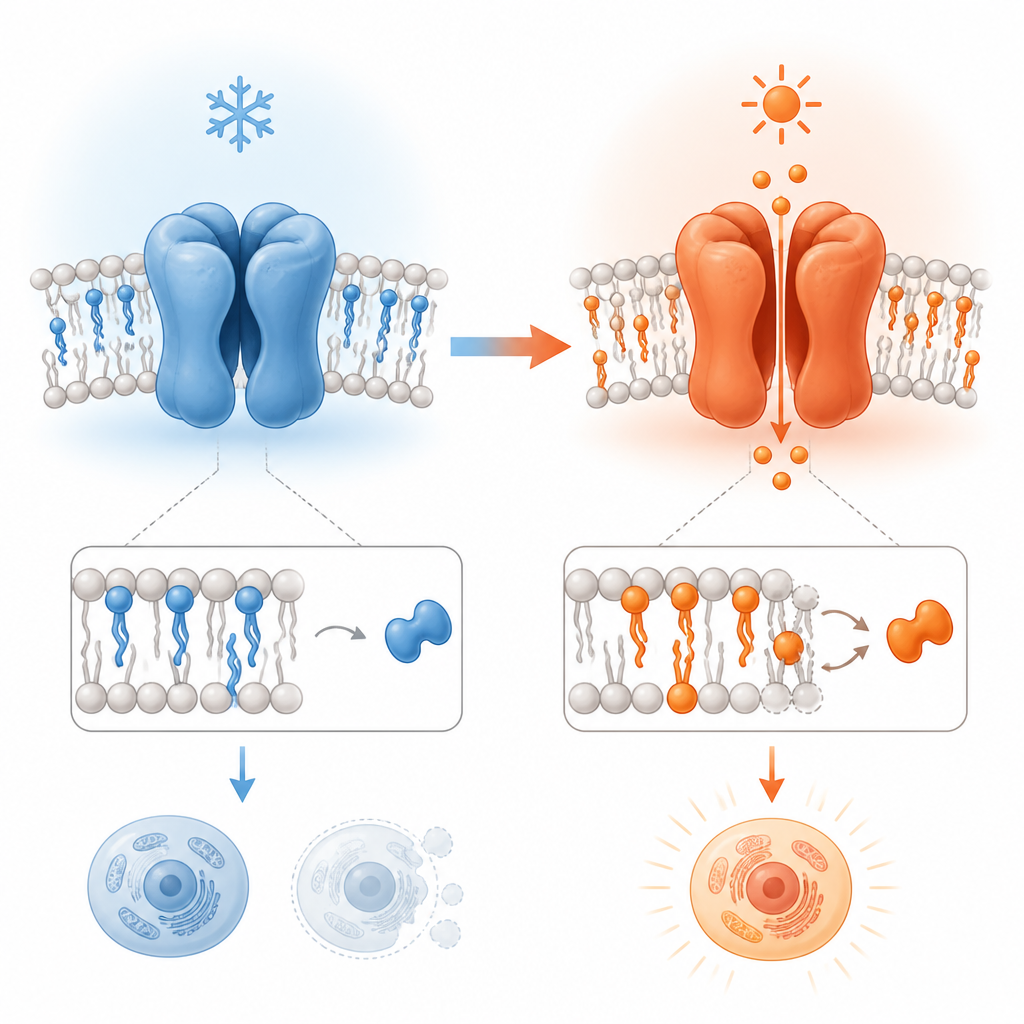
Observando cómo cambia la forma del canal
Para investigar esto, el estudio comparó estructuras de alta resolución obtenidas por crio-microscopía electrónica de TRPV3 de muestras de ratón y humano a diferentes temperaturas. El canal se examinó en discos semejantes a membranas que incluyen grasas naturales y una molécula de origen vegetal especial, tetrahidrocannabivarina (THCV), que puede unirse en un sitio normalmente ocupado por un lípido. Al observar TRPV3 con y sin THCV a temperaturas frías, y comparar esas estructuras con una forma activada por calor, el trabajo trazó los cambios estructurales por etapas que acompañan la apertura, la inactivación y un inusual estado de “poro dilatado” en el que el canal se ensancha y cambia su ensamblaje.
Reglas térmicas ocultas en una respuesta al frío
El análisis clave trata la proteína como una red de pequeños enlaces no covalentes entre aminoácidos. Esos enlaces forman lazos, o “anillos térmicos”, cuyo tamaño y fuerza reflejan cuán estable es cada parte de la estructura. El enlace menos estable en el anillo más grande actúa como un punto térmico débil que determina la temperatura a la que ocurre una reorganización mayor. Al seguir cómo cambian esos puntos débiles y lazos entre los estados cerrado, abierto e inactivado, el autor pudo estimar los umbrales de temperatura para cada transición. Es importante que, cuando un lípido de la membrana en el sitio vanilloide fue desplazado por THCV, la apertura inicial inducida por el frío mostró una sensibilidad estructural a la temperatura que coincidía estrechamente con la sensibilidad al calor conocida para TRPV3 durante el calentamiento. Este comportamiento en espejo respalda la idea de que un único cambio en la capacidad calorífica puede sustentar tanto la detección del calor como del frío.
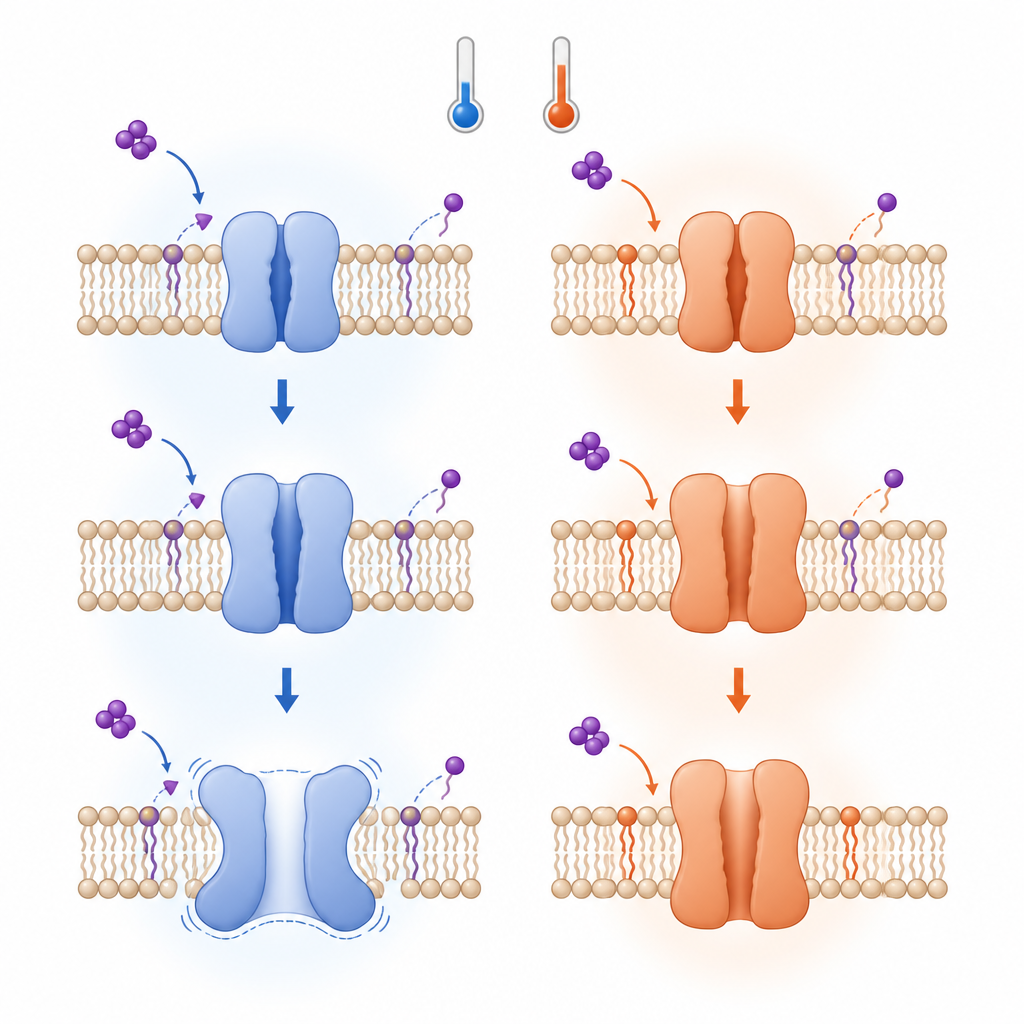
Por qué la inactivación parece tan diferente
Aunque los primeros pasos de la activación por calor y por frío obedecen la misma regla termodinámica, los pasos posteriores divergen. A bajas temperaturas, tras la apertura de TRPV3, reordenamientos adicionales estabilizan un estado inactivado e incluso pueden impulsar un cambio desde el ensamblaje habitual de cuatro subunidades a una forma de cinco subunidades con poro dilatado y una apertura más ancha. Estos cambios implican la ruptura de contactos específicos que normalmente acoplan distintos segmentos del canal, haciendo la estructura más estable en ciertos aspectos pero también menos predecible. Por el contrario, por encima de unos 30 grados Celsius, una vez que el lípido ha sido desplazado y el canal se abre, tiende a permanecer abierto sin seguir la misma vía de inactivación.
Qué significa esto para la detección de calor y frío
Para un lector no especialista, el mensaje central es que TRPV3 se comporta como un dispositivo térmico cuya primera reacción al calor y al frío está gobernada por la misma regla energética subyacente, aunque su comportamiento posterior pueda ramificarse en rutas estructurales distintas. El trabajo muestra que tanto el calentamiento como el enfriamiento pueden partir del mismo “interruptor” molecular en un sitio de unión lipídico y producir aperturas con sensibilidad similar a la temperatura. A partir de ahí, especialmente a temperaturas más bajas, el canal puede cerrarse por inactivación o incluso remodelarse hacia un ensamblaje diferente. Esto respalda un modelo general en el que un único marco termodinámico puede explicar cómo una proteína sensora contribuye tanto a la sensación de calor como de frío, a la vez que destaca cómo capas adicionales de cambio estructural determinan lo que nuestras células hacen finalmente con esa señal.
Cita: Wang, G. Temperature-dependent gating pathways in TRPV3. Sci Rep 16, 15030 (2026). https://doi.org/10.1038/s41598-026-44194-0
Palabras clave: TRPV3, detección de temperatura, canales iónicos, termodinámica, crioelectrónica por microscopía