Clear Sky Science · ja
TRPV3における温度依存的ゲーティング経路
私たちの皮膚が暑さと冷たさを感知する仕組み
私たちの皮膚は、温かいマグカップと氷の入ったグラスを瞬時に見分けられます。これは、温度に応じて開閉する細胞膜上の小さなタンパク質ゲートのおかげです。その一つであるTRPV3は温かさの検出に関わり、皮膚の生物学的機能にも寄与します。本研究は単純だが本質的な問いを立てます。活動が後に自らオフになる場合でも、このタンパク質が熱と冷気の両方を感知するのを同じ基本的ルールで説明できるのか、という点です。
一つのセンサーへの二つの温度経路
TRPV3は膜に埋まる4つのサブユニットから成るチャネルで、開くと荷電したイオンを通します。以前の研究は、熱に対する応答が温度変化をエネルギーや比熱の変化と結びつける古典的な熱力学式で記述できることを示唆していました。その式は適切な条件下で同じチャネルが冷却にも応答するはずだと予測します。しかしTRPV3は扱いが難しく、一度活性化すると刺激が続いても導通をやめる不活性化が起きます。著者は、こうした後続の変化があっても、初期の熱および冷の応答が同じエネルギー則に従うかを確かめようとしました。
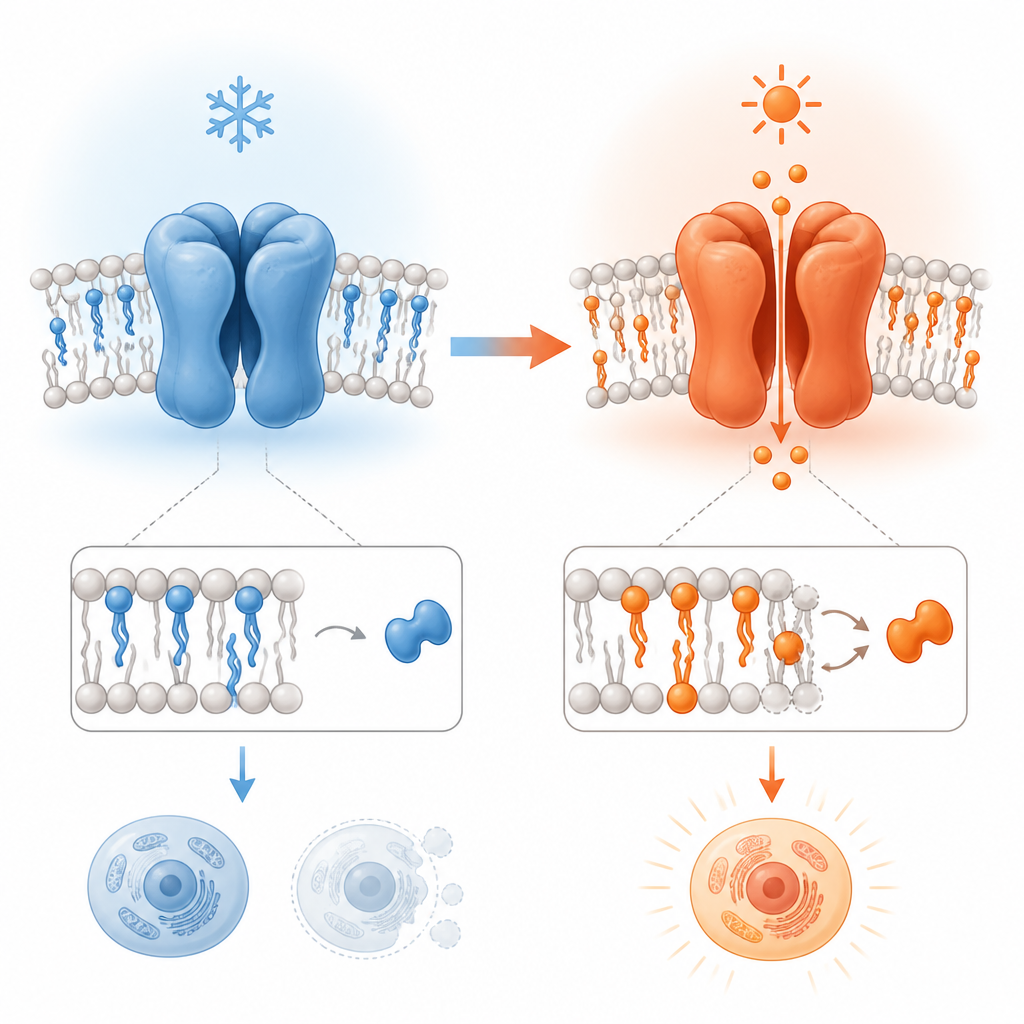
チャネルの形が変わるのを観察する
これを調べるために、本研究ではマウスとヒト由来TRPV3の高解像度クライオ電子顕微鏡構造を異なる温度で比較しました。チャネルは天然脂質を含む膜様ディスク内で、通常脂質が占める部位に結合できる植物由来の分子テトラヒドロカンナビバリン(THCV)を含めて調べられました。低温でTHCVの有無を比較し、これらの構造を熱活性化形と対比することで、開口、不活性化、そしてチャネルが拡張してアセンブリを変えるという非凡な「孔拡張」状態に伴う段階的な構造変化をマッピングしました。
冷応答に隠れた熱のルール
主要な解析は、タンパク質をアミノ酸間の小さな非共有結合的結びつきのネットワークとして扱います。これらの結びつきはループ、つまり「サーモリング」を形成し、その大きさと強さは構造の各部分の安定性を反映します。最大のリングにおける最も不安定な結びつきが、主要な再配置が生じる温度を決める熱的な弱点として働きます。閉鎖、開口、不活性化状態の間でこれらの弱点とループがどのように移動するかを追跡することで、各遷移の温度閾値を推定できます。重要な点は、バニロイド部位の膜脂質がTHCVによって置換されたとき、初期の冷誘導開口が、温度上昇時にTRPV3で測定された既知の熱感受性と非常に近い構造的温度依存性を示したことです。この鏡像的な挙動は、熱容量の単一の変化が熱と冷の両方の感知の基盤になり得ることを支持します。
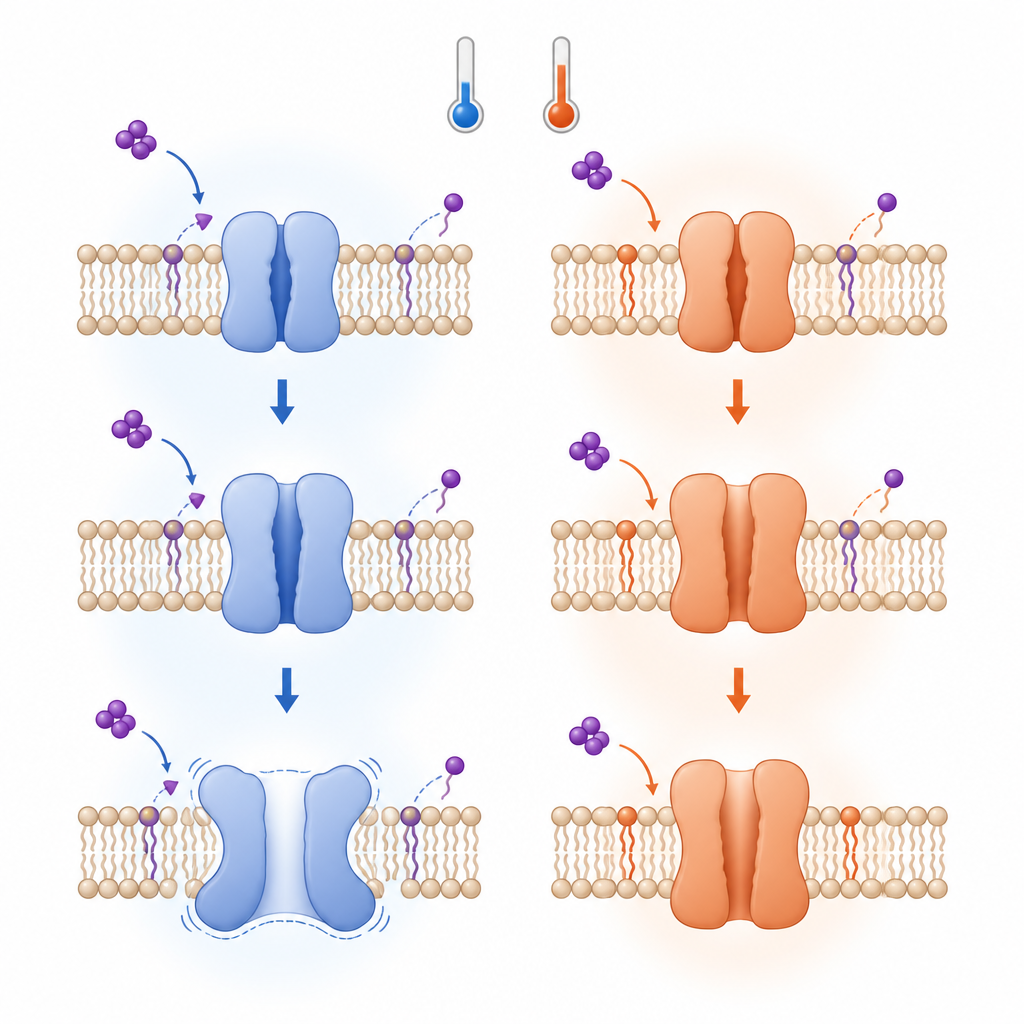
なぜ不活性化が異なって見えるのか
初期の熱および冷の活性化の段階は同じ熱力学ルールに従いますが、後の段階は分岐します。低温では、TRPV3が一度開くとさらに再配置が進み、不活性化状態を安定化させ、通常の4量体から5量体の孔拡張形へと変化することさえあります。これらの変化は、チャネルの異なるセグメントを結びつける特定の接触の破壊を伴い、ある点では構造をより安定化させる一方で予測を難しくします。対照的に約30度C以上では、脂質が置換されチャネルが開くと、そのまま開いた状態を維持し、同じ不活性化経路を経ることは少ない傾向があります。
熱と冷の感知にとっての意義
専門外の読者への要点は、TRPV3は熱と冷の最初の反応が同じ基礎的エネルギールールで支配される“熱的ギア”のように振る舞うが、その後の挙動は異なる構造経路に分かれることがある、ということです。この研究は、温めと冷却の両方が脂質結合部位にある単一の分子的“起動装置”から始まり、温度に対して似た感度を持つ開口を生じさせ得ることを示します。その後、特に低温ではチャネルが自ら停止したり、別のアセンブリに再構築されたりする可能性があります。これは一つの熱力学的枠組みが一つのセンサータンパク質による熱・冷感受性の双方を説明しうることを支持すると同時に、追加の構造変化が細胞が最終的にその信号で何をするかを形成することを明らかにします。
引用: Wang, G. Temperature-dependent gating pathways in TRPV3. Sci Rep 16, 15030 (2026). https://doi.org/10.1038/s41598-026-44194-0
キーワード: TRPV3, 温度感知, イオンチャネル, 熱力学, クライオ電子顕微鏡