Clear Sky Science · sv
Xq28-duplication, inte F8-inversion: integrerad genetisk omanalys omdefinierar prenatal bärarediagnostik
När ett rutinmässigt fostertest ger ett tvetydigt budskap
Blivande föräldrar vänder sig i allt större utsträckning till genetisk bärarscreening för att upptäcka allvarliga ärftliga sjukdomar innan barnet är fött. Men vad händer när ett betrott test ger ett oroande resultat som senare visar sig vara missvisande? Denna studie följer en gravid kvinna vars screening antydde att hon kunde föra vidare en allvarlig blödningsrubbning, för att mer avancerade tester senare avslöjade en mycket annorlunda — och mindre entydig — förändring i hennes DNA. Fallet belyser både kraften och fallgroparna i modern genetik och varför konfirmerande tester är viktiga för verkliga familjer som måste fatta svåra beslut.
En blödningsrubbning som börjar i generna
Berättelsen kretsar kring hemofili A, en välkänd blödningsrubbning som främst drabbar pojkar. Den orsakas av skadliga förändringar i en gen på X-kromosomen som kallas F8, som behövs för att tillverka ett koagulationsprotein. Många av de svåraste fallen beror på en särskild sorts omarrangemang i denna gen, känd som inversion i en lång DNA-sekvens kallad intron 22. Eftersom denna inversion är relativt vanlig och tekniskt sett lätt att testa för, ingår ofta ett specifikt test för just detta omarrangemang i bärarscreeningpaneler för personer som planerar graviditet eller redan är gravida.
När det första testet pekar åt fel håll
I det här fallet gjorde en frisk 27-årig kvinna en utökad bärarscreening tidigt i graviditeten. Ett specialiserat långdistans-PCR-test antydde att hon bar den klassiska F8-inversionen och markerade henne som en potentiell bärare av hemofili A. Förståeligt nog oroades hon för sitt ofödda barn och genomgick prenatal diagnostik. Inledande tester på fostret verkade visa samma inversion. Vid första anblicken såg det ut som en enkel historia: mor och dotter bar båda en känd, högriskvariant för en allvarlig blödningssjukdom.
En dold DNA-duplicering kommer i dagen
När man tittade närmare framkom en mer komplicerad berättelse. Ett genomomfattande test som söker efter vinster och förluster av DNA-segment — ett SNP-array — bekräftade inte bara en inversion. I stället avslöjade det att både modern och fostret hade en extra kopia av en halvmegabas-region i den yttersta delen av X-kromosomen, ett område känt som distala Xq28 som inkluderar stora delar av F8-genen tillsammans med flera hjärnrelaterade gener. Ytterligare tekniker som kan läsa långa DNA-sträckor i ett stycke — optisk genomsökning och långläsningssekvensering — visade att denna extra kopia uppstod från en duplikation mellan två nästan identiska DNA-block som flankerar regionen. Viktigt är att F8-genen i sig inte var inverterad, utan delvis duplicerad på ett sätt som lämnade dess funktion intakt.
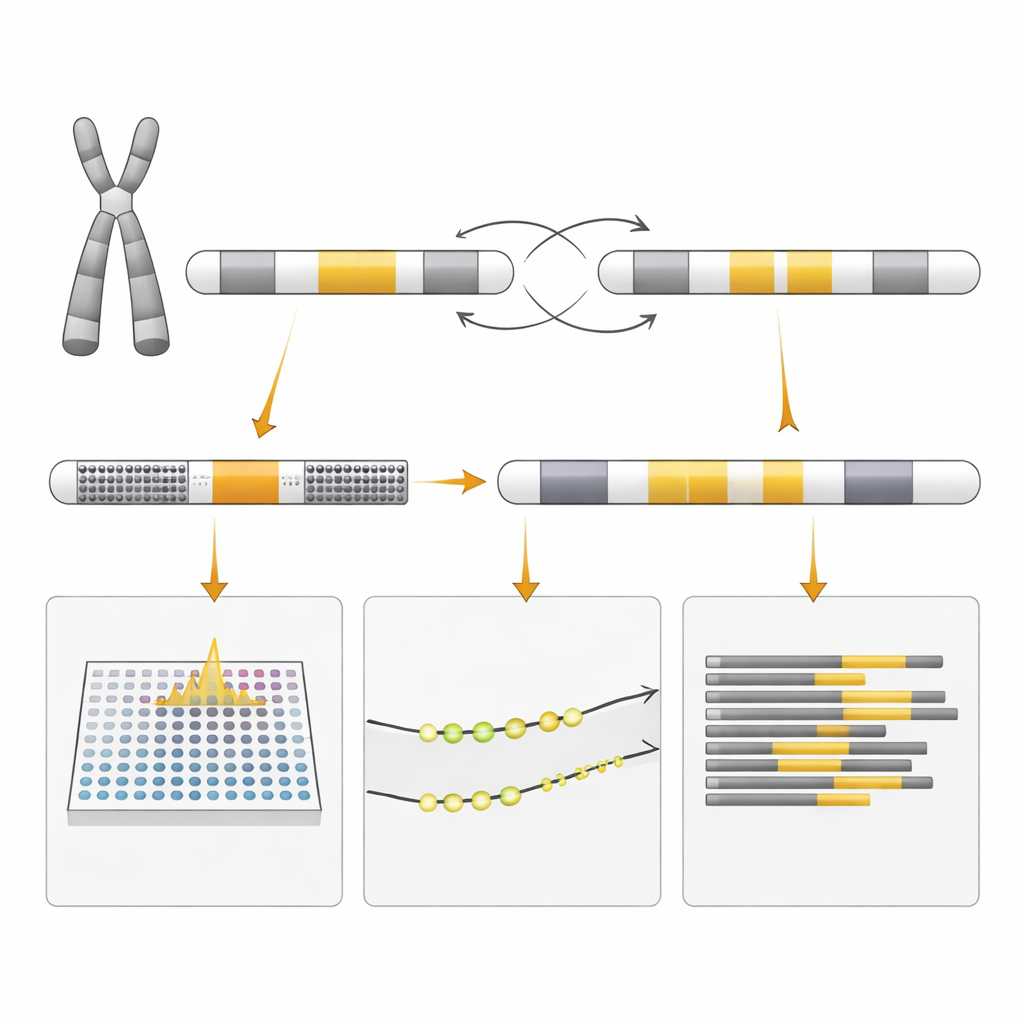
Samma signal, annan betydelse
Varför verkade det standardiserade inversionstestet positivt när det inte fanns någon inversion? Svaret ligger i hur testet är utformat. Det använder par av DNA-primers som normalt ger ett mönster av fragment hos personer utan omarrangemang och ett annat mönster när den klassiska inversionen är närvarande. Duplikationen som skapades genom felparning mellan upprepade DNA-segment genererade en blandning av fragment som imiterade inversionsmönstret, även om den underliggande strukturen var annorlunda. Endast de mer detaljerade metoderna kunde reda ut huruvida DNA:t faktiskt var vänt, kopierat eller både och. Forskarna undersökte också hur de två X-kromosomerna var aktiverade eller inaktiverade hos modern och fostret, en process kallad X-kromosominaktivering, för att förstå varför modern var frisk och för att bedöma möjliga effekter på barnet, även om detta inte kunde förutsäga utgången med säkerhet.
Vad detta betyder för familjer och kliniker
Huvudlärdomen är att även långvariga, betrodda tester kan vilseleda när de används brett i friska populationer snarare än hos patienter som redan är kända för att ha sjukdomen. I detta fall flaggade det initiala testet korrekt för ett ovanligt omarrangemang i F8-området men kunde inte avgöra om det var den klassiska inversionen som orsakar hemofili A eller en närliggande duplikation kopplad till ett annat syndrom som ofta ger milda eller inga effekter hos kvinnor. Genom att lägga enkla förstahands-screeningar över varandra med nyare tekniker som läser längre DNA-segment visade teamet hur man kan skilja dessa möjligheter åt. De föreslår ett stegvis förfarande: använd det snabba, billigare inversionstestet som första urval, men följ upp alla positiva resultat med optisk genomsökning eller långläsningssekvensering för att klargöra om förändringen verkligen är farlig. För familjer innebär detta att ett oroande screeningsresultat bör ses som början på en mer noggrann utredning — inte som sista ordet.
Citering: Yang, X., Maimaiti, S., Qi, Q. et al. Xq28 duplication not F8 inversion: integrated genetic reanalysis redefines prenatal carrier diagnosis. Sci Rep 16, 13390 (2026). https://doi.org/10.1038/s41598-026-43654-x
Nyckelord: hemofili A, prenatal genetisk testning, duplikation på X-kromosomen, bärarscreening, genomets strukturella varianter