Clear Sky Science · pt
Duplicação em Xq28, não inversão em F8: reanálise genética integrada redefine diagnóstico pré-natal de portadoras
Quando um teste de rotina para bebês envia uma mensagem ambígua
Futuros pais recorrem cada vez mais à triagem genética de portadoras para detectar doenças hereditárias graves antes do nascimento. Mas o que acontece quando um teste confiável devolve um resultado alarmante que depois se revela enganoso? Este estudo acompanha uma gestante cuja triagem sugeriu que ela poderia transmitir um distúrbio hemorrágico grave, mas testes mais avançados revelaram uma alteração no DNA muito diferente — e bem menos direta. O caso ilustra tanto o poder quanto as armadilhas da genética moderna e por que testes confirmatórios importam para famílias reais que precisam tomar decisões difíceis.
Um distúrbio hemorrágico que começa nos genes
A história gira em torno da hemofilia A, um distúrbio hemorrágico bem conhecido que afeta principalmente meninos. É causado por alterações deletérias em um gene no cromossomo X chamado F8, necessário para produzir uma proteína de coagulação. Muitos dos casos mais graves decorrem de um tipo particular de rearranjo nesse gene, conhecido como inversão no longo trecho de DNA chamado íntron 22. Como essa inversão é comum e relativamente fácil de detectar, muitos painéis de triagem de portadoras para pessoas que planejam uma gravidez ou que já estão grávidas incluem um ensaio específico que procura apenas esse rearranjo.
Quando o primeiro teste aponta na direção errada
Neste caso, uma mulher saudável de 27 anos realizou um painel ampliado de triagem de portadoras no início da gravidez. Um teste PCR de longa distância especializado sugeriu que ela carregava a clássica inversão em F8, identificando-a como possível portadora de hemofilia A. Com razão preocupada com o feto, ela fez testes pré-natais. Os exames iniciais no feto pareceram mostrar a mesma inversão. À primeira vista, parecia uma história simples: mãe e filha carregavam um variante conhecida de alto risco para uma doença hemorrágica grave.
Um repetido de DNA oculto vem à tona
Uma inspeção mais detalhada contou uma história mais complicada. Um teste genômico de varredura que procura ganhos e perdas de segmentos de DNA — chamado microarranjo de SNP — não confirmou simplesmente uma inversão. Em vez disso, revelou que tanto a mãe quanto o feto tinham uma cópia extra de uma região de meio megabase na extremidade distal do cromossomo X, uma área conhecida como Xq28 distal que inclui grande parte do gene F8 junto com vários genes relacionados ao cérebro. Tecnologias adicionais capazes de visualizar longos trechos de DNA de uma só vez — mapeamento óptico do genoma e sequenciamento de leitura longa — mostraram que essa cópia extra veio de uma duplicação entre dois blocos de DNA quase idênticos que flankam a região. De forma crucial, o próprio gene F8 não estava invertido, apenas parcialmente duplicado de maneira que preservou sua função.
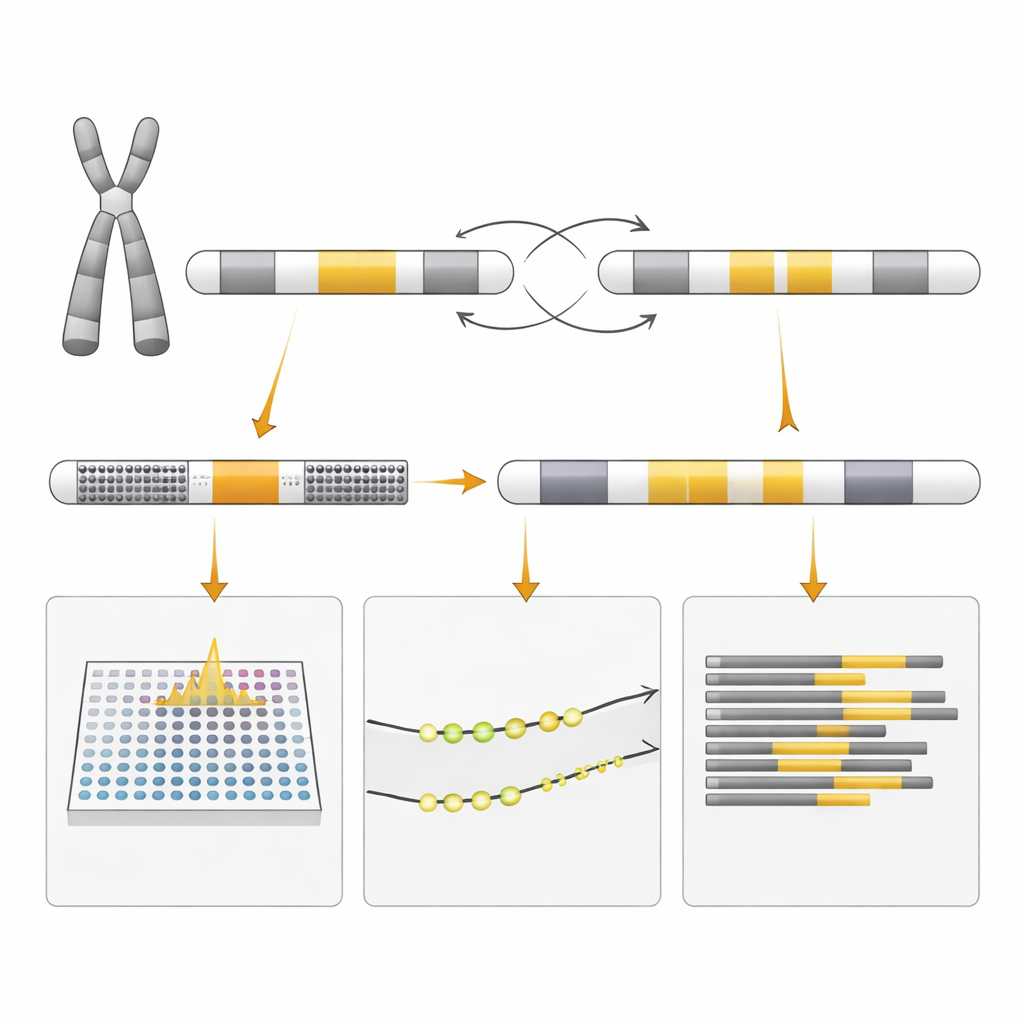
Mesmo sinal, significado diferente
Por que o teste padrão de inversão pareceu positivo se não havia inversão? A resposta está no desenho do ensaio. Ele usa pares de primers de DNA que normalmente produzem um padrão de fragmentos em pessoas sem rearranjos e um padrão diferente quando a inversão clássica está presente. A duplicação criada pelo pareamento incorreto entre segmentos repetidos de DNA gerou uma mistura de fragmentos que imitou o padrão de inversão, mesmo que a estrutura subjacente fosse distinta. Somente métodos mais detalhados puderam desvendar se o DNA estava realmente invertido, copiado ou ambos. Os pesquisadores também examinaram como os dois cromossomos X eram ativados ou desativados na mãe e no feto, um processo chamado inativação do cromossomo X, para entender por que a mãe estava saudável e para avaliar possíveis efeitos na criança, embora isso não pudesse prever o desfecho com certeza.
O que isso significa para famílias e clínicas
A lição principal é que mesmo testes consolidados e confiáveis podem enganar quando aplicados amplamente em populações saudáveis, em vez de pacientes já conhecidos por apresentar doença. Neste caso, o ensaio inicial sinalizou corretamente um rearranjo incomum na região de F8, mas não pôde distinguir se era a inversão clássica que causa hemofilia A ou uma duplicação vizinha associada a uma síndrome diferente que frequentemente tem efeitos leves ou nulos em mulheres. Ao sobrepor a triagem rápida de primeira linha com tecnologias mais recentes que lêem trechos maiores de DNA, a equipe mostrou como separar essas possibilidades. Eles propõem uma abordagem em etapas: usar o teste rápido e barato de inversão como triagem inicial, mas acompanhar qualquer resultado positivo com mapeamento óptico do genoma ou sequenciamento de leitura longa para esclarecer se a alteração é realmente perigosa. Para as famílias, isso significa que um resultado de triagem preocupante deve ser visto como o começo de uma investigação mais cuidadosa — não como a palavra final.
Citação: Yang, X., Maimaiti, S., Qi, Q. et al. Xq28 duplication not F8 inversion: integrated genetic reanalysis redefines prenatal carrier diagnosis. Sci Rep 16, 13390 (2026). https://doi.org/10.1038/s41598-026-43654-x
Palavras-chave: hemofilia A, teste genético pré-natal, duplicação no cromossomo X, triagem de portadoras, variantes estruturais do genoma