Clear Sky Science · de
Xq28-Duplikation statt F8-Inversion: integrierte genetische Nachanalyse definiert pränatale Trägerdiagnostik neu
Wenn ein Routine-Babyscreening eine zwiespältige Botschaft sendet
Erwartende Eltern greifen immer häufiger auf genetisches Träger-Screening zurück, um schwere vererbbare Erkrankungen vor der Geburt zu erkennen. Was aber, wenn ein vertrauenswürdiger Test ein alarmierendes Ergebnis liefert, das sich später als irreführend erweist? Diese Studie begleitet eine schwangere Frau, deren Screening zunächst vermuten ließ, sie könne eine schwere Blutgerinnungsstörung vererben, während weiterführende Tests eine ganz andere — und wesentlich komplexere — Veränderung in ihrer DNA zutage förderten. Der Fall zeigt sowohl die Stärken als auch die Fallstricke moderner Genetik und weshalb Bestätigungstests für reale Familien, die schwierige Entscheidungen treffen, wichtig sind.
Eine Blutungsstörung, die in den Genen beginnt
Im Mittelpunkt der Geschichte steht Hämophilie A, eine bekannte Blutungsstörung, die überwiegend Jungen betrifft. Sie wird durch schädliche Veränderungen in einem Gen auf dem X‑Chromosom namens F8 verursacht, das für ein blutgerinnungsförderndes Protein benötigt wird. Viele der schwersten Fälle entstehen durch eine bestimmte Umordnung in diesem Gen, bekannt als Inversion innerhalb einer langen DNA‑Region, dem Intron 22. Da diese Inversion häufig vorkommt und technisch relativ einfach nachweisbar ist, enthalten viele Träger-Screening‑Panels für Personen mit Kinderwunsch oder Schwangere eine spezifische Untersuchung, die nur auf genau diese eine Umordnung abzielt.
Wenn der erste Test in die falsche Richtung deutet
In diesem Fall unterzog sich eine gesunde 27‑jährige Frau früh in der Schwangerschaft einem erweiterten Träger-Screening. Ein spezieller Long‑Distance‑PCR‑Test deutete darauf hin, dass sie die klassische F8‑Inversion trug und damit potenziell Trägerin von Hämophilie A war. Verständlicherweise besorgt um ihr ungeborenes Kind ließ sie eine pränatale Diagnostik durchführen. Die Erstuntersuchung des Fetus schien dieselbe Inversion zu zeigen. Auf den ersten Blick schien es eine klare Sache: Mutter und Tochter trugen beide eine bekannte, hochriskante Variante für eine schwere Blutungsstörung.
Eine verborgene DNA‑Duplikation tritt zutage
Bei näherer Untersuchung zeigte sich ein komplexeres Bild. Ein genomweiter Test, der Gewinn und Verlust von DNA‑Segmenten erkennt — ein SNP‑Array — bestätigte nicht einfach eine Inversion. Stattdessen zeigte er, dass sowohl Mutter als auch Fetus eine zusätzliche Kopie eines etwa halben Megabasen großen Abschnitts am entfernten Ende des X‑Chromosoms hatten, einem Bereich bekannt als distales Xq28, das große Teile des F8‑Gens sowie mehrere gehirnbezogene Gene umfasst. Ergänzende Technologien, die lange DNA‑Abschnitte in einem Stück sichtbar machen — optische Genomkartierung und Langzeitsequenzierung — zeigten, dass diese zusätzliche Kopie aus einer Duplikation zwischen zwei nahezu identischen DNA‑Blöcken flankierend um die Region stammte. Wichtig war, dass das F8‑Gen selbst nicht invertiert war, sondern teilweise dupliziert in einer Weise, die seine Funktion intakt ließ.
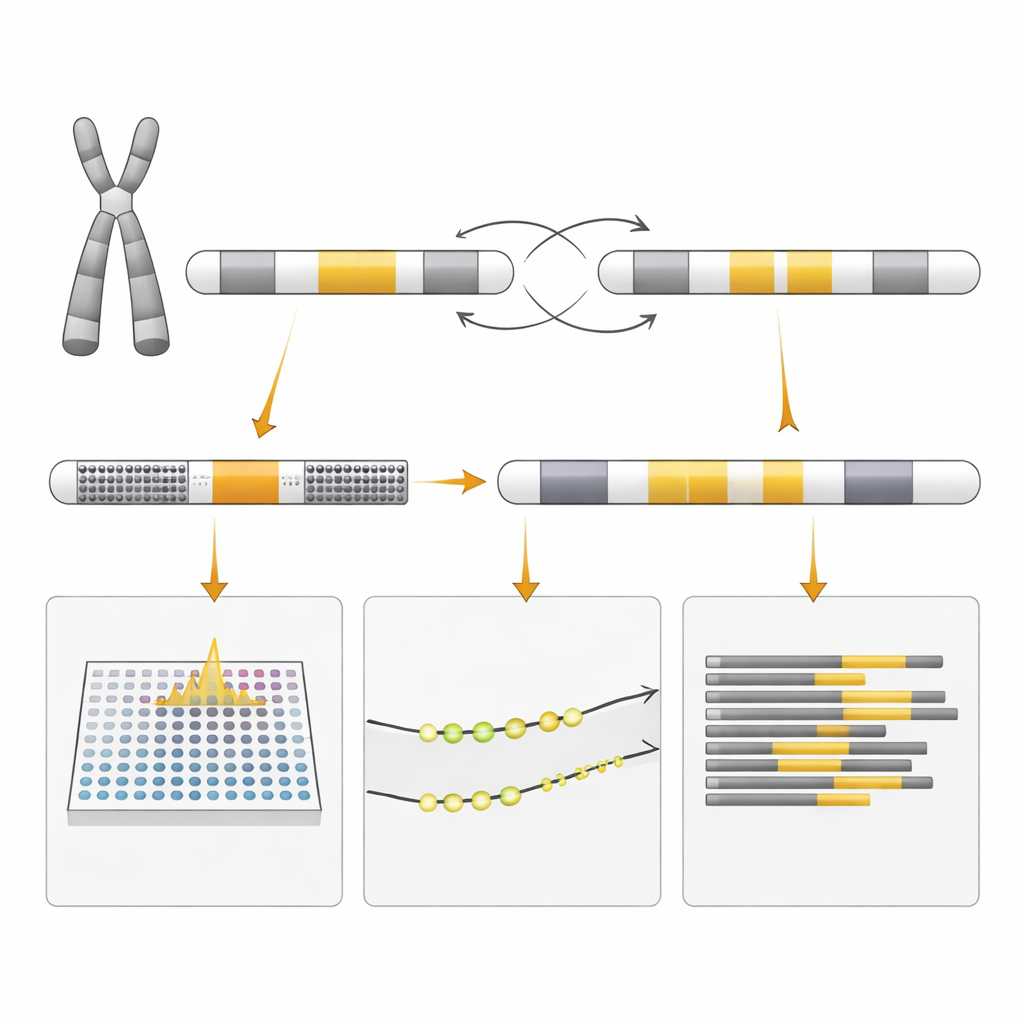
Dasselbe Signal, andere Bedeutung
Warum ergab der standardmäßige Inversionstest ein positives Ergebnis, wenn gar keine Inversion vorlag? Die Antwort liegt im Design des Tests. Er verwendet Paare von DNA‑Primern, die bei Personen ohne Umordnung ein bestimmtes Muster von Fragmenten erzeugen und bei Vorliegen der klassischen Inversion ein anderes Muster. Die durch Fehlpaarung zwischen wiederholten DNA‑Segmenten entstandene Duplikation erzeugte eine Mischung von Fragmenten, die das Inversionsmuster imitierte, obwohl die zugrunde liegende Struktur eine andere war. Nur die detaillierteren Methoden konnten klären, ob die DNA tatsächlich gedreht, kopiert oder beides war. Die Forschenden untersuchten außerdem, wie die beiden X‑Chromosomen bei Mutter und Fetus ein‑ oder ausgeschaltet wurden — ein Prozess, der als X‑Chromosomen‑Inaktivierung bezeichnet wird — um zu verstehen, warum die Mutter gesund war und mögliche Auswirkungen auf das Kind abzuschätzen, obwohl dies keine sichere Vorhersage erlaubte.
Was das für Familien und Kliniken bedeutet
Die zentrale Lehre ist, dass selbst lang etablierte, vertrauenswürdige Tests irreführend sein können, wenn sie breit in gesunden Populationen angewendet werden statt bei bereits erkrankten Patienten. In diesem Fall wies das anfängliche Verfahren korrekt auf eine ungewöhnliche Umordnung im F8‑Bereich hin, konnte jedoch nicht unterscheiden, ob es sich um die klassische Inversion handelte, die Hämophilie A verursacht, oder um eine benachbarte Duplikation, die mit einem anderen Syndrom assoziiert ist und bei Frauen oft milde oder keine Effekte hat. Durch das Schichten einfacher Ersttests mit neueren Techniken, die längere DNA‑Abschnitte lesen, zeigte das Team, wie sich diese Möglichkeiten unterscheiden lassen. Sie schlagen einen stufenweisen Ansatz vor: den schnellen, kostengünstigen Inversionstest als erste Stufe verwenden, bei jedem positiven Befund jedoch mit optischer Genomkartierung oder Langzeitsequenzierung nachzuklären, ob die Veränderung tatsächlich gefährlich ist. Für Familien bedeutet das: Ein beunruhigendes Screening‑Ergebnis sollte als Beginn einer sorgfältigeren Untersuchung verstanden werden — nicht als endgültiges Urteil.
Zitation: Yang, X., Maimaiti, S., Qi, Q. et al. Xq28 duplication not F8 inversion: integrated genetic reanalysis redefines prenatal carrier diagnosis. Sci Rep 16, 13390 (2026). https://doi.org/10.1038/s41598-026-43654-x
Schlüsselwörter: Hämophilie A, pränatale Gentests, Duplikation des X‑Chromosoms, Träger-Screening, strukturelle Varianten im Genom