Clear Sky Science · es
Duplicación en Xq28, no inversión en F8: reanálisis genético integrado redefine el diagnóstico prenatal de portadoras
Cuando una prueba de rutina para el bebé envía un mensaje confuso
Cada vez más futuros padres recurren al cribado genético de portadoras para detectar enfermedades hereditarias graves antes del nacimiento. Pero, ¿qué ocurre cuando una prueba de confianza da un resultado alarmante que después resulta ser engañoso? Este estudio sigue el caso de una mujer embarazada cuyo cribado sugirió que podría transmitir un trastorno hemorrágico grave, y en el que pruebas más avanzadas revelaron un cambio en su ADN muy distinto —y mucho menos directo—. El caso muestra tanto el poder como las limitaciones de la genética moderna, y por qué las pruebas confirmatorias importan para familias reales que tienen que tomar decisiones difíciles.
Un trastorno hemorrágico que comienza en los genes
La historia se centra en la hemofilia A, un conocido trastorno hemorrágico que afecta sobre todo a los varones. Se debe a cambios dañinos en un gen del cromosoma X llamado F8, necesario para fabricar una proteína que ayuda a la coagulación. Muchos de los casos más graves provienen de un tipo particular de reorganización en este gen, conocida como inversión en un tramo largo de ADN llamado intrón 22. Debido a que esta inversión es frecuente y técnicamente fácil de detectar, muchos paneles de cribado de portadoras para personas que planean un embarazo o que ya están embarazadas incluyen un ensayo específico que busca solo esa inversión concreta.
Cuando la primera prueba señala en la dirección equivocada
En este caso, una mujer sana de 27 años se sometió a un panel ampliado de cribado de portadoras al inicio del embarazo. Una prueba especializada de PCR de largo alcance sugirió que era portadora de la inversión clásica en F8, lo que la marcó como posible portadora de hemofilia A. Con razón preocupada por su futuro hijo, se sometió a pruebas prenatales. Las pruebas iniciales en el feto parecían mostrar la misma inversión. A primera vista, parecía una historia sencilla: madre e hija portadoras de una variante conocida de alto riesgo para una enfermedad hemorrágica grave.
Una repetición de ADN oculta sale a la luz
Una inspección más detallada contó una historia más compleja. Una prueba a escala genómica que busca ganancias y pérdidas de segmentos de ADN—llamada microarray de SNP—no confirmó simplemente una inversión. En su lugar, reveló que tanto la madre como el feto tenían una copia adicional de una región de medio megabase en el extremo distal del cromosoma X, un área conocida como Xq28 distal que incluye gran parte del gen F8 junto con varios genes relacionados con el cerebro. Tecnologías adicionales capaces de leer tramos largos de ADN en una sola pieza—mapeo genómico óptico y secuenciación de lecturas largas—mostraron que esta copia extra procedía de una duplicación entre dos bloques de ADN casi idénticos que flanquean la región. De forma crucial, el gen F8 en sí no estaba invertido, sino parcialmente duplicado de una manera que dejó su función intacta.
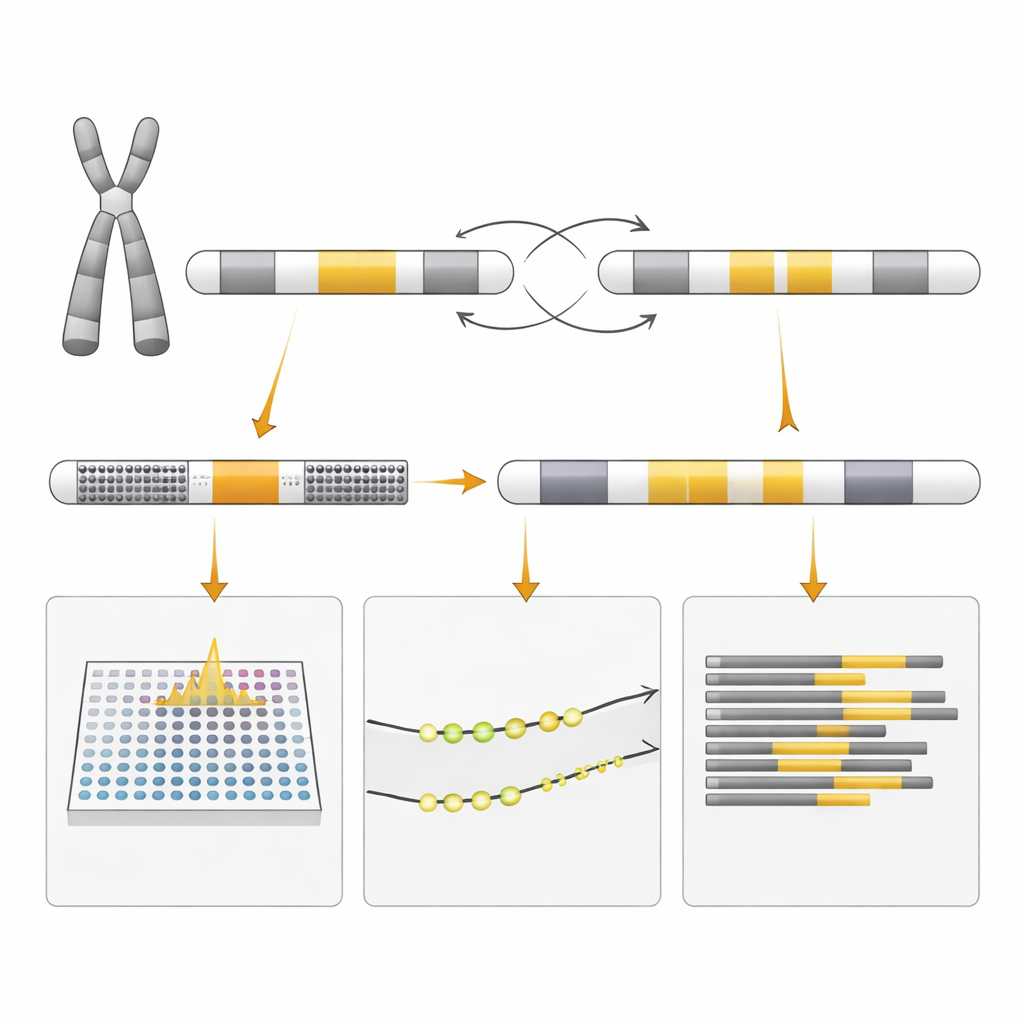
Misma señal, significado diferente
¿Por qué la prueba estándar de inversión pareció positiva si no había inversión? La respuesta radica en el diseño de la prueba. Emplea pares de cebadores de ADN que normalmente producen un patrón de fragmentos en personas sin reorganizaciones y un patrón distinto cuando está presente la inversión clásica. La duplicación creada por un emparejamiento indebido entre segmentos repetidos de ADN generó una mezcla de fragmentos que imitó el patrón de inversión, aunque la estructura subyacente fuera distinta. Solo los métodos más detallados pudieron desenredar si el ADN estaba realmente invertido, copiado o ambas cosas. Los investigadores también examinaron cómo se activan o desactivan los dos cromosomas X en madre y feto, un proceso llamado inactivación del cromosoma X, para entender por qué la madre estaba sana y estimar posibles efectos en la criatura, aunque esto no pudo predecir el resultado con certeza.
Qué significa esto para familias y clínicas
La lección clave es que incluso pruebas consolidadas y de larga trayectoria pueden inducir a error cuando se aplican de forma amplia en poblaciones sanas en lugar de en pacientes ya conocidos con la enfermedad. En este caso, el ensayo inicial señaló correctamente una reorganización inusual en la región de F8, pero no pudo decir si se trataba de la inversión clásica que causa hemofilia A o de una duplicación vecina asociada a un síndrome diferente que suele tener efectos leves o nulos en las mujeres. Al superponer el cribado simple de primera línea con tecnologías más nuevas que leen fragmentos de ADN más largos, el equipo mostró cómo distinguir estas posibilidades. Proponen un enfoque por fases: usar la prueba rápida y económica de inversión como primera pasada, pero dar seguimiento a cualquier resultado positivo con mapeo genómico óptico o secuenciación de lecturas largas para clarificar si el cambio es realmente peligroso. Para las familias, esto significa que un resultado inquietante en el cribado debe entenderse como el inicio de una investigación más cuidadosa, no como la última palabra.
Cita: Yang, X., Maimaiti, S., Qi, Q. et al. Xq28 duplication not F8 inversion: integrated genetic reanalysis redefines prenatal carrier diagnosis. Sci Rep 16, 13390 (2026). https://doi.org/10.1038/s41598-026-43654-x
Palabras clave: hemofilia A, pruebas genéticas prenatales, duplicación del cromosoma X, cribado de portadoras, variantes estructurales del genoma