Clear Sky Science · sv
Karakteristika för NK‑cellsaktivering efter stimulering med cytokinerna IL‑12, IL‑15, IL‑18 för prekliniska ändamål
Varför det spelar roll att ”superladda” immunceller
Cancerbehandlingar försöker i allt större utsträckning hjälpa kroppen att läka sig själv genom att stärka dess egna försvar. Bland våra immungardister sticker natural killer‑celler (NK‑celler) ut eftersom de snabbt kan upptäcka och förstöra abnorma celler, inklusive många tumörer. NK‑celler tagna direkt från kroppen är dock ofta tröga. Denna studie ställer en praktisk fråga för framtida cancerbehandlingar: vilka ”immunväxtfaktorer” väcker bäst upp NK‑celler i laboratoriet så att de blir starka, säkra och redo att attackera tumörer när de återförs till patienter?
Hur kroppens förstainsatser fungerar
NK‑celler är en del av det medfödda immunförsvaret och fungerar som snabba insatsenheter mot virusinfekterade och cancerösa celler. De dödar genom att släppa giftiga paket samt genom att sända fara‑signaler som mobiliserar andra immunceller. Deras beteende påverkas starkt av kemiska budbärare kallade cytokiner, som antingen kan få dem i gång eller hålla dem tysta. Kliniker och forskare använder redan vissa av dessa cytokiner, såsom IL‑2 och IL‑15, för att odla NK‑celler utanför kroppen, men dessa substanser kan ge biverkningar eller till och med utarma NK‑celler om de används felaktigt. Nyare kombinationer, särskilt trion IL‑12, IL‑15 och IL‑18, har föreslagits som ett sätt att skapa långlivade, ”minneslika” NK‑celler som svarar kraftfullare när de möter cancer.
Tester av olika recept för immunstärkning
För att jämföra dessa tillvägagångssätt mot varandra isolerade forskarna NK‑celler från mjälten hos två vanliga laboratoriemusstammar. De utsatte sedan cellerna i 24 timmar för olika enskilda cytokiner, par och IL‑12/IL‑15/IL‑18‑cocktailen, samt för en STING‑vägaktivator kallad cGAMP som är känd för att stimulera immunsvar. De mätte hur många NK‑celler som överlevde, vilka ”på”‑ och ”av”‑switchar som dök upp på deras ytor, hur mycket av dödsmolekylen granzyme B de bar och vilka inflammatoriska signaler de producerade. Slutligen samexponerade de dessa NK‑celler med två typer av muscancerceller: en som visar normala själv‑markörer (MHC‑positiv) och en som förlorat dessa markörer (MHC‑negativ), ett vanligt knep tumörer använder för att undkomma andra immunceller.
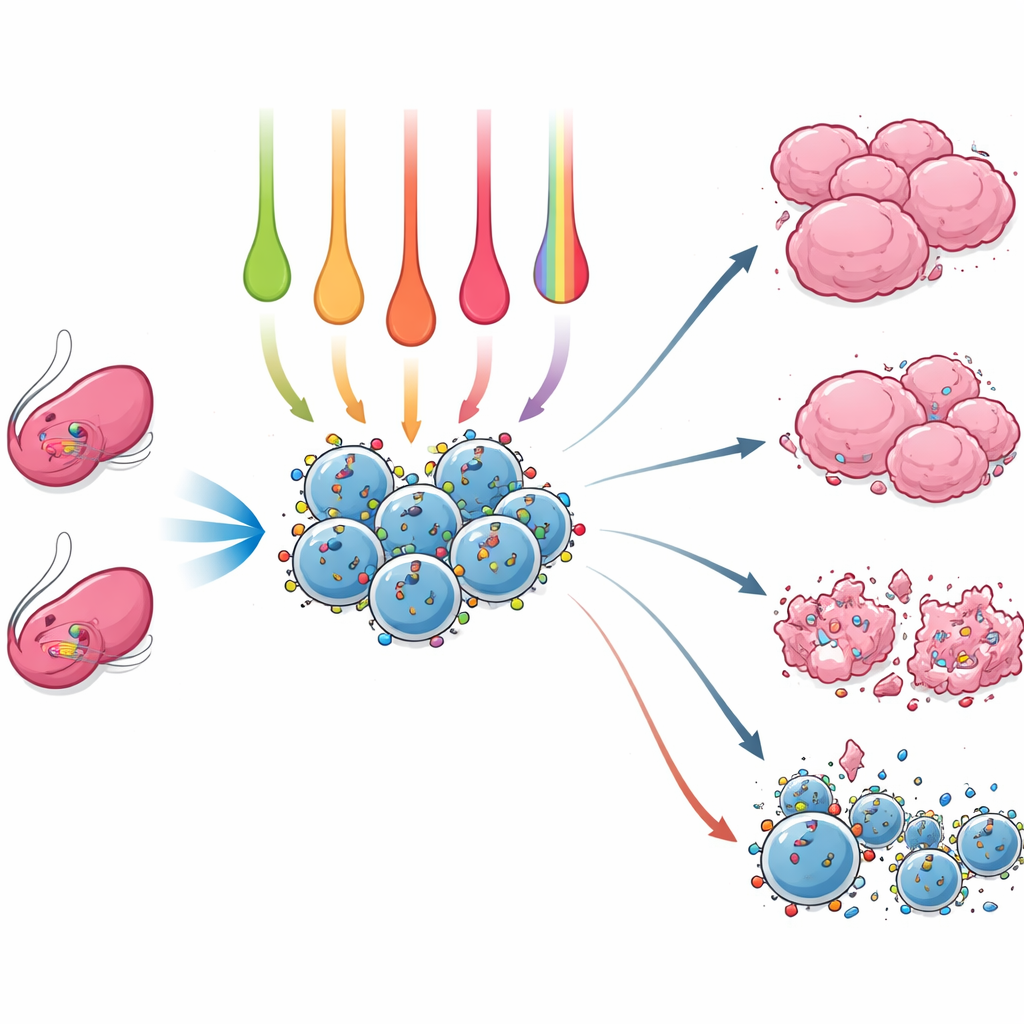
Vad som gör NK‑celler starkast
Olika aktiveringsrecept producerade slående olika NK‑cellsprofiler. IL‑15 ensam gav högst korttidsöverlevnad och goda nivåer av aktiverande receptorer och granzyme B, vilket gör det till en stark allmän förstärkare. Att lägga till IL‑12 till IL‑15 ökade ytterligare produktionen av vissa signalmolekyler, såsom IFN‑gamma och CCL3, som hjälper till att samordna bredare immunattacker. Men de mest dramatiska förändringarna kom från trippelblandningen IL‑12, IL‑15 och IL‑18. Denna cocktail förvandlade NK‑celler till potenta fabriker av proinflammatoriska cytokiner och kemokiner, vilket kraftigt ökade IFN‑gamma och andra signaler som kan rekrytera och aktivera ytterligare immunceller. Dessa ”minneslika” NK‑celler visade också högre nivåer av den tidiga aktiveringsmarkören CD69, även om deras överlevnad var något lägre och deras granzyme B‑innehåll inte översteg vissa enklare behandlingar.
Från petriskål till tumörkontroll
När dessa olika förberedda NK‑celler placerades tillsammans med cancerceller kunde alla aktiverade grupper begränsa tumörtillväxt och inducera cancercelldöd, oavsett om målcellernas bar normala själv‑markörer eller hade förlorat dem. Trippelcytokincocktailen och IL‑12/IL‑15‑paret tenderade att ge tydligare synlig skada på cancercellslagren och långsammare tumörcellsproliferation, särskilt mot melanomceller som saknade själv‑markörer. Däremot var långvarig exponering för STING‑agonisten cGAMP ensam skadlig för NK‑celler, med en kraftig minskning av deras överlevnad och dämpning av deras funktionella markörer, vilket tyder på att denna typ av stimulans måste tajmas noggrant eller kombineras med skyddande cytokiner som IL‑15.
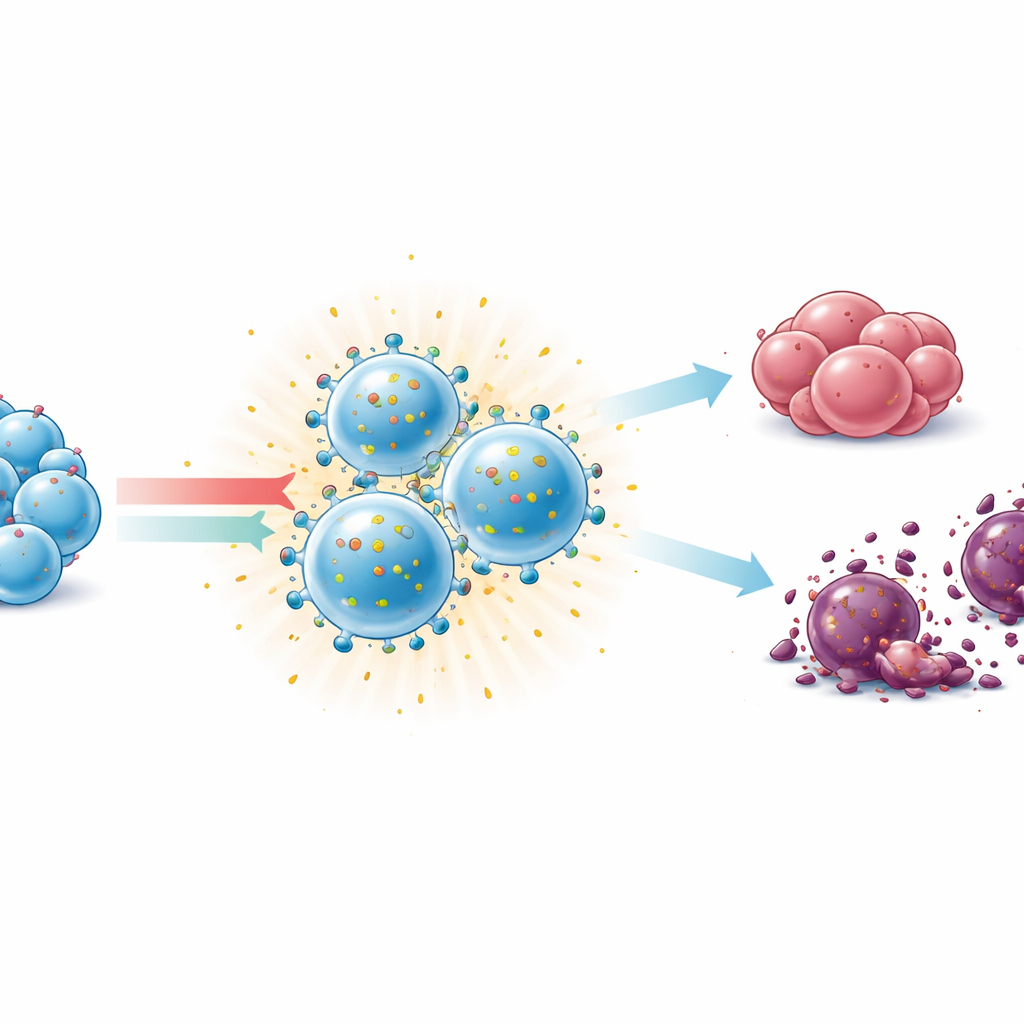
Vad detta innebär för framtidens cancervård
Sammantaget visar fynden att inte alla immunstyrkande signaler är likvärdiga. IL‑15 framstår som ett pålitligt sätt att hålla NK‑celler vid liv och redo, medan kombinationen IL‑12/IL‑15/IL‑18 skapar starkt aktiverade, minneslika NK‑celler som frisätter kraftfulla inflammatoriska signaler och kan hämma tillväxten av både ”synliga” och ”dolda” tumörceller i labbet. Även om dessa experiment gjordes på möss och i odlingsskålar snarare än på patienter, stödjer de användningen av IL‑12/IL‑15/IL‑18‑cocktailen för att förbereda NK‑celler för adoptiv cellterapi. I praktiska termer hjälper detta arbete att förfina receptet för att odla smartare, tuffare NK‑celler som en dag kan ge läkare ett säkrare och effektivare sätt att värva immunförsvaret mot cancer.
Citering: Czapla, J., Drzyzga, A. & Smolarczyk, R. Characteristics of NK cells activation following IL-12, IL-15, IL-18 cytokines stimulation for preclinical purposes. Sci Rep 16, 13665 (2026). https://doi.org/10.1038/s41598-026-42816-1
Nyckelord: natural killer cells, cytokine therapy, cancer immunotherapy, memory-like NK cells, adoptive cell therapy