Clear Sky Science · pl
Charakterystyka aktywacji komórek NK po stymulacji cytokinami IL-12, IL-15, IL-18 w celach przedklinicznych
Dlaczego „doładowanie” komórek odpornościowych ma znaczenie
Terapie przeciwnowotworowe coraz częściej próbują pomóc organizmowi w samoleczeniu poprzez wzmocnienie własnych mechanizmów obronnych. Wśród strażników układu odpornościowego wyróżniają się komórki NK (natural killers), ponieważ potrafią szybko rozpoznawać i niszczyć nieprawidłowe komórki, w tym wiele nowotworów. Jednak komórki NK pobrane bezpośrednio z organizmu często wykazują słabą aktywność. W tym badaniu stawiono praktyczne pytanie istotne dla przyszłych terapii przeciwnowotworowych: które „czynniki wzrostu odpornościowego” najlepiej pobudzają komórki NK in vitro, aby były silne, bezpieczne i gotowe do ataku na guzy po podaniu pacjentowi?
Jak działają pierwsi reagujący organizmu
Komórki NK należą do wrodzonego układu odpornościowego i pełnią funkcję szybkiej odpowiedzi przeciwko komórkom zakażonym wirusem oraz nowotworowym. Niszczenie odbywa się poprzez uwalnianie toksycznych pęcherzyków oraz wysyłanie sygnałów alarmowych, które mobilizują inne komórki odpornościowe. Ich zachowanie jest w dużej mierze zależne od przekaźników chemicznych zwanych cytokinami, które mogą je pobudzać lub hamować. Klinicyści i badacze już stosują niektóre z tych cytokin, takie jak IL-2 i IL-15, do hodowli komórek NK poza organizmem, ale substancje te mogą wywoływać działania niepożądane lub nawet prowadzić do wyczerpania komórek NK przy niewłaściwym stosowaniu. Nowe kombinacje, zwłaszcza trio IL-12, IL-15 i IL-18, zaproponowano jako metodę uzyskania dłużej żyjących, „pamięciopodobnych” komórek NK, które reagują silniej w kontakcie z rakiem.
Testowanie różnych „przepisów” na wzmocnienie odporności
Aby porównać te podejścia bezpośrednio, badacze wyizolowali komórki NK z śledzion dwóch powszechnie stosowanych szczepów myszy laboratoryjnych. Następnie przez 24 godziny wystawiali komórki na działanie pojedynczych cytokin, par oraz koktajlu IL-12/IL-15/IL-18, a także na aktywator szlaku STING o nazwie cGAMP, znany ze stymulacji odpowiedzi odpornościowej. Mierzono liczbę przetrwających komórek NK, występowanie receptorów „włączających” i „wyłączających” na ich powierzchni, zawartość enzymu zabijającego — granzymu B, oraz profil produkowanych przez nie sygnałów zapalnych. Na koniec współhodowano te komórki NK z dwoma typami mysich komórek nowotworowych: jednymi prezentującymi normalne markery własne (MHC-dodatnie) i drugimi, które utraciły te markery (MHC-ujemne), co jest częstym trikiem nowotworów ułatwiającym ucieczkę przed innymi elementami układu odpornościowego.
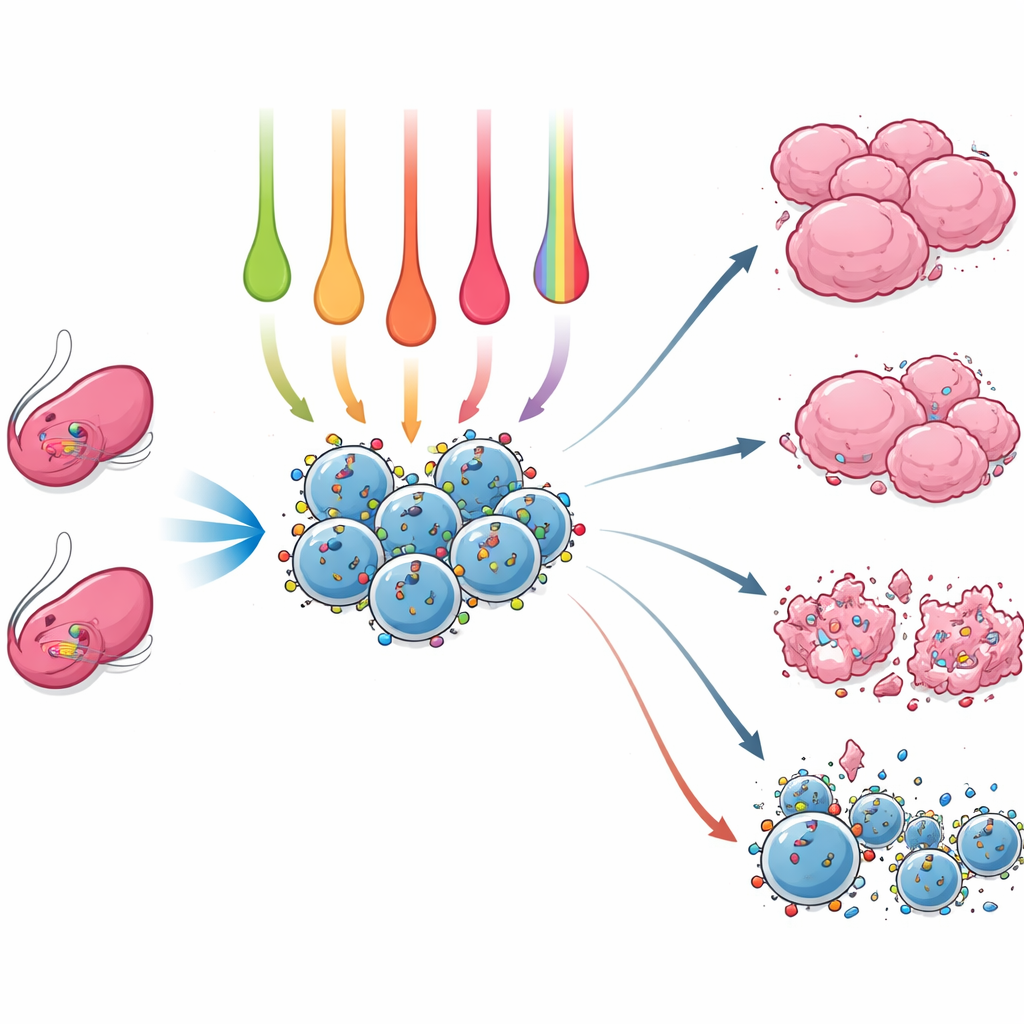
Co czyni komórki NK najsilniejszymi
Różne „przepisy” aktywacji dały wyraźnie różne profile komórek NK. Samo IL-15 zapewniało najwyższą krótkoterminową przeżywalność oraz dobre poziomy receptorów aktywujących i granzymu B, co czyni je solidnym, ogólnym wzmacniaczem. Dodanie IL-12 do IL-15 zwiększało wytwarzanie niektórych cząsteczek sygnałowych, takich jak IFN-gamma i CCL3, które wspomagają koordynację szerszej odpowiedzi immunologicznej. Najbardziej dramatyczne zmiany wywołał jednak potrójny koktajl IL-12, IL-15 i IL-18. Ta mieszanka przekształcała komórki NK w wydajne fabryki cytokin prozapalnych i chemokin, znacznie podnosząc poziomy IFN-gamma i innych sygnałów zdolnych rekrutować i aktywować kolejne komórki odpornościowe. Te „pamięciopodobne” komórki NK wykazywały także wyższe poziomy wczesnego markera aktywacji CD69, chociaż ich przeżywalność była nieco niższa, a zawartość granzymu B nie przewyższała tej uzyskanej przy niektórych prostszych schematach.
Od szalki do kontroli guza
Gdy różnie przygotowane komórki NK zestawiono z komórkami nowotworowymi, wszystkie aktywowane grupy potrafiły ograniczyć wzrost guza i indukować śmierć komórek nowotworowych, niezależnie od tego, czy cele miały normalne markery własne, czy je utraciły. Koktajl trzech cytokin oraz para IL-12/IL-15 miały tendencję do wywoływania silniejszych widocznych uszkodzeń warstw komórek nowotworowych i wolniejszej proliferacji komórek guza, szczególnie wobec komórek czerniaka pozbawionych markerów własnych. Natomiast długotrwała ekspozycja wyłącznie na agonistę STING, cGAMP, była szkodliwa dla komórek NK — wyraźnie redukowała ich przeżywalność i osłabiała ich funkcjonalne markery, co sugeruje, że tego typu bodziec musi być precyzyjnie dawkowany lub łączony z ochronnymi cytokinami, takimi jak IL-15.
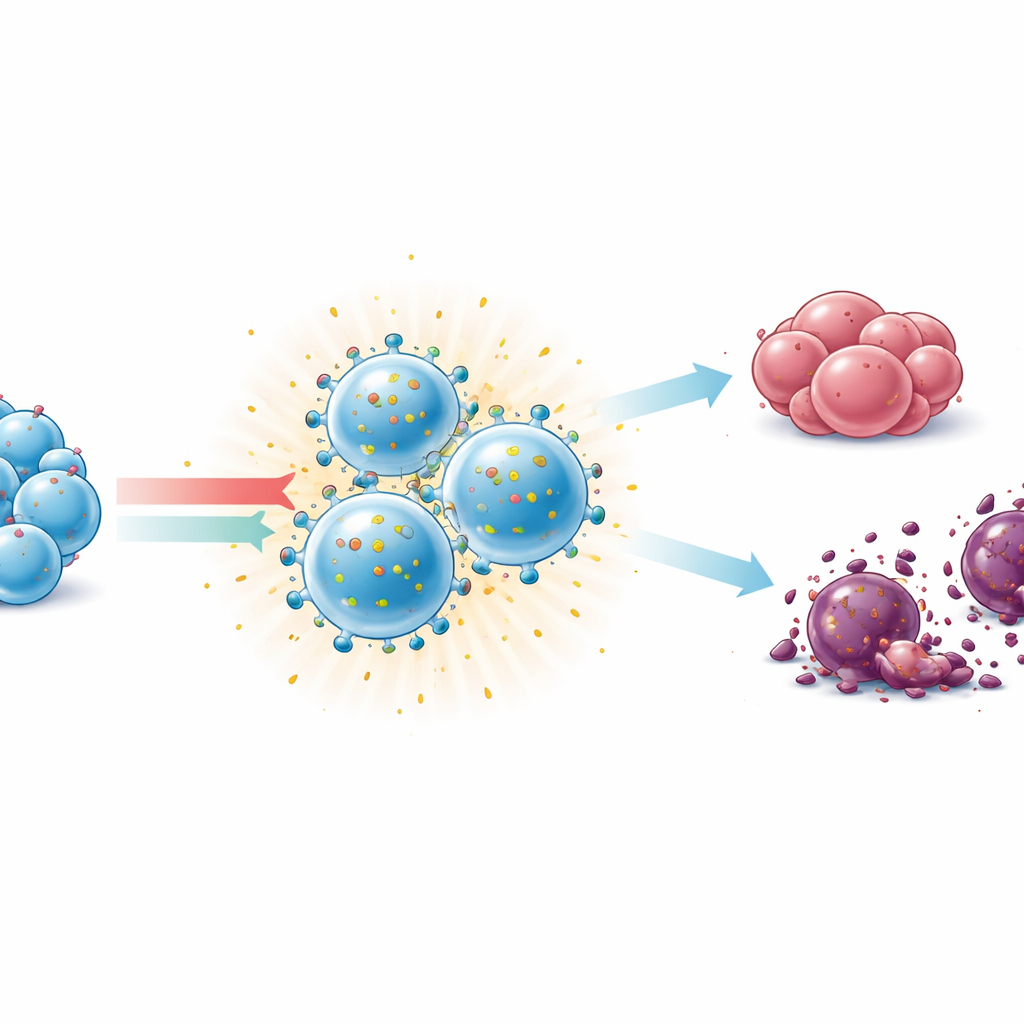
Co to oznacza dla przyszłej opieki przeciwnowotworowej
Podsumowując, wyniki podkreślają, że nie wszystkie sygnały wzmacniające odporność są sobie równe. IL-15 wyróżnia się jako wiarygodny środek utrzymujący komórki NK przy życiu i w stanie gotowości, podczas gdy kombinacja IL-12/IL-15/IL-18 tworzy silnie aktywowane, pamięciopodobne komórki NK wydzielające potężne sygnały zapalne i zdolne do hamowania wzrostu zarówno „widocznych”, jak i „ukrytych” komórek nowotworowych in vitro. Chociaż eksperymenty przeprowadzono na mysich modelach i w warunkach in vitro, a nie u pacjentów, wyniki wspierają zastosowanie koktajlu IL-12/IL-15/IL-18 do przygotowywania komórek NK do terapii adoptatywnej. W praktycznym wymiarze praca ta pomaga dopracować przepis na hodowlę „mądrzejszych”, twardszych komórek NK, które mogą kiedyś dać lekarzom bezpieczniejszy i skuteczniejszy sposób wykorzystania układu odpornościowego przeciwko nowotworom.
Cytowanie: Czapla, J., Drzyzga, A. & Smolarczyk, R. Characteristics of NK cells activation following IL-12, IL-15, IL-18 cytokines stimulation for preclinical purposes. Sci Rep 16, 13665 (2026). https://doi.org/10.1038/s41598-026-42816-1
Słowa kluczowe: komórki natural killers, terapia cytokinowa, immunoterapia przeciwnowotworowa, komórki NK o pamięciowej charakterystyce, terapia adoptatywna komórek