Clear Sky Science · fr
Caractéristiques de l’activation des cellules NK après stimulation par les cytokines IL-12, IL-15, IL-18 à des fins précliniques
Pourquoi il est important de suralimenter les cellules immunitaires
Les traitements du cancer cherchent de plus en plus à aider le corps à se guérir lui‑même en renforçant ses propres défenses. Parmi nos gardiens immunitaires, les cellules tueuses naturelles (NK) se démarquent car elles peuvent repérer et détruire rapidement des cellules anormales, y compris de nombreux cancers. Cependant, les NK fraîchement isolées sont souvent peu réactives. Cette étude pose une question pratique pour les futurs traitements : quels « facteurs de croissance immunitaire » réveillent le mieux les NK en laboratoire afin qu’elles soient puissantes, sûres et prêtes à attaquer les tumeurs lorsqu’on les réinjecte aux patients ?
Comment fonctionnent les premiers intervenants de l’organisme
Les NK font partie de l’immunité innée, agissant comme des unités d’intervention rapide contre les cellules infectées par des virus et les cellules tumorales. Elles tuent en libérant des paquets toxiques et en émettant des signaux d’alerte qui mobilisent d’autres cellules immunitaires. Leur comportement dépend fortement de messagers chimiques appelés cytokines, qui peuvent soit les stimuler soit les maintenir au repos. Les cliniciens et chercheurs utilisent déjà certaines de ces cytokines, comme l’IL‑2 et l’IL‑15, pour cultiver des NK hors du corps, mais ces substances peuvent provoquer des effets indésirables ou même épuiser les NK si elles sont mal utilisées. De nouvelles combinaisons, en particulier le trio IL‑12, IL‑15 et IL‑18, ont été proposées pour créer des NK plus durables, « à mémoire », qui répondent plus fortement au contact du cancer.
Tester différentes recettes de stimulation immunitaire
Pour comparer ces approches, les chercheurs ont isolé des NK de la rate de deux souches de souris de laboratoire courantes. Ils ont ensuite exposé les cellules pendant 24 heures à différentes cytokines seules, par paires, au cocktail IL‑12/IL‑15/IL‑18, ainsi qu’à un activateur de la voie STING appelé cGAMP, connu pour stimuler les réponses immunitaires. Ils ont mesuré la survie des NK, l’expression des récepteurs activateurs et inhibiteurs à leur surface, la quantité de granzyme B portée, et les signaux inflammatoires qu’elles produisaient. Enfin, ils ont co‑cultivé ces NK avec deux types de cellules cancéreuses murines : une exprimant des marqueurs du soi normaux (MHC‑positives) et une ayant perdu ces marqueurs (MHC‑négatives), un stratagème fréquent des tumeurs pour échapper à d’autres cellules immunitaires.
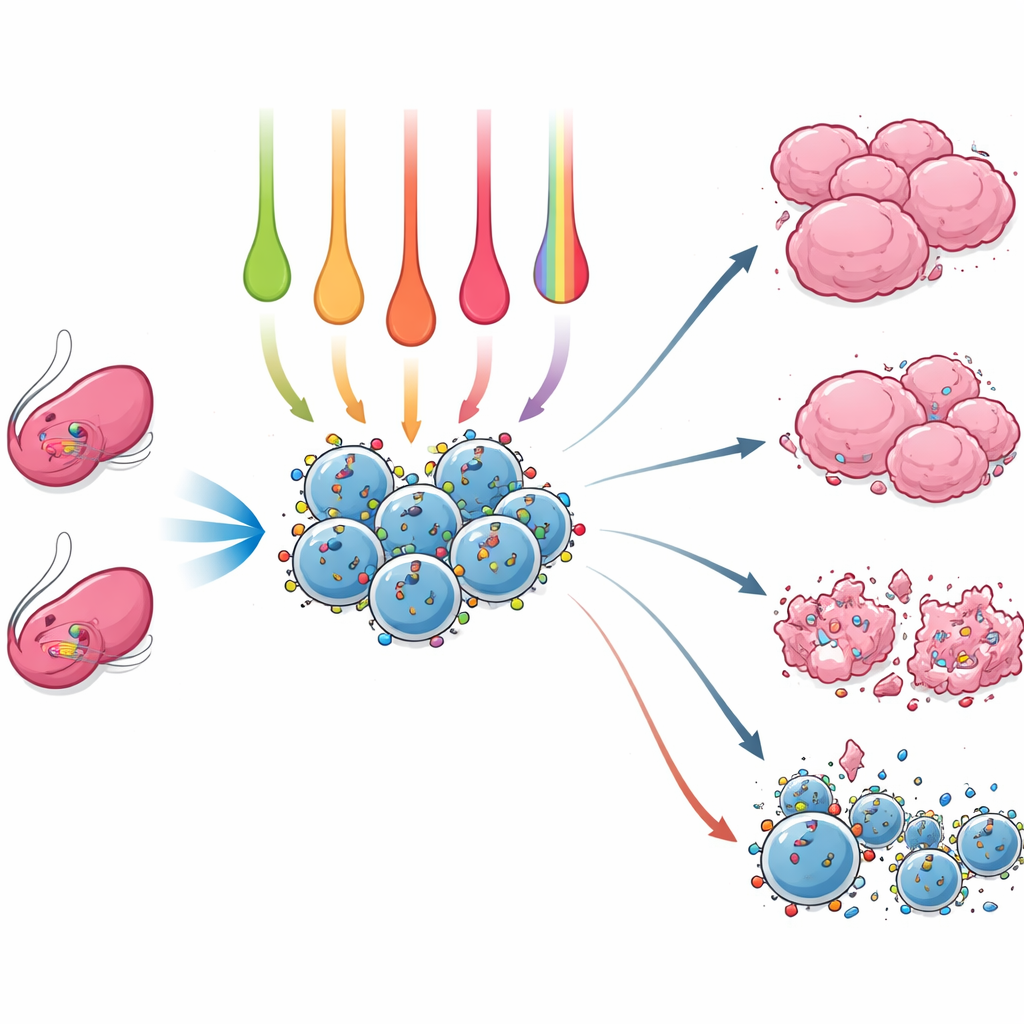
Ce qui rend les NK les plus puissantes
Les différentes recettes d’activation ont produit des profils de NK nettement distincts. L’IL‑15 seule a assuré la meilleure survie à court terme et des niveaux satisfaisants de récepteurs activateurs et de granzyme B, en faisant un bon stimulateur général. L’ajout d’IL‑12 à l’IL‑15 a encore augmenté la production de certaines molécules de signalisation, comme l’IFN‑gamma et la CCL3, qui aident à coordonner une réponse immunitaire plus large. Mais les changements les plus spectaculaires sont venus du mélange triple IL‑12/IL‑15/IL‑18. Ce cocktail a transformé les NK en véritables usines de cytokines et chimiokines pro‑inflammatoires, en augmentant fortement l’IFN‑gamma et d’autres signaux capables de recruter et d’activer des cellules immunitaires supplémentaires. Ces NK « à mémoire » montraient aussi des niveaux plus élevés du marqueur d’activation précoce CD69, même si leur survie était un peu moindre et que leur contenu en granzyme B ne dépassait pas celui de certains traitements plus simples.
De l’assiette de laboratoire au contrôle tumoral
Lorsque ces NK préparées différemment ont été mises en contact avec des cellules cancéreuses, tous les groupes activés ont été capables de limiter la croissance tumorale et d’induire la mort des cellules cancéreuses, que les cibles expriment des marqueurs du soi ou les aient perdus. Le cocktail triple et la paire IL‑12/IL‑15 ont tendance à provoquer des dommages visibles plus importants aux couches de cellules tumorales et à ralentir la prolifération des cellules tumorales, notamment contre des mélanomes dépourvus de marqueurs du soi. En revanche, une exposition prolongée à l’agoniste STING cGAMP seul s’est révélée toxique pour les NK, réduisant fortement leur survie et atténuant leurs marqueurs fonctionnels, ce qui suggère que ce type de stimulation doit être minutieusement synchronisé ou associé à des cytokines protectrices comme l’IL‑15.
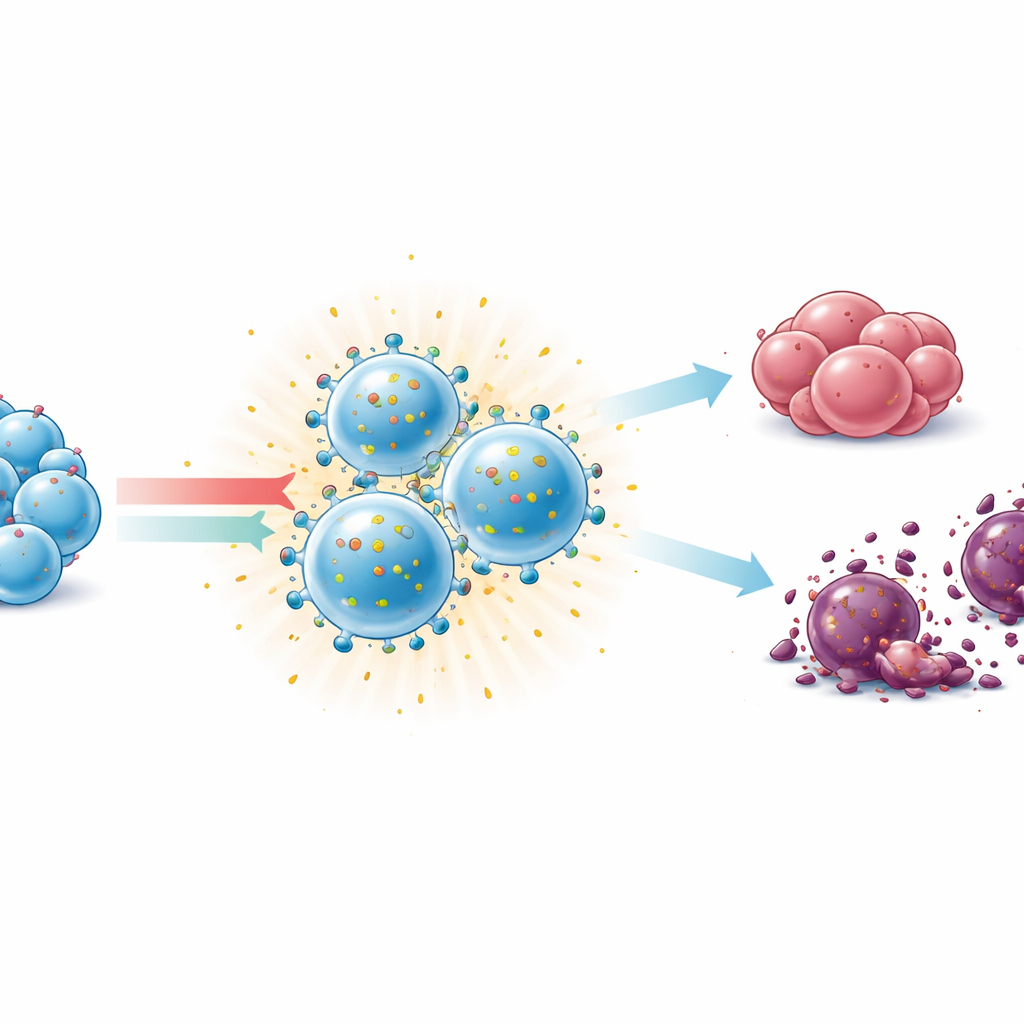
Ce que cela implique pour les soins du cancer à venir
Dans l’ensemble, les résultats soulignent que tous les signaux de renforcement immunitaire ne se valent pas. L’IL‑15 se distingue comme un moyen fiable de maintenir les NK en vie et prêtes, tandis que la combinaison IL‑12/IL‑15/IL‑18 génère des NK hautement activées, à mémoire, qui libèrent de puissants signaux inflammatoires et peuvent freiner la croissance de cellules tumorales « visibles » et « cachées » en laboratoire. Bien que ces expériences aient été réalisées chez la souris et en cultures cellulaires plutôt que chez des patients, elles confortent l’usage du cocktail IL‑12/IL‑15/IL‑18 pour préparer des NK destinées à la thérapie cellulaire adoptive. Concrètement, ce travail aide à affiner la recette pour produire des NK plus intelligentes et plus résistantes qui pourraient un jour offrir aux médecins une manière plus sûre et plus efficace de mobiliser le système immunitaire contre le cancer.
Citation: Czapla, J., Drzyzga, A. & Smolarczyk, R. Characteristics of NK cells activation following IL-12, IL-15, IL-18 cytokines stimulation for preclinical purposes. Sci Rep 16, 13665 (2026). https://doi.org/10.1038/s41598-026-42816-1
Mots-clés: cellules tueuses naturelles, thérapie par cytokines, immunothérapie du cancer, cellules NK à mémoire, thérapie cellulaire adoptive