Clear Sky Science · es
Características de la activación de las células NK tras la estimulación con las citocinas IL-12, IL-15 e IL-18 para fines preclínicos
Por qué importa potenciar las células inmunitarias
Las terapias contra el cáncer intentan cada vez más ayudar al organismo a curarse a sí mismo potenciando sus propias defensas. Entre nuestros guardianes inmunitarios, las células asesinas naturales (NK) destacan porque pueden identificar y destruir con rapidez células anormales, incluidos muchos tumores. Sin embargo, las NK recién extraídas del organismo suelen estar poco activas. Este estudio plantea una pregunta práctica para futuros tratamientos contra el cáncer: ¿qué “factores de crecimiento inmunitarios” despiertan mejor a las NK en el laboratorio para que sean potentes, seguras y estén listas para atacar tumores cuando se devuelvan a los pacientes?
Cómo funcionan los primeros respondedores del cuerpo
Las NK forman parte del sistema inmunitario innato y actúan como unidades de respuesta rápida frente a células infectadas por virus y células cancerosas. Matan liberando paquetes tóxicos y emitiendo señales de alarma que movilizan a otras células inmunitarias. Su comportamiento depende en gran medida de mensajeros químicos llamados citocinas, que pueden estimularlas o mantenerlas en calma. Clínicos e investigadores ya emplean algunas de estas citocinas, como IL-2 e IL-15, para expandir NK fuera del cuerpo, pero estas sustancias pueden causar efectos secundarios o incluso agotar a las NK si se usan incorrectamente. Se han propuesto combinaciones más recientes, especialmente un trío de citocinas IL-12, IL-15 e IL-18, como forma de generar células NK de vida más prolongada y “tipo memoria” que responden con más fuerza al encontrarse con el cáncer.
Probando distintas recetas para potenciar la respuesta inmune
Para comparar estos enfoques cara a cara, los investigadores aislaron NK del bazo de dos cepas de ratón de laboratorio comunes. A continuación expusieron las células durante 24 horas a distintas citocinas individuales, pares y al cóctel IL-12/IL-15/IL-18, así como a un activador de la vía STING llamado cGAMP, conocido por estimular respuestas inmunitarias. Midieron cuántas NK sobrevivían, qué interruptores de “encendido” y “apagado” aparecían en su superficie, cuánto de la enzima letal granzima B contenían y qué señales inflamatorias producían. Finalmente, co-cultivaron estas NK con dos tipos de células tumorales de ratón: una que muestra marcadores propios normales (MHC-positivo) y otra que ha perdido estos marcadores (MHC-negativo), un truco común que usan los tumores para escapar de otras células inmunitarias.
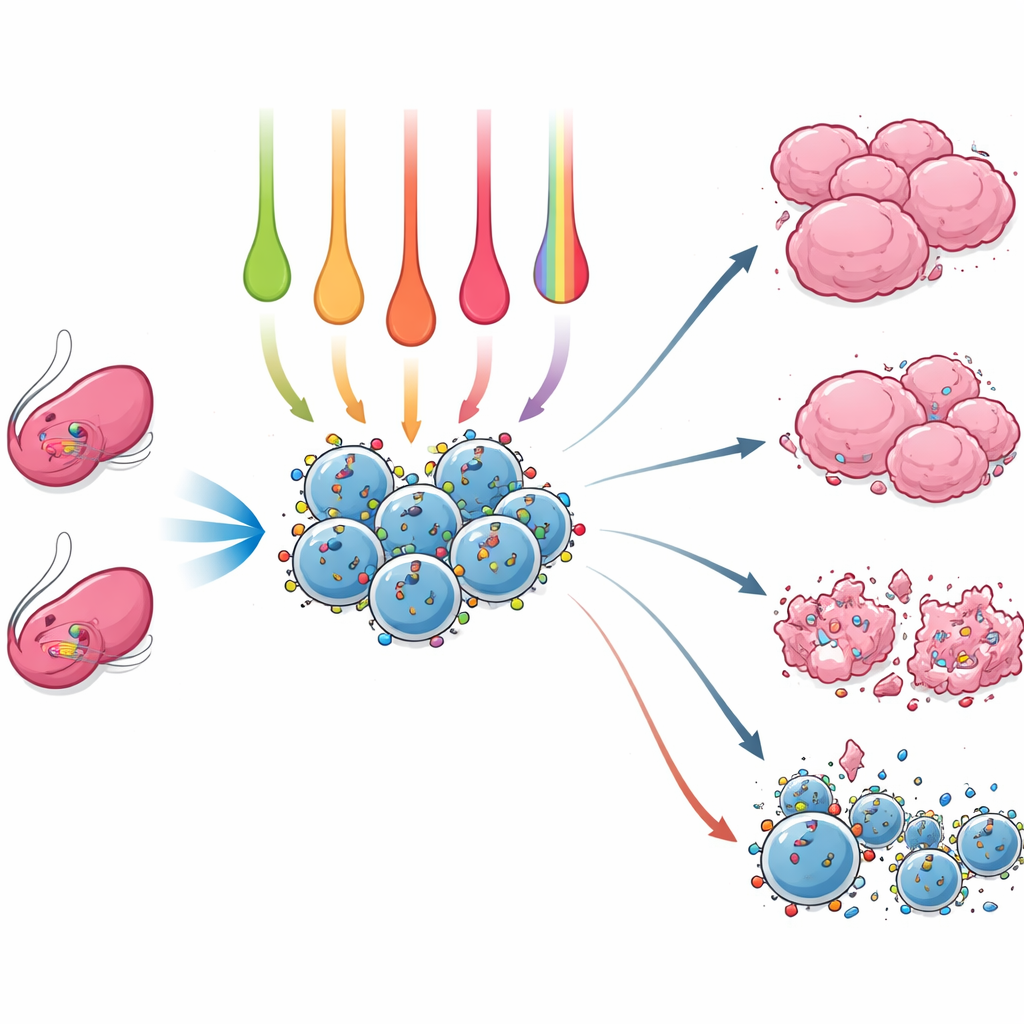
Qué hace que las NK sean más potentes
Las distintas recetas de activación produjeron perfiles de NK notablemente distintos. IL-15 sola proporcionó la mayor supervivencia a corto plazo y buenos niveles de receptores activadores y de granzima B, lo que la convierte en un potente estimulador general. Añadir IL-12 a IL-15 incrementó además la producción de ciertas moléculas señalizadoras, como IFN-gamma y CCL3, que ayudan a coordinar ataques inmunitarios más amplios. Pero los cambios más dramáticos provinieron de la mezcla triple de IL-12, IL-15 e IL-18. Este cóctel transformó a las NK en fábricas potentes de citocinas y quimiocinas proinflamatorias, elevando de forma notable IFN-gamma y otras señales que pueden reclutar y activar células inmunitarias adicionales. Estas NK “tipo memoria” también mostraron niveles más altos del marcador de activación temprana CD69, aunque su supervivencia fue algo menor y su contenido de granzima B no superó al observado con algunos tratamientos más simples.
Del plato de cultivo al control tumoral
Cuando estas NK preparadas de forma distinta se pusieron en contacto con células tumorales, todos los grupos activados pudieron limitar el crecimiento tumoral e inducir la muerte de las células cancerosas, tanto si las dianas portaban marcadores propios normales como si los habían perdido. El cóctel triple de citocinas y la pareja IL-12/IL-15 tendieron a producir daños visibles más intensos en las capas de células tumorales y una proliferación tumoral más lenta, especialmente frente a células de melanoma que carecían de marcadores propios. En contraste, la exposición prolongada al agonista de STING cGAMP por sí sola fue perjudicial para las NK, reduciendo drásticamente su supervivencia y atenuando sus marcadores funcionales, lo que sugiere que este tipo de estímulo debe administrarse con cuidado en el tiempo o combinarse con citocinas protectoras como IL-15.
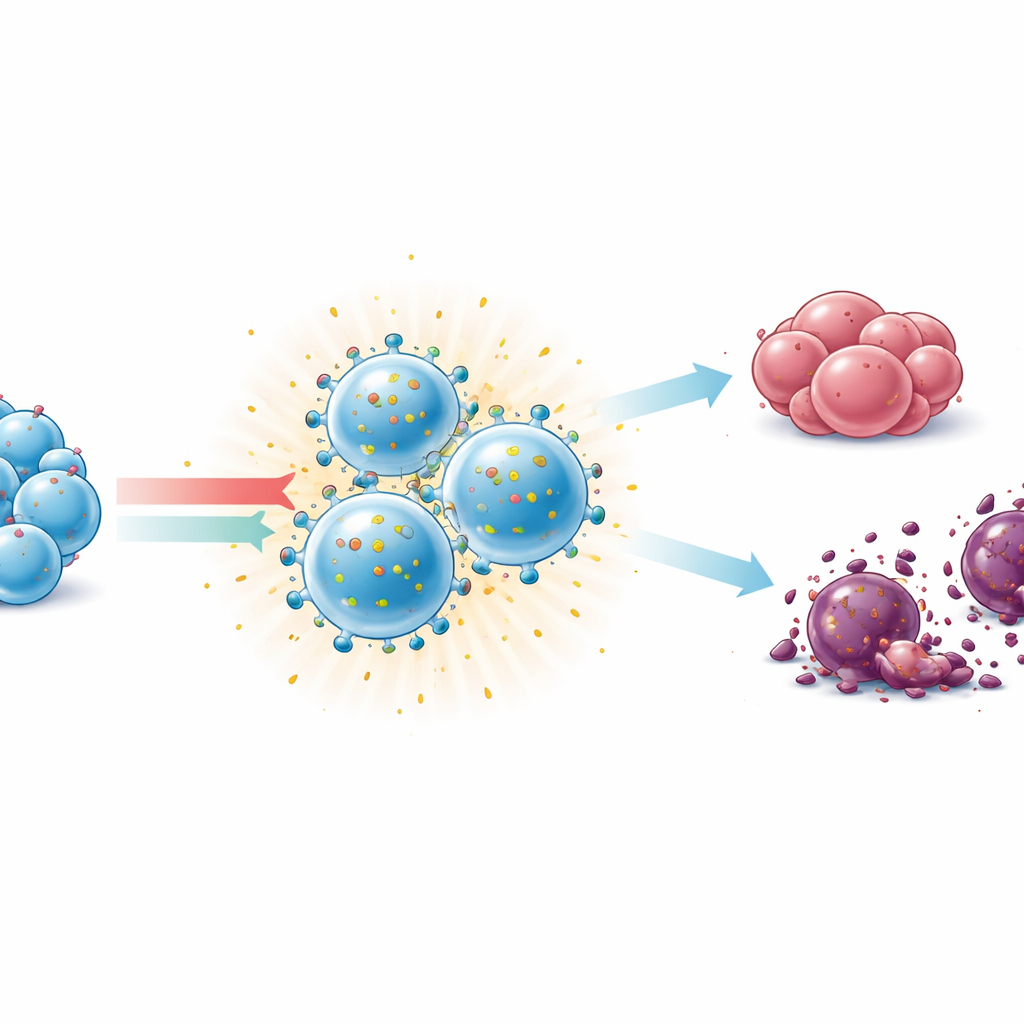
Qué significa esto para la atención oncológica futura
En conjunto, los hallazgos subrayan que no todas las señales que potencian el sistema inmunitario son iguales. IL-15 destaca como una vía fiable para mantener vivas y preparadas a las NK, mientras que la combinación IL-12/IL-15/IL-18 genera células NK altamente activadas y tipo memoria que liberan potentes señales inflamatorias y pueden frenar el crecimiento de células tumorales “visibles” y “ocultas” en el laboratorio. Aunque estos experimentos se realizaron en ratones y en placas de cultivo más que en pacientes, apoyan el uso del cóctel IL-12/IL-15/IL-18 para preparar NK destinadas a la terapia celular adoptiva. En términos prácticos, este trabajo ayuda a refinar la receta para cultivar NK más inteligentes y resistentes que quizá algún día permitan a los médicos contar con una forma más segura y eficaz de reclutar al sistema inmunitario contra el cáncer.
Cita: Czapla, J., Drzyzga, A. & Smolarczyk, R. Characteristics of NK cells activation following IL-12, IL-15, IL-18 cytokines stimulation for preclinical purposes. Sci Rep 16, 13665 (2026). https://doi.org/10.1038/s41598-026-42816-1
Palabras clave: células asesinas naturales, terapia con citocinas, inmunoterapia contra el cáncer, células NK con memoria, terapia celular adoptiva