Clear Sky Science · de
Charakteristika der Aktivierung von NK‑Zellen nach Stimulation mit den Zytokinen IL‑12, IL‑15, IL‑18 für präklinische Zwecke
Warum es wichtig ist, Immunzellen zu stärken
Krebstherapien versuchen zunehmend, dem Körper zu helfen, sich selbst zu heilen, indem sie seine eigenen Abwehrkräfte stärken. Unter unseren Immunwächtern heben sich natürliche Killerzellen (NK‑Zellen) hervor, weil sie schnell auffällige und abnorme Zellen — einschließlich vieler Krebszellen — erkennen und zerstören können. Frisch aus dem Körper entnommene NK‑Zellen sind jedoch oft träge. Diese Studie stellt eine praktische Frage für künftige Krebstherapien: Welche "Immunwachstumsfaktoren" wecken NK‑Zellen im Labor am besten auf, sodass sie kraftvoll, sicher und bereit sind, Tumore anzugreifen, wenn sie den Patienten zurückgegeben werden?
Wie die Ersthelfer des Körpers arbeiten
NK‑Zellen gehören zum angeborenen Immunsystem und wirken als schnelle Eingreiftruppe gegen virusinfizierte und entartete Zellen. Sie töten, indem sie toxische Pakete freisetzen, und senden Gefahrsignale aus, die andere Immunzellen mobilisieren. Ihr Verhalten hängt stark von chemischen Botenstoffen ab, den Zytokinen, die sie entweder in Aktion versetzen oder dämpfen können. Kliniker und Forscher nutzen bereits einige dieser Zytokine, etwa IL‑2 und IL‑15, um NK‑Zellen außerhalb des Körpers zu vermehren, doch diese Substanzen können Nebenwirkungen verursachen oder NK‑Zellen erschöpfen, wenn sie falsch eingesetzt werden. Neuere Kombinationen, insbesondere das Trio IL‑12, IL‑15 und IL‑18, wurden vorgeschlagen, um langlebigere, „memory‑artige“ NK‑Zellen zu erzeugen, die bei Kontakt mit Krebs kraftvoller reagieren.
Vergleich verschiedener immunstimulierender Rezepte
Um diese Ansätze direkt zu vergleichen, isolierten die Forscher NK‑Zellen aus der Milz zweier gängiger Labormauslinien. Sie setzten die Zellen für 24 Stunden verschiedenen einzelnen Zytokinen, Paaren sowie dem Cocktail aus IL‑12/IL‑15/IL‑18 aus und testeten außerdem einen STING‑Weg‑Aktivator namens cGAMP, der bekannt dafür ist, Immunantworten zu stimulieren. Gemessen wurde, wie viele NK‑Zellen überlebten, welche Aktivierungs‑ und Hemmschalter auf ihrer Oberfläche erschienen, wie viel des Tötungsenzyms Granzyme B sie enthielten und welche entzündlichen Signale sie produzierten. Schließlich kultivierten sie diese NK‑Zellen gemeinsam mit zwei Typen von Mauskrebszellen: einer, die normale Selbsterkennungsmarker (MHC‑positiv) zeigt, und einer, die diese Marker verloren hat (MHC‑negativ), ein häufiger Trick von Tumoren, um anderen Immunzellen zu entgehen.
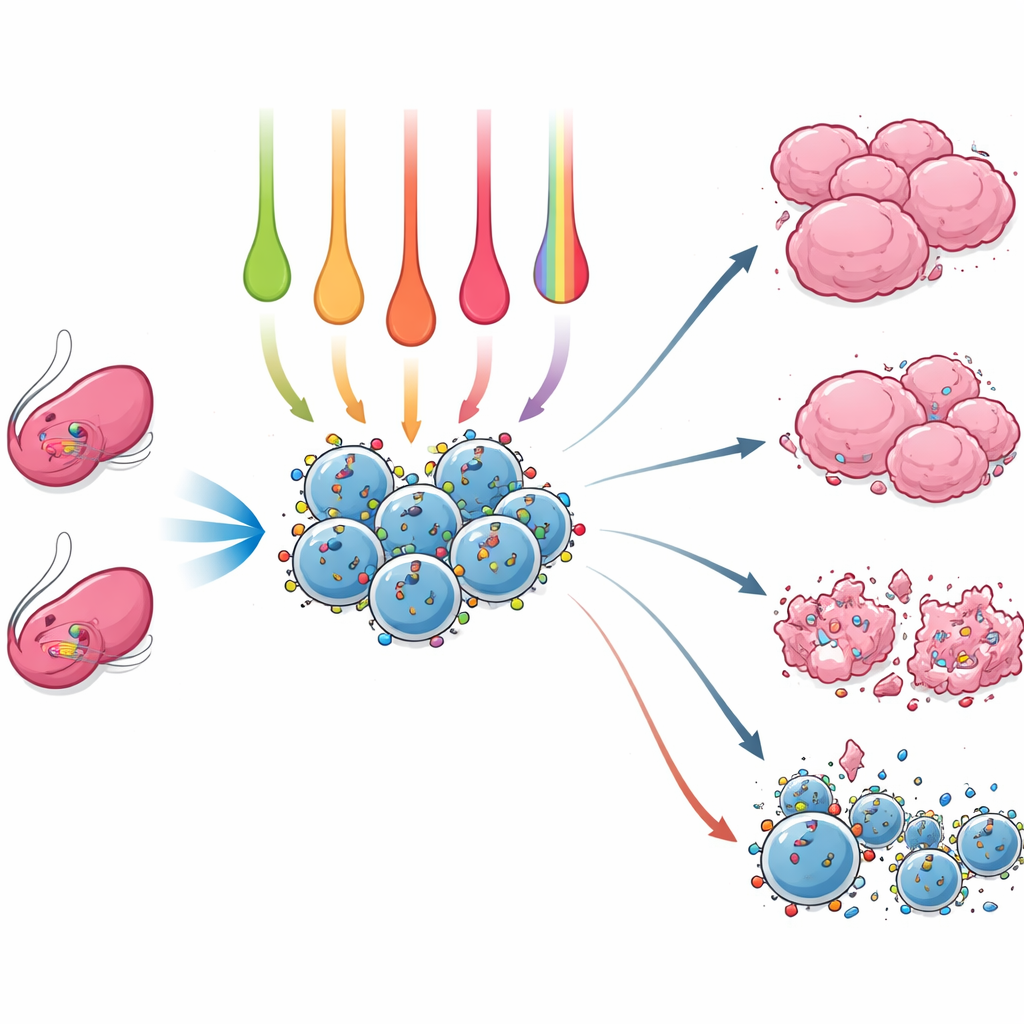
Was NK‑Zellen am stärksten macht
Verschiedene Aktivierungsrezepte erzeugten deutlich unterschiedliche NK‑Zell‑Profile. IL‑15 allein gab das höchste kurzfristige Überleben sowie gute Werte an aktivierenden Rezeptoren und Granzyme B und erwies sich damit als starker allgemeiner Booster. Das Hinzufügen von IL‑12 zu IL‑15 steigerte weiter die Produktion bestimmter Signalmoleküle wie IFN‑gamma und CCL3, die helfen, breitere Immunangriffe zu koordinieren. Die dramatischsten Veränderungen zeigte jedoch die Dreifachmischung aus IL‑12, IL‑15 und IL‑18. Dieser Cocktail verwandelte NK‑Zellen in potente Fabriken proinflammatorischer Zytokine und Chemokine und erhöhte IFN‑gamma sowie andere Signale deutlich, die zusätzliche Immunzellen anlocken und aktivieren können. Diese „memory‑artigen“ NK‑Zellen zeigten außerdem höhere Werte des frühen Aktivierungsmarkers CD69, obwohl ihr Überleben etwas geringer war und ihr Granzyme‑B‑Gehalt nicht über dem einiger einfacherer Behandlungen lag.
Vom Reagenzglas zur Tumorkontrolle
Wurden diese unterschiedlich vorbereiteten NK‑Zellen mit Krebszellen zusammengebracht, konnten alle aktivierten Gruppen das Tumorwachstum begrenzen und den Zelltod auslösen — sowohl gegen Zielzellen mit normalen Selbsterkennungsmarkern als auch gegen solche ohne diese Marker. Der Dreifach‑Zytokin‑Cocktail und das Paar IL‑12/IL‑15 erzeugten tendenziell stärkere sichtbare Schäden an Krebszellschichten und verlangsamten die Tumorzellproliferation, insbesondere gegen Melanomzellen ohne Selbsterkennungsmarker. Im Gegensatz dazu war eine längere Exposition gegenüber dem STING‑Agonisten cGAMP allein schädlich für NK‑Zellen: Sie reduzierte deren Überleben stark und dämpfte funktionelle Marker, was darauf hindeutet, dass dieser Stimulus sorgfältig zeitlich abgestimmt oder mit schützenden Zytokinen wie IL‑15 kombiniert werden muss.
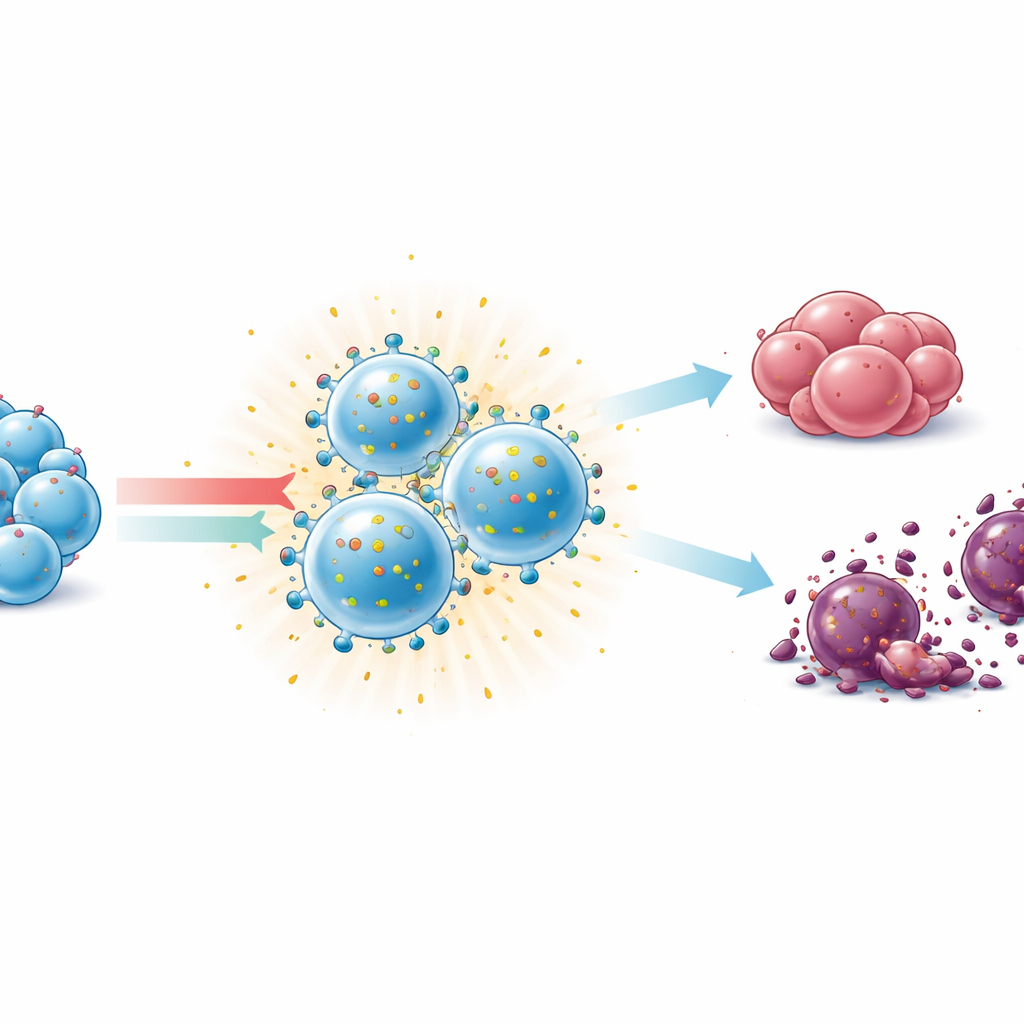
Was das für die künftige Krebsversorgung bedeutet
In der Summe heben die Ergebnisse hervor, dass nicht alle immunstimulierenden Signale gleichwertig sind. IL‑15 sticht als verlässliche Methode hervor, NK‑Zellen am Leben und vorbereitet zu halten, während die Kombination IL‑12/IL‑15/IL‑18 hochaktivierte, memory‑artige NK‑Zellen erzeugt, die starke entzündliche Signale freisetzen und das Wachstum sowohl „sichtbarer“ als auch „versteckter“ Tumorzellen im Labor eindämmen können. Obwohl diese Experimente an Mäusen und in Zellkulturen und nicht an Patienten durchgeführt wurden, unterstützen sie den Einsatz des IL‑12/IL‑15/IL‑18‑Cocktails zur Vorbereitung von NK‑Zellen für die adoptive Zelltherapie. Praktisch hilft diese Arbeit, das Rezept zur Züchtung klügerer, widerstandsfähigerer NK‑Zellen zu verfeinern, die Ärzten eines Tages eine sicherere und effektivere Möglichkeit bieten könnten, das Immunsystem gegen Krebs einzusetzen.
Zitation: Czapla, J., Drzyzga, A. & Smolarczyk, R. Characteristics of NK cells activation following IL-12, IL-15, IL-18 cytokines stimulation for preclinical purposes. Sci Rep 16, 13665 (2026). https://doi.org/10.1038/s41598-026-42816-1
Schlüsselwörter: natürliche Killerzellen, Zytokintherapie, Krebsimmuntherapie, memory‑artige NK‑Zellen, adoptive Zelltherapie