Clear Sky Science · sv
Ultra-prestanda vätske-kromatografi–masspektrometrianalys av post-mortem hjärnvävnad avslöjar specifik störning i aminosyraprofil hos patienter med Parkinsons sjukdom och Alzheimers sjukdom
Varför små hjärnkemikalier spelar roll
Parkinsons och Alzheimers sjukdom beskrivs ofta i termer av nervcellsdöd och ansamlingar av felveckade proteiner. Men bakom dessa synliga förändringar finns en subtil kemisk värld av små molekyler som driver och finjusterar hjärnans aktivitet. Denna studie ställer en enkel men viktig fråga: förändras mönstren av dessa små byggstenar, särskilt aminosyror, inuti hjärnan vid Parkinsons sjukdom, och skiljer sig dessa förändringar från vad som sker vid Alzheimers och i resten av kroppen? Svaret kan hjälpa till att förklara symtom, styra läkemedelsutveckling och peka mot mer precisa diagnostiska tester.
Inuti hjärnor efter döden
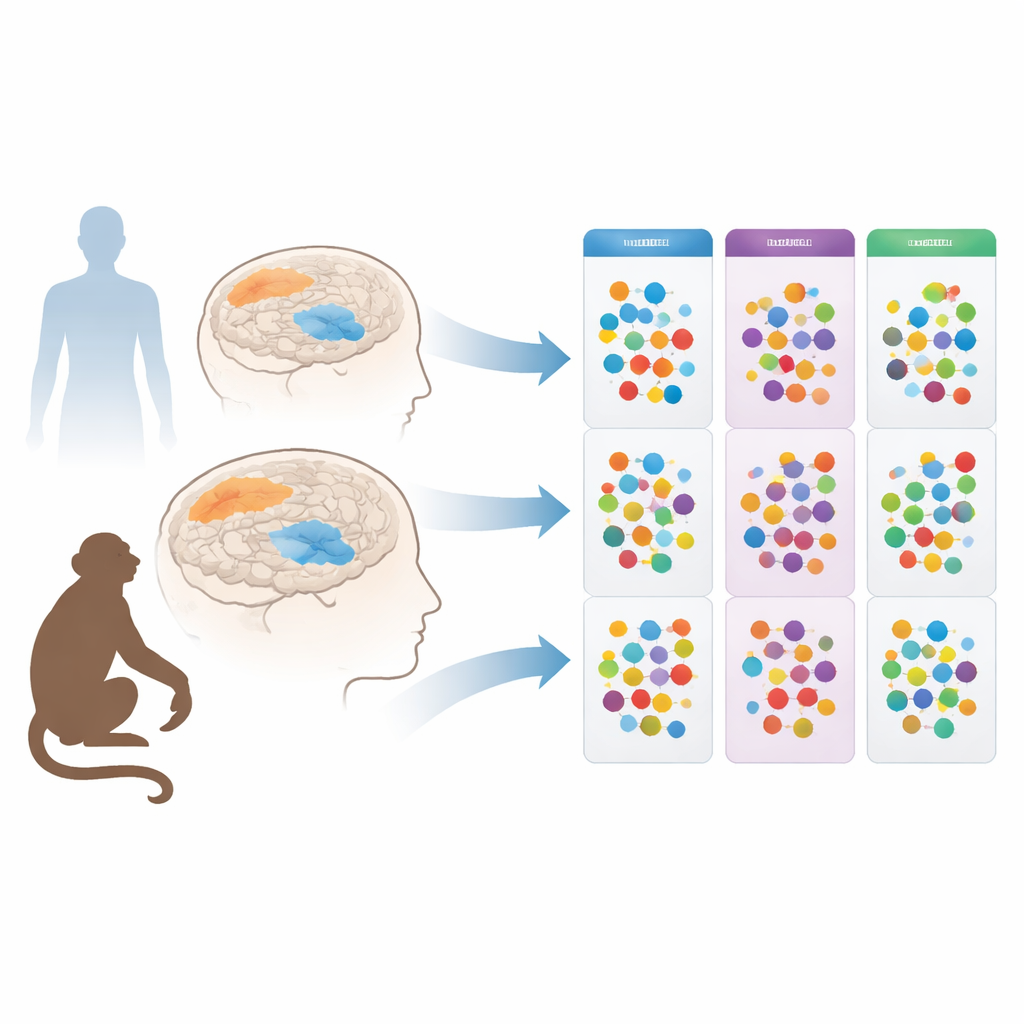
Forskarna fokuserade på aminosyror, de små enheterna som bygger upp proteiner och som också fungerar som budbärare och energihjälpare i hjärnan. Tidigare arbete hade visat att personer med Parkinsons har förändrade aminosyranivåer i blod, ryggmärgsvätska, saliv och urin. Det var dock oklart om dessa skift direkt speglade vad som hände i hjärnan, eller bara var ekon av bredare förändringar i organ som levern och njurarna. För att få en klarare bild vände sig teamet till post-mortem-prover: de undersökte två hjärnregioner hos personer som avlidit med Parkinsons eller Alzheimers, och hos noggrant matchade kontrollgivare utan neurodegenerativ sjukdom. De studerade också en etablerad makakmodell för Parkinsons, där ett toxin selektivt skadar dopaminproducerande celler, med eller utan långtidsbehandling med standardläkemedlet L-DOPA.
Två hjärnregioner, mycket olika berättelser
Forskarna jämförde en djup rörelserelaterad struktur—caudat‑putamen (eller putamen hos apor)—med en frontal tänkande region kallad superior frontal gyrus. Med en ultrasensitiv teknik (UPLC‑MS) som kan mäta många aminosyror samtidigt med hög precision upptäckte de att förändringarna vid Parkinsons var slående specifika för den djupa rörelseområdet. Hos toxinbehandlade apor visade putamen förhöjda nivåer av flera aminosyror, inklusive glutamat och aspartat (viktiga för excitation), GABA (inhibering), grenade aminosyror, fenylalanin och serin. Tillägg av L‑DOPA förändrade mönstret ytterligare genom att öka andra molekyler såsom glycin, treonin och citrullin. I frontal cortex hos samma djur var aminosyranivåerna i stort sett oförändrade, även efter månader av dopaminförlust och behandling.
Parkinsons kontra Alzheimers i människans hjärna
Mänskliga prover berättade en kompletterande historia. I caudat‑putamen hos Parkinsonpatienter var endast en liten delmängd av aminosyror konsekvent påverkade. Genom alla stadier av sjukdomsspridning (Braak Lewy body-stadier) var nivåerna av serin förhöjda; i det mest avancerade stadiet var också prolin högre, medan fosfoetanolamin var lägre, och arginin tenderade att sjunka jämfört med tidigare stadier. Dessa förändringar tyder på att när Parkinsons fortskrider blir vissa kemiska vägar—kopplade till energianvändning, antioxidantförsvar och signalering—alltmer obalanserade. Viktigt är att superior frontal gyrus hos Parkinsonpatienter i detta avseende såg i stort sett normal ut, vilket speglar fynden hos aporna och understryker att den metaboliska störningen är koncentrerad till rörelse-cirkuiterna. I kontrast visade personer med Alzheimers sjukdom motsatt mönster i samma frontala region: flera aminosyror, inklusive tryptofan, fenylalanin, treonin, tyrosin och metionin, var tydligt förhöjda, vilket pekar på en kortikal‑centrerad störning som skiljer sig från den som ses vid Parkinsons.
Den särskilda rollen för en aminosyra
Bland alla undersökta molekyler över djur, hjärnregioner och sjukdomsstadier utmärkte sig serin. Det var konsekvent högre i det skadade rörelseområdet hos toxinbehandlade apor och hos personer med Parkinsons, och tidigare arbete av samma grupp har funnit förhöjt serin i ryggmärgsvätska och blod hos patienter också. Serin finns i två spegelvända former som tillsammans stödjer både hjärnsignalering och cellernas underhåll: en form hjälper till att aktivera en nyckel glutamatreceptor som är involverad i inlärning och kommunikation mellan neuroner, medan den andra bidrar till produktionen av membrankomponenter, nukleotider och antioxidanter. Den upprepade ökningen av serin i flera experiment antyder att hjärnan kan försöka anpassa sig till dopaminförlust genom att stärka vissa kretsar och skyddande vägar, även när sjukdomen fortskrider.
Vad detta betyder för patienter och framtida tester
Tillsammans visar resultaten att förändringar i små hjärnkemikalier inte är slumpmässiga, utan följer tydliga mönster kopplade både till hjärnregion och sjukdomstyp. Vid Parkinsons klustras aminosyraförändringar i de dopaminberoende rörelsekretsarna och är relativt begränsade i omfattning, med serin som framträder som en pålitlig markör för störning; vid Alzheimers är aminosyraförändringarna mer framträdande i frontala cortex. Detta tyder på att metabola fingeravtryck i blod delvis speglar, men inte fullt ut fångar, vad som händer i hjärnan. För en lekmannaläsare är huvuddragen att övervaka specifika aminosyror—särskilt serin—en dag kunna hjälpa till att förfina diagnos, följa Parkinsons utveckling och utvärdera om nya behandlingar återställer en hälsosammare hjärnkemistri, samtidigt som man skiljer Parkinsons från andra former av demens.
Citering: Gervasoni, J., Di Maio, A., Serra, M. et al. Ultra-performance liquid chromatography–mass spectrometry analysis of post-mortem brain tissue reveals specific amino acid profile dysregulation in Parkinson’s disease and Alzheimer’s disease patients. npj Parkinsons Dis. 12, 95 (2026). https://doi.org/10.1038/s41531-026-01306-x
Nyckelord: Parkinsons sjukdom, aminosyror, serin, hjärnans ämnesomsättning, Alzheimers sjukdom