Clear Sky Science · ar
تحليل باستخدام الكروماتوغرافيا السائلة فائقة الأداء–مطيافية الكتلة لأنسجة الدماغ ما بعد الوفاة يكشف عن اضطراب ملف أمين حمضي محدد في مرضي باركنسون ومرضى الزهايمر
لماذا تهم المواد الكيميائية الصغيرة في الدماغ
عادةً ما يُوصف مرضا باركنسون والزهايمر بمصطلحات موت الخلايا العصبية وتراكم كتل من البروتينات المشوهة. لكن وراء هذه التغيرات الظاهرة يكمن عالم كيميائي دقيق من الجزيئات الصغيرة التي تغذي وتنظّم نشاط الدماغ. تطرح هذه الدراسة سؤالاً بسيطاً لكنه مهمّاً: هل تتغير أنماط هذه اللبنات الصغيرة، وخصوصاً الأحماض الأمينية، داخل الدماغ نفسه في مرض باركنسون، وهل تختلف تلك التغيرات عما يحدث في مرض الزهايمر وفي بقية أنحاء الجسم؟ قد يساعد الجواب في تفسير الأعراض، وتوجيه تطوير الأدوية، والإشارة إلى اختبارات تشخيصية أكثر دقة.
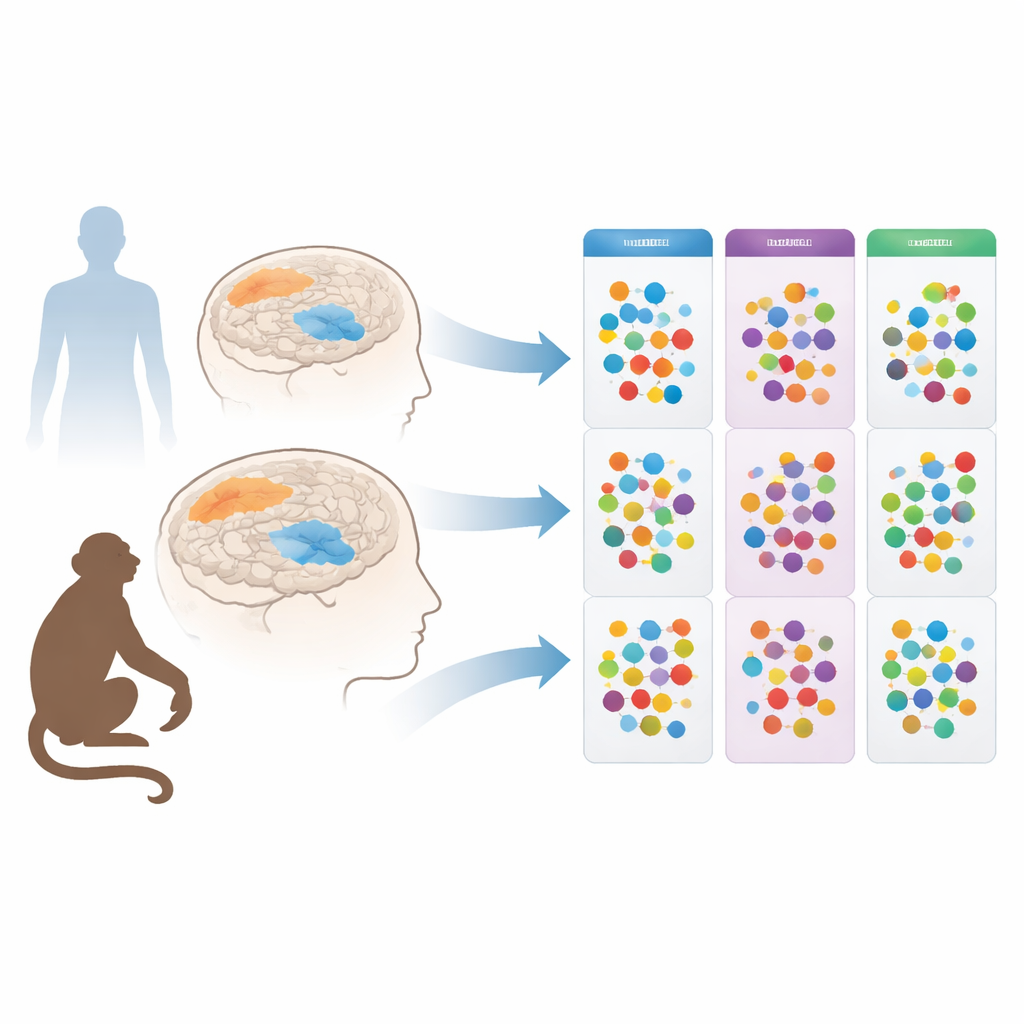
إلقاء نظرة داخل الأدمغة بعد الوفاة
ركّز الباحثون على الأحماض الأمينية، الوحدات الصغيرة التي تبني البروتينات وتعمل أيضاً كرسل ومساعدين للطاقة في الدماغ. أظهرت أعمال سابقة أن مستويات الأحماض الأمينية لدى مرضى باركنسون تختلف في الدم والسائل النخاعي واللعاب والبول. ومع ذلك، لم يتضح ما إذا كانت هذه التحولات تعكس مباشرة ما يحدث في الدماغ، أم أنها مجرد صدى لتغيرات أوسع في أعضاء مثل الكبد والكليتين. للحصول على صورة أوضح، لجأ الفريق إلى عينات ما بعد الوفاة: فحصوا منطقتين دماغيتين لدى أشخاص توفوا مع باركنسون أو الزهايمر، وفي متبرعين مراقبين بعناية دون أمراض تنكسية عصبية. كما درسوا نموذج قردي راسخ لباركنسون، حيث يتسبب سمّ بشكل انتقائي في تلف الخلايا المنتجة للدوبامين، مع أو بدون علاج طويل الأمد بالدواء القياسي إل‑دوبا.
منطقتان دماغيتان وقصتان مختلفتان جداً
قارن العلماء بنية عميقة مرتبطة بالحركة — المذيل‑المخفظ (أو المخفظ في القردة) — مع منطقة أمامية مرتبطة بالتفكير تُسمى التلافيف الجبهية العلوية. باستخدام تقنية فائقة الحساسية (UPLC‑MS) التي تقيس بدقة عشرات الأحماض الأمينية دفعة واحدة، اكتشفوا أن التغيرات في باركنسون كانت محددة للغاية في منطقة الحركة العميقة. في القرود المعالجة بالسم، أظهر المخفظ مستويات أعلى لعدة أحماض أمينية، بما في ذلك الغلوتامات والأسبارتات (المهمة في الإثارة)، الجابا (التثبيط)، الأحماض الأمينية متفرعة السلسلة، الفينيل ألانين، والسيرين. أضافت معالجة إل‑دوبا تغييرات أخرى، مع ارتفاع جزيئات مثل الجليسين والثريونين والسترتولين. ومع ذلك، في قشرة الفص الجبهي لتلك الحيوانات نفسها، كانت مستويات الأحماض الأمينية شبه ثابتة، حتى بعد شهور من فقدان الدوبامين والعلاج.
باركنسون مقابل الزهايمر في دماغ الإنسان
قدمت عينات البشر قصة متممة. في المذيل‑المخفظ لمرضى باركنسون، تغيّرت مجموعة صغيرة فقط من الأحماض الأمينية بشكل متكرر. عبر جميع مراحل انتشار المرض (مراحل برايك لحبيبات ليوي)، كانت مستويات السيرين مرتفعة؛ وفي أقدم المراحل، ارتفعت مستويات البروتين أيضاً، بينما انخفضت الفسفوإيثانولامين، وميّل الأرجينين إلى الانخفاض مقارنة بالمراحل السابقة. تشير هذه التحولات إلى أنه مع تقدم باركنسون، تصبح مسارات كيميائية معينة — المرتبطة باستخدام الطاقة والدفاعات المضادة للأكسدة والإشارة — أقل توازناً. بشكل مهم، بدا تلافيف القشرة الجبهية العلوية لدى مرضى باركنسون طبيعية في هذا الصدد، ما يواكب نتائج القردة ويؤكد أن الاضطراب الأيضي يتركز في دوائر الحركة. بالمقابل، أظهر مرضى الزهايمر نمطاً معاكساً في نفس المنطقة الجبهية: ارتفعت بوضوح عدة أحماض أمينية، بما في ذلك التربتوفان والفينيل ألانين والثريونين والتيروزين والميثيونين، مما يشير إلى اضطراب متركز قشري مختلف عن ذلك الذي يُرى في باركنسون.
الدور الخاص لحمض أميني واحد
من بين جميع الجزيئات المبحوثة عبر الحيوانات والمناطق الدماغية ومراحل المرض، برز السيرين. كان مرتفعاً باستمرار في منطقة الحركة المتضررة لدى القرود المعالجة بالسم ولدى مرضى باركنسون، وقد وجدت أعمال سابقة لنفس الفريق ارتفاع السيرين أيضاً في السائل النخاعي والدم للمرضى. للسيرين شكلان مرآتيان يدعمان معاً كل من الإشارة الدماغية وصيانة الخلايا: يساهم أحدهما في تنشيط مستقبل غلوتامات رئيسي مشارك في التعلم والتواصل بين الخلايا العصبية، بينما يدخل الآخر في تصنيع مكونات الأغشية والنوكليوتيدات ومضادات الأكسدة. التكرر المستمر لارتفاع السيرين عبر التجارب يقترح أن الدماغ قد يحاول التكيّف مع فقدان الدوبامين بتقوية دوائر ومسارات حماية معينة، حتى مع تقدم المرض.
ماذا يعني هذا للمرضى والاختبارات المستقبلية
تبين النتائج مجتمعة أن تغيّرات المواد الكيميائية الصغيرة في الدماغ ليست عشوائية، بل تتبع أنماطاً واضحة مرتبطة بمنطقة الدماغ ونوع المرض. في باركنسون، تتجمع تحولات الأحماض الأمينية في دوائر الحركة المعتمدة على الدوبامين وتكون محدودة نسبياً في النطاق، مع بروز السيرين كعلامة موثوقة للاضطراب؛ أما في الزهايمر، فالتغيرات الأحماض الأمينية أكثر وضوحاً في القشرة الجبهية. هذا يوحي بأن بصمات الأيض القائمة على الدم قد تعكس جزئياً، لكنها لا تلتقط بالكامل، ما يحدث داخل الدماغ. للخلاصة العامة للقارئ العادي: مراقبة أحماض أمينية محددة — وخصوصاً السيرين — قد يساعد في المستقبل على تحسين التشخيص، وتتبع تقدم باركنسون، وتقييم ما إذا كانت العلاجات الجديدة تعيد توازن كيمياء الدماغ، مع التمييز بين باركنسون وأشكال أخرى من الخرف.
الاستشهاد: Gervasoni, J., Di Maio, A., Serra, M. et al. Ultra-performance liquid chromatography–mass spectrometry analysis of post-mortem brain tissue reveals specific amino acid profile dysregulation in Parkinson’s disease and Alzheimer’s disease patients. npj Parkinsons Dis. 12, 95 (2026). https://doi.org/10.1038/s41531-026-01306-x
الكلمات المفتاحية: مرض باركنسون, الأحماض الأمينية, السيرين, تمثيل الدماغ الغذائي, مرض الزهايمر