Clear Sky Science · it
Cromatografia liquida ad alte prestazioni accoppiata a spettrometria di massa per l’analisi di tessuto cerebrale post‑mortem rivela una disregolazione specifica del profilo degli amminoacidi nei pazienti con malattia di Parkinson e malattia di Alzheimer
Perché sono importanti le piccole molecole del cervello
La malattia di Parkinson e la malattia di Alzheimer vengono di solito descritte in termini di morte dei neuroni e di aggregati di proteine mal ripiegate. Ma dietro questi cambiamenti visibili esiste un mondo chimico sottile fatto di piccole molecole che alimentano e regolano finemente l’attività cerebrale. Questo studio pone una domanda semplice ma importante: i modelli di questi piccoli mattoni, in particolare gli amminoacidi, cambiano all’interno stesso del cervello nella malattia di Parkinson, e tali cambiamenti sono differenti rispetto a quanto avviene nella malattia di Alzheimer e nel resto del corpo? La risposta potrebbe aiutare a spiegare i sintomi, guidare lo sviluppo di farmaci e indicare test diagnostici più precisi.
Osservare i cervelli dopo la morte
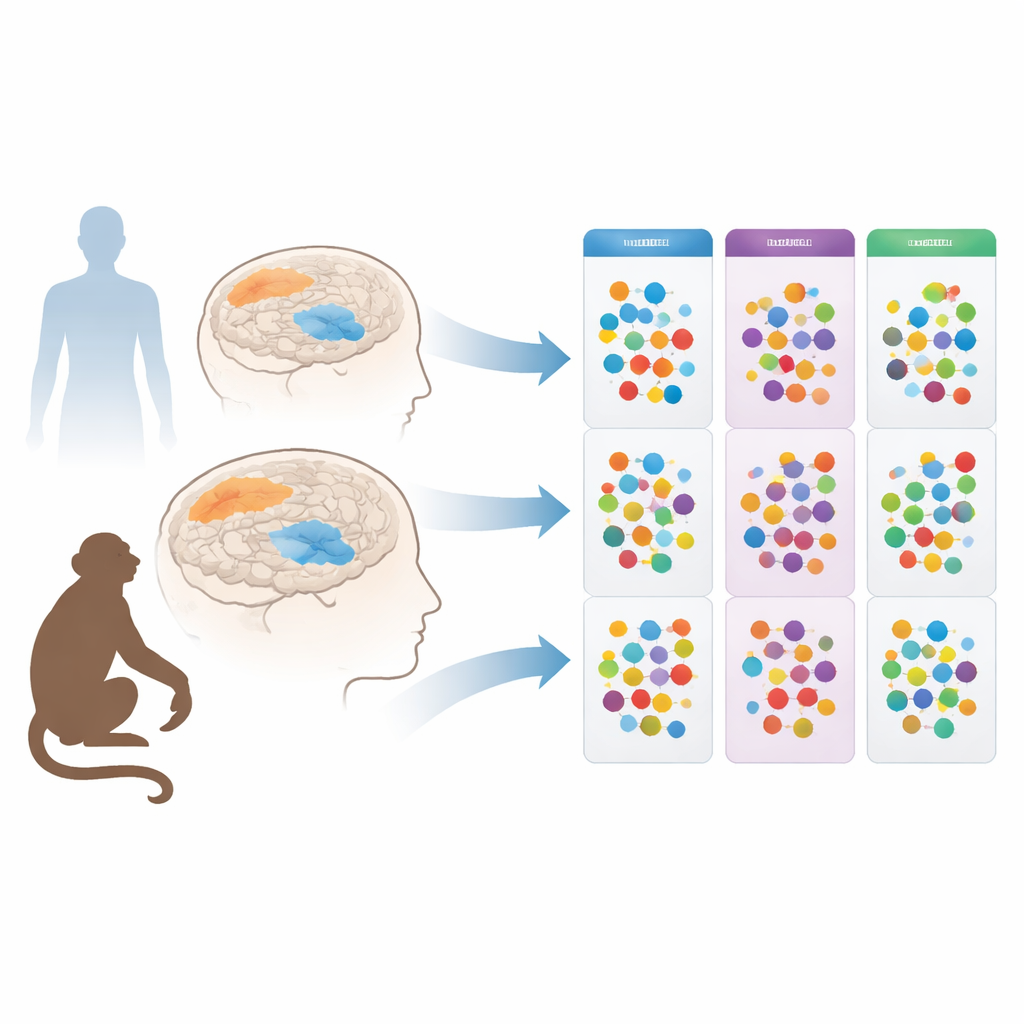
I ricercatori si sono concentrati sugli amminoacidi, le piccole unità che costituiscono le proteine e che fungono anche da messaggeri e coadiuvanti energetici nel cervello. Lavori precedenti avevano mostrato che le persone con Parkinson presentano livelli alterati di amminoacidi in sangue, liquido cerebrospinale, saliva e urine. Tuttavia, non era chiaro se questi spostamenti riflettessero direttamente ciò che accade nel cervello, o fossero semplici echi di cambiamenti più ampi in organi come fegato e reni. Per ottenere un quadro più chiaro, il gruppo ha utilizzato campioni post‑mortem: ha esaminato due regioni cerebrali in soggetti deceduti con Parkinson o Alzheimer e in donatori di controllo accuratamente appaiati senza malattie neurodegenerative. Hanno anche studiato un modello di Parkinson consolidato nel macaco, in cui una tossina danneggia selettivamente le cellule produttrici di dopamina, con o senza trattamento a lungo termine con il farmaco standard L‑DOPA.
Due regioni cerebrali, storie molto diverse
Gli scienziati hanno confrontato una struttura profonda legata al movimento — il caudato‑putamen (o putamen nei macachi) — con una regione frontale implicata nel pensiero, il giro frontale superiore. Utilizzando una tecnica ultra‑sensibile (UPLC‑MS) in grado di misurare con precisione decine di amminoacidi contemporaneamente, hanno scoperto che i cambiamenti nel Parkinson erano sorprendentemente specifici per l’area profonda legata al movimento. Nei macachi trattati con la tossina, il putamen mostrava livelli più elevati di diversi amminoacidi, tra cui glutammato e aspartato (importanti per l’eccitazione), GABA (inibizione), gli amminoacidi a catena ramificata, fenilalanina e serina. L’aggiunta di L‑DOPA ha spostato ulteriormente il profilo, aumentando altre molecole come glicina, treonina e citrullina. Tuttavia, nella corteccia frontale degli stessi animali i livelli di amminoacidi erano essenzialmente invariati, anche dopo mesi di perdita dopaminergica e trattamento.
Parkinson rispetto ad Alzheimer nel cervello umano
I campioni umani hanno raccontato una storia complementare. Nel caudato‑putamen dei pazienti con Parkinson, solo un piccolo sottoinsieme di amminoacidi risultava costantemente alterato. In tutti gli stadi di diffusione della malattia (stadi di Braak delle corpi di Lewy), i livelli di serina erano aumentati; nello stadio più avanzato, la prolina risultava anch’essa più elevata, mentre la fosfoetanolamina era più bassa e l’arginina tendeva a diminuire rispetto agli stadi precedenti. Questi spostamenti suggeriscono che, con il progredire del Parkinson, alcuni percorsi chimici — legati all’uso di energia, alle difese antiossidanti e alla segnalazione — diventano sempre più squilibrati. È importante che il giro frontale superiore dei pazienti con Parkinson apparisse sostanzialmente normale sotto questo aspetto, rispecchiando i riscontri nei macachi e sottolineando che la perturbazione metabolica è concentrata nei circuiti del movimento. Al contrario, le persone con malattia di Alzheimer mostravano il modello opposto nella stessa regione frontale: diversi amminoacidi, tra cui triptofano, fenilalanina, treonina, tirosina e metionina, erano chiaramente aumentati, indicando un disturbo corticale distinto da quello osservato nel Parkinson.
Il ruolo particolare di un amminoacido
Tra tutte le molecole esaminate attraverso animali, regioni cerebrali e stadi della malattia, la serina è emersa in modo netto. Risultava costantemente più alta nell’area del movimento danneggiata nei macachi trattati con la tossina e nelle persone con Parkinson, e lavori precedenti dello stesso gruppo avevano rilevato serina elevata anche nel liquido cerebrospinale e nel sangue dei pazienti. La serina esiste in due forme speculari che insieme supportano sia la segnalazione cerebrale sia i processi di manutenzione cellulare: una forma contribuisce ad attivare un recettore chiave del glutammato coinvolto nell’apprendimento e nella comunicazione tra neuroni, mentre l’altra alimenta la produzione di componenti di membrana, nucleotidi e antiossidanti. L’aumento ripetuto della serina attraverso gli esperimenti suggerisce che il cervello potrebbe cercare di adattarsi alla perdita di dopamina rafforzando certi circuiti e percorsi protettivi, anche mentre la malattia avanza.
Cosa significa per i pazienti e per i futuri test
Considerati nel loro insieme, i risultati mostrano che i cambiamenti nelle piccole molecole cerebrali non sono casuali, ma seguono schemi chiari legati sia alla regione cerebrale sia al tipo di malattia. Nel Parkinson, gli spostamenti degli amminoacidi si concentrano nei circuiti del movimento dipendenti dalla dopamina e sono relativamente limitati nella portata, con la serina che emerge come un marcatore affidabile della perturbazione; nell’Alzheimer, le modifiche degli amminoacidi sono più pronunciate nella corteccia frontale. Questo suggerisce che i profili metabolici rilevati nel sangue rispecchiano in parte, ma non catturano completamente, ciò che avviene nel cervello. Per il lettore non specialistico, la conclusione chiave è che monitorare amminoacidi specifici — in particolare la serina — potrebbe un giorno aiutare a perfezionare la diagnosi, a seguire la progressione del Parkinson e a valutare se nuovi trattamenti stanno ripristinando una chimica cerebrale più sana, distinguendo al contempo il Parkinson da altre forme di demenza.
Citazione: Gervasoni, J., Di Maio, A., Serra, M. et al. Ultra-performance liquid chromatography–mass spectrometry analysis of post-mortem brain tissue reveals specific amino acid profile dysregulation in Parkinson’s disease and Alzheimer’s disease patients. npj Parkinsons Dis. 12, 95 (2026). https://doi.org/10.1038/s41531-026-01306-x
Parole chiave: Malattia di Parkinson, amminoacidi, serina, metabolismo cerebrale, Malattia di Alzheimer