Clear Sky Science · es
Análisis mediante cromatografía líquida de ultra‑alto rendimiento acoplada a espectrometría de masas de tejido cerebral post‑mortem revela desregulación específica del perfil de aminoácidos en pacientes con enfermedad de Parkinson y enfermedad de Alzheimer
Por qué importan los químicos diminutos del cerebro
Las enfermedades de Parkinson y Alzheimer suelen describirse en términos de muerte neuronal y de acúmulos de proteínas mal plegadas. Pero tras esos cambios visibles existe un mundo químico sutil de moléculas pequeñas que alimentan y afinan la actividad cerebral. Este estudio plantea una pregunta simple pero importante: ¿cambian los patrones de esos pequeños bloques constructores, en particular los aminoácidos, dentro del propio cerebro en la enfermedad de Parkinson, y son esos cambios distintos de los que ocurren en la enfermedad de Alzheimer y en el resto del cuerpo? La respuesta podría ayudar a explicar los síntomas, orientar el desarrollo de fármacos y señalar pruebas diagnósticas más precisas.
Mirando dentro de cerebros post‑mortem
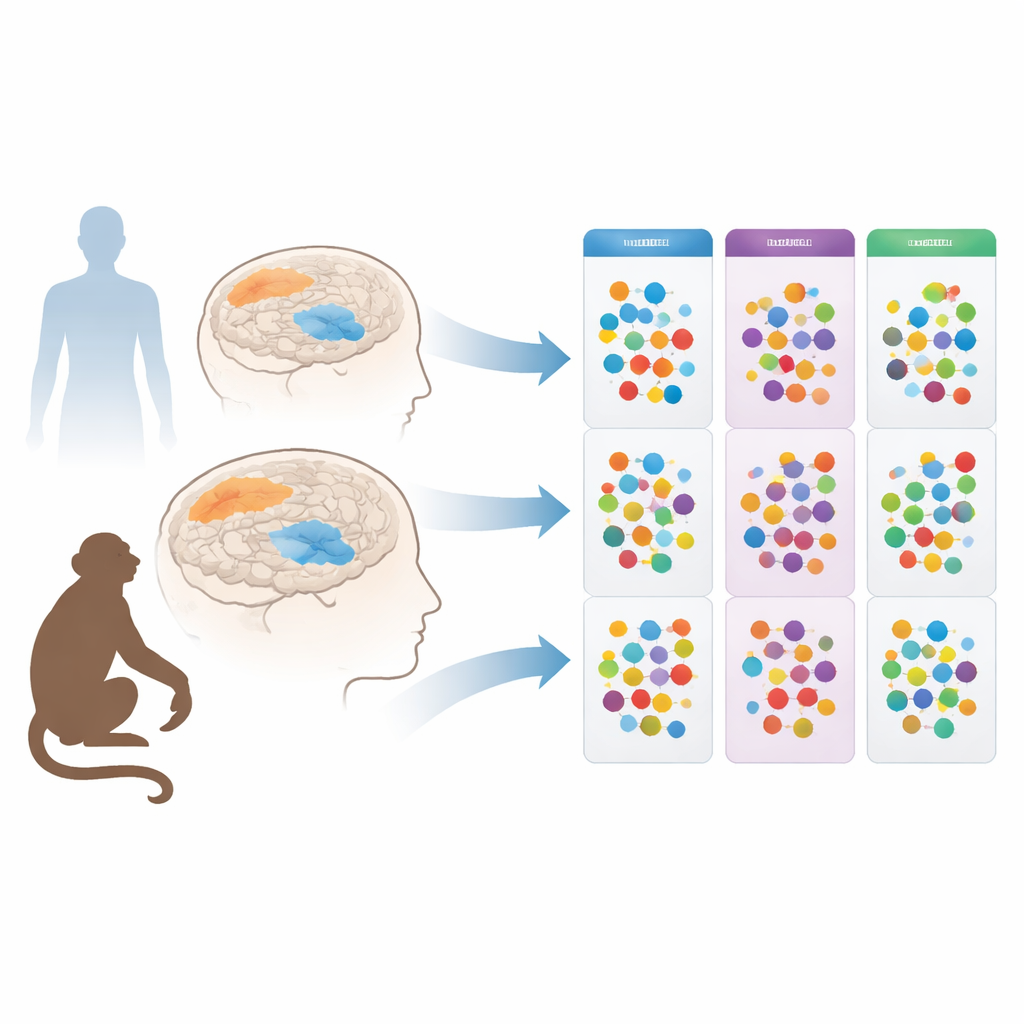
Los investigadores se centraron en los aminoácidos, las pequeñas unidades que forman las proteínas y que también actúan como mensajeros y ayudantes energéticos en el cerebro. Trabajos anteriores habían mostrado que las personas con Parkinson presentan niveles alterados de aminoácidos en sangre, líquido cefalorraquídeo, saliva y orina. Sin embargo, no estaba claro si esos cambios reflejaban directamente lo que ocurría en el cerebro, o si eran meros ecos de alteraciones más generales en órganos como el hígado y los riñones. Para obtener una imagen más clara, el equipo recurrió a muestras post‑mortem: examinaron dos regiones cerebrales de personas que habían fallecido con Parkinson o Alzheimer, y de donantes control cuidadosamente emparejados sin enfermedad neurodegenerativa. También estudiaron un modelo de mono para Parkinson bien establecido, en el que una toxina daña selectivamente las células que producen dopamina, con o sin tratamiento a largo plazo con el fármaco estándar L‑DOPA.
Dos regiones cerebrales, historias muy diferentes
Los científicos compararon una estructura profunda relacionada con el movimiento—el caudado‑putamen (o putamen en monos)—con una región frontal implicada en el pensamiento llamada giro frontal superior. Usando una técnica ultra‑sensible (UPLC‑MS) que puede medir con precisión decenas de aminoácidos a la vez, descubrieron que los cambios en Parkinson eran llamativamente específicos de la zona profunda relacionada con el movimiento. En monos tratados con la toxina, el putamen mostró niveles más altos de varios aminoácidos, incluidos glutamato y aspartato (importantes para la excitación), GABA (inhibición), los aminoácidos de cadena ramificada, fenilalanina y serina. La administración de L‑DOPA desplazó aún más el patrón, aumentando otras moléculas como glicina, treonina y citrulina. Sin embargo, en la corteza frontal de esos mismos animales, los niveles de aminoácidos permanecieron esencialmente sin cambios, incluso después de meses de pérdida de dopamina y tratamiento.
Parkinson frente a Alzheimer en el cerebro humano
Las muestras humanas contaron una historia complementaria. En el caudado‑putamen de pacientes con Parkinson, solo un pequeño subconjunto de aminoácidos se alteró de forma consistente. A lo largo de todas las etapas de propagación de la enfermedad (estadios de Lewy de Braak), los niveles de serina aumentaron; en el estadio más avanzado, la prolina también fue más alta, mientras que la fosfoetanolamina fue menor, y la arginina tendió a disminuir en comparación con estadios anteriores. Estos cambios sugieren que, a medida que progresa el Parkinson, ciertas rutas químicas —vinculadas al uso de energía, defensas antioxidantes y señalización— se desequilibran cada vez más. Es importante destacar que el giro frontal superior de los pacientes con Parkinson se mostró esencialmente normal en este aspecto, reflejando los hallazgos en monos y subrayando que la alteración metabólica se concentra en el circuito del movimiento. En contraste, las personas con enfermedad de Alzheimer mostraron el patrón opuesto en la misma región frontal: varios aminoácidos, incluyendo triptófano, fenilalanina, treonina, tirosina y metionina, se encontraban claramente elevados, lo que apunta a una alteración cortical centrada y distinta de la vista en Parkinson.
El papel especial de un aminoácido
Entre todas las moléculas examinadas a través de animales, regiones cerebrales y estadios de la enfermedad, la serina destacó. Estuvo consistentemente más alta en la zona de movimiento dañada de monos tratados con la toxina y en personas con Parkinson, y trabajos previos del mismo grupo han encontrado serina elevada también en el líquido cefalorraquídeo y la sangre de pacientes. La serina existe en dos formas en espejo que, en conjunto, sostienen tanto la señalización cerebral como las tareas de mantenimiento celular: una forma ayuda a activar un receptor clave de glutamato implicado en el aprendizaje y la comunicación entre neuronas, mientras que la otra se incorpora en la producción de componentes de membrana, nucleótidos y antioxidantes. El aumento repetido de la serina a lo largo de los experimentos sugiere que el cerebro podría estar intentando adaptarse a la pérdida de dopamina fortaleciendo ciertos circuitos y vías protectoras, incluso a medida que la enfermedad avanza.
Qué significa esto para los pacientes y futuras pruebas
Tomados en conjunto, los resultados muestran que los cambios en las pequeñas moléculas cerebrales no son aleatorios, sino que siguen patrones claros ligados tanto a la región cerebral como al tipo de enfermedad. En Parkinson, las alteraciones de aminoácidos se agrupan en los circuitos de movimiento dependientes de dopamina y son relativamente limitadas en alcance, con la serina emergiendo como un marcador fiable de la alteración; en Alzheimer, los cambios de aminoácidos se manifiestan con mayor protagonismo en la corteza frontal. Esto sugiere que las huellas metabólicas basadas en sangre reflejan en parte, pero no capturan completamente, lo que sucede en el cerebro. Para un lector general, la conclusión clave es que monitorizar aminoácidos específicos—especialmente la serina—podría en el futuro ayudar a refinar el diagnóstico, vigilar la progresión del Parkinson y evaluar si nuevos tratamientos restauran una química cerebral más saludable, todo ello diferenciando Parkinson de otras formas de demencia.
Cita: Gervasoni, J., Di Maio, A., Serra, M. et al. Ultra-performance liquid chromatography–mass spectrometry analysis of post-mortem brain tissue reveals specific amino acid profile dysregulation in Parkinson’s disease and Alzheimer’s disease patients. npj Parkinsons Dis. 12, 95 (2026). https://doi.org/10.1038/s41531-026-01306-x
Palabras clave: Enfermedad de Parkinson, aminoácidos, serina, metabolismo cerebral, Enfermedad de Alzheimer