Clear Sky Science · he
ניתוח בחשיפה גבוהה של כרומטוגרפיה נוזלית–ספירת מסה של רקמת מוח לאחר המוות חושף דיסרגולציה ספציפית בפרופיל חומצות אמינו בחולי פרקינסון ובחולי אלצהיימר
מדוע חומרים מוחיים זעירים חשובים
מחלת פרקינסון ואלצהיימר מתוארות בדרך כלל במונחים של מוות תאי עצב והצטברויות של חלבונים מקופלים באופן שגוי. אבל מאחורי השינויים הגלויים האלה נמצא עולם כימי עדין של מולקולות קטנות שמזינות ומעדנות את פעילות המוח. המחקר הזה שואל שאלה פשוטה אך חשובה: האם דפוסי אבני הבניין הקטנות האלה, ובפרט חומצות האמינו, משתנים בתוך המוח עצמו במחלת פרקינסון, והאם שינויים אלה שונים מאלה המתרחשים במחלת אלצהיימר ובשאר הגוף? התשובה עשויה לעזור להסביר תסמינים, לכוון פיתוח תרופות ולהצביע על בדיקות אבחוניות מדויקות יותר.
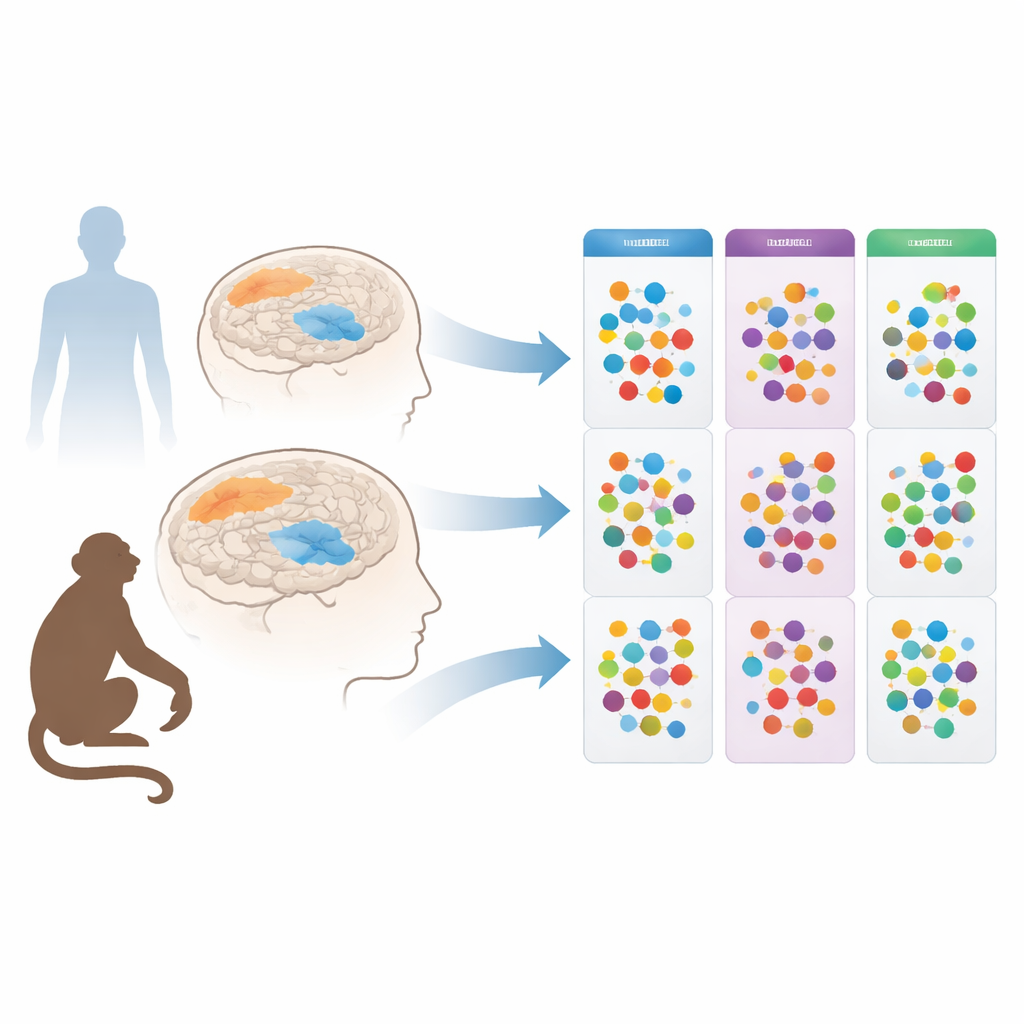
מסתכלים לתוך המוחות אחרי המוות
החוקרים התמקדו בחומצות אמינו, היחידות הזעירות שמרכיבות חלבונים ומשמשות גם כמוליכי אותות וסייעניות אנרגטיות במוח. עבודות קודמות הראו שלאנשים עם פרקינסון יש רמות חומצות אמינו משונות בדם, בנוזל השדרה, ברוק ובשתן. עם זאת, לא היה ברור האם השינויים הללו משקפים ישירות את מה שמתרחש במוח, או שהם רק הד מהשינויים מערכתיים באיברים כגון כבד וכליות. כדי לקבל תמונה ברורה יותר, הצוות פנה לדגימות לאחר המוות: הם בחנו שתי אזורי מוח באנשים שנפטרו עם פרקינסון או אלצהיימר, ובתורמים מבוקרים מותאמים בקפידה ללא מחלה ניוונית. הם גם חקרו מודל קוף מבוסס של פרקינסון, שבו רעלן מפגע בתאי הייצור של דופמין, עם או בלי טיפול ארוך טווח בתרופת הסטנדרט L‑DOPA.
שני אזורי מוח, סיפורים שונים באופן ניכר
המדענים השוו מבנה עמוק הקשור לתנועה—הקאדט‑פוטמן (או הפוטמן בקופים)—עם אזור קדם‑מצחוני הקשור לחשיבה שנקרא הסופריור פרונטל גירוס. באמצעות טכניקה בעלת רגישות גבוהה מאוד (UPLC‑MS) שיכולה למדוד בדיוק עשרות חומצות אמינו בבת אחת, הם גילו כי השינויים בפרקינסון היו ספציפיים באופן בולט לאזור התנועה העמוק. בקופים שטופלו ברעלן, הפוטמן הראה רמות מוגברות של מספר חומצות אמינו, כולל גלוטמט ואספרטט (חשובות להגברה), GABA (עיכוב), חומצות אמינו מסועפות, פנילאלנין וסרין. הוספת L‑DOPA שינתה עוד יותר את הדפוס, והגבירה מולקולות נוספות כגון גליצין, תראונין וציטרולין. עם זאת, בקורטקס המצחוני של אותם בעלי חיים, רמות חומצות האמינו היו בעצם ללא שינוי משמעותי, גם לאחר חודשי אובדן דופמין וטיפול.
פרקינסון מול אלצהיימר במוח האנושי
דגימות אנושיות סיפקו סיפור משלים. בקאדט‑פוטמן של חולי פרקינסון רק תת‑קבוצה קטנה של חומצות אמינו השתנתה בעקביות. בכל שלבי התפשטות המחלה (שלבי בראק ליבי), רמות הסרין עלו; בשלב המתקדם ביותר הפרולין עלה אף הוא, בעוד שפוספואתנולאמין ירדה, והארגינין נטה לרדת בהשוואה לשלבים מוקדמים יותר. שינויים אלו מרמזים שככל שפרקינסון מתקדם, מסלולים כימיים מסוימים—הקושרים שימוש באנרגיה, הגנות נוגדות חמצון ואיתות—מתנדנדים. באופן חשוב, הסופריור פרונטל גירוס של חולי פרקינסון נראה בעיקרו תקין בהקשר זה, מה שמשקף את ממצאי הקוף ומדגיש שהשיבוש המטבולי מרוכז במעגלי התנועה. לעומת זאת, אנשים עם מחלת אלצהיימר הראו דפוס הפוך באותו אזור קדמי: מספר חומצות אמינו, כולל טריפטופן, פנילאלנין, תראונין, טירוזין ומתיונין, היו מוגברות בבירור, מה שמצביע על הפרעה ממוקדת קורטיקלית השונה מהנראית בפרקינסון.
התפקיד המיוחד של חומצת אמינו אחת
מבין כל המולקולות שנבדקו ברחבי בעלי החיים, אזורי המוח ושלבי המחלה, הסרין בלטה. היא הייתה מוגברת בקביעות באזור התנועה הפגוע בקופים שטופלו ברעלן ובאנשים עם פרקינסון, ועבודות קודמות של אותה קבוצה מצאו גם סרין מוגבר בנוזל השדרה ובדם של מטופלים. לסרין יש שתי צורות המראות זו את זו במראה, שהן יחד תומכות גם באיתות המוחי וגם בעבודות תחזוקה תאיות: צורה מסוימת מסייעת להפעיל קולטן מרכזי לגלוטמט המעורב בלמידה ותקשורת בין נוירונים, ואילו הצורה השניה מזינה יצירה של מרכיבי ממברנה, נוקלאוטידים ונוגדי חמצון. העלייה החוזרת של הסרין בניסויים השונים מרמזת שהמוח עשוי לנסות להסתגל לאובדן דופמין על‑ידי חיזוק מעגלים ומסלולי הגנה מסוימים, גם כשהמחלה מתקדמת.
מה זה אומר לחולים ולמבחנים עתידיים
בהסתכלות כוללת, התוצאות מראות ששינויים בכימיה של מולקולות קטנות במוח אינם אקראיים, אלא עוקבים אחרי דפוסים ברורים התלויים באזור המוח ובסוג המחלה. בפרקינסון, שינויים בחומצות האמינו מת聚ים במעגלי התנועה התלויים בדופמין והם יחסית מוגבלים בהיקפם, כאשר הסרין מתבלט כסמן מהימן של השיבוש; באלצהיימר, שינויים בחומצות האמינו בולטים יותר בקורטקס המצחוני. זה מרמז שחותמות מטבוליות בדם משקפות חלקית, אך אינן לכידות לגמרי, את מה שמתרחש במוח. עבור הקורא הכללי, המסקנה המרכזית היא שמעקב אחרי חומצות אמינו ספציפיות—ובפרט סרין—יכול אי‑פעם לסייע לדייק אבחנה, לעקוב אחרי התקדמות הפרקינסון ולהעריך האם טיפולים חדשים משיבים את הכימיה המוחית לכיוון בריא יותר, תוך אבחנה בין פרקינסון לצורות אחרות של דמנציה.
ציטוט: Gervasoni, J., Di Maio, A., Serra, M. et al. Ultra-performance liquid chromatography–mass spectrometry analysis of post-mortem brain tissue reveals specific amino acid profile dysregulation in Parkinson’s disease and Alzheimer’s disease patients. npj Parkinsons Dis. 12, 95 (2026). https://doi.org/10.1038/s41531-026-01306-x
מילות מפתח: מחלת פרקינסון, חומצות אמינו, סרין, מטבוליזם מוחי, מחלת אלצהיימר