Clear Sky Science · sv
TBL1X/TBL1XR1 styr β‑cells identitet via ett genregleringsnätverk som innehåller PAX6
Varför diabetes kan vara ett problem med cellernas identitet
De flesta ser diabetes som en störning av blodsockret, men djupt inne i bukspottkörteln handlar historien egentligen om identitet. Specialiserade betaceller känner normalt av stigande socker och frisätter insulin. Vid typ 2‑diabetes förlorar många av dessa celler sitt mogna kännetecken och slutar fungera korrekt. Denna studie avslöjar ett tidigare saknat kontrolllager som hjälper betaceller att behålla sin identitet, och visar hur dess fel kan dra kroppen mot diabetes.
Väktarna inne i betaceller
Betaceller lever i små kluster i bukspottkörteln som kallas öar och ansvarar för att bilda och utsöndra insulin. Deras identitet upprätthålls av ”huvudströmbrytare” i DNA, så kallade transkriptionsfaktorer, som slår på rätt gener och stänger av felaktiga. Men dessa huvudströmbrytare arbetar inte ensamma; de är beroende av hjälpproteiner som finjusterar när gener aktiveras eller tystas. Författarna fokuserar på två sådana hjälpare, TBL1X och TBL1XR1 (tillsammans kallade TBL/R1), och frågar om de är nödvändiga för att hålla betaceller funktionella och om de spelar roll för mänsklig diabetes.
Vad händer när väktarna tas bort
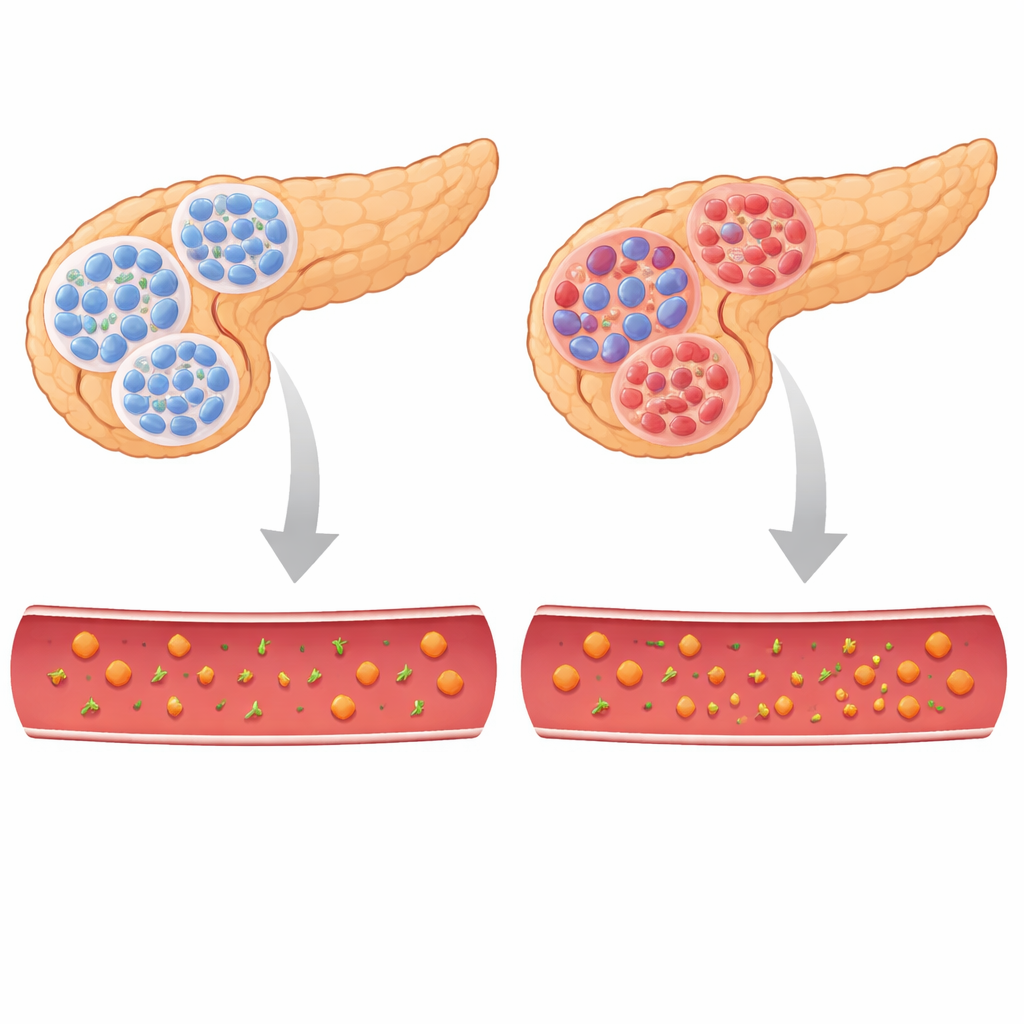
För att testa TBL/R1:s roll skapade forskarna möss där dessa hjälpproteiner togs bort endast i betaceller. I början verkade de unga djuren normala, men snart utvecklade de mycket högt blodsocker och gick ner i vikt, en klassisk diabeteslik bild. Deras kroppar var inte insulinresistenta; snarare producerade bukspottkörteln helt enkelt inte tillräckligt. Mätningar visade låga insulinnivåer i blodet och minskade insulinlager i bukspottkörteln, medan nivåerna av hormonet glukagon, som höjer blodsocker, ökade. Redan innan blodsockret steg var öarnas struktur störd: färre betaceller, alfaceller spridda genom öarna och en balans mellan celltyperna som liknade den man ser hos diabetiska djur.
Celler som glömmer vem de är
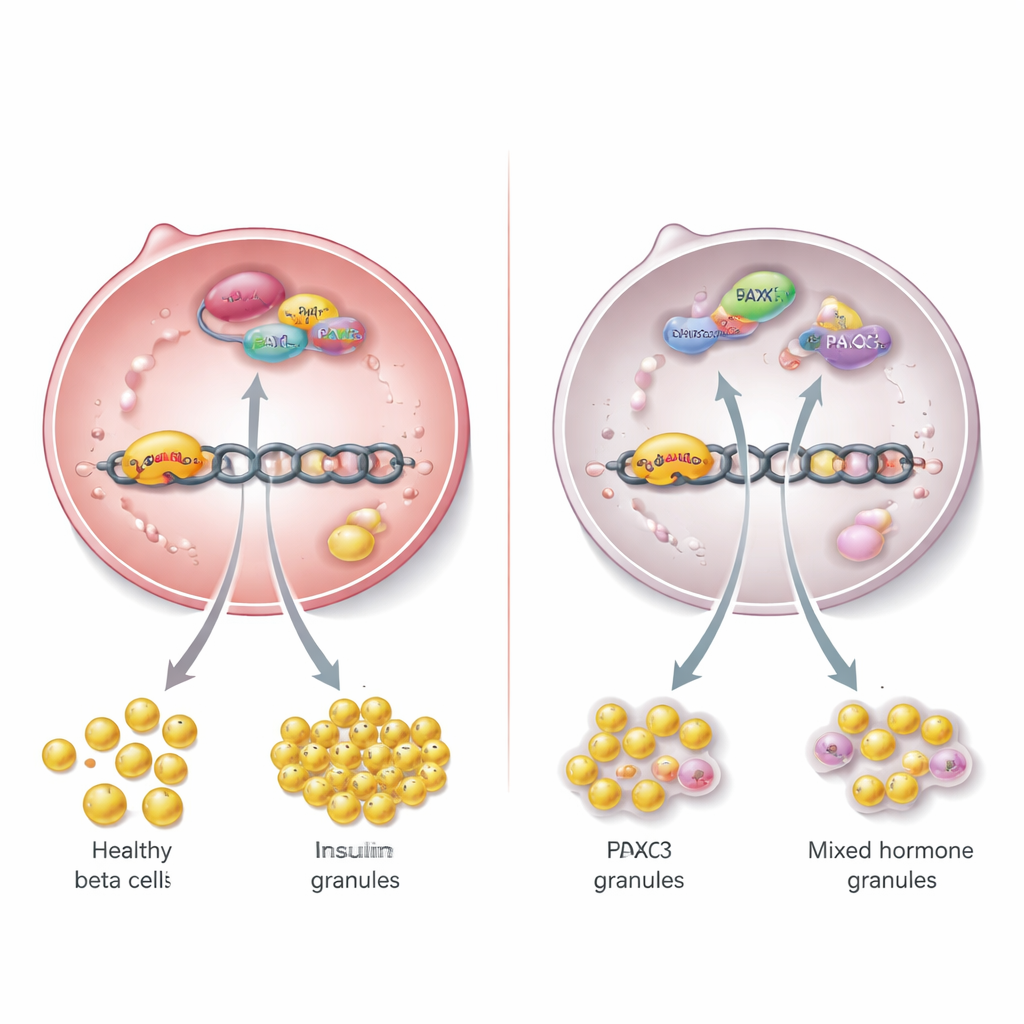
När teamet granskade genaktiviteten i öarna mer i detalj fann de omfattande förändringar. Tusentals gener ändrade sitt beteende när TBL/R1 saknades. Nyckelmarkörer för mogna betaceller, inklusive gener som kodar för insulin och proteiner som behövs för att känna av och hantera glukos, skiftade nedåt. Samtidigt ökade gener som normalt är ”icke tillåtna” i friska betaceller, liksom markörer för omogna eller alternativa öcellstyper. Singelcells‑RNA‑sekvensering, som profilerar individuella celler, bekräftade att äkta betaceller förlorades och ersattes av mindre mogna celler och sällsynta ”polyhormonella” celler som producerade blandningar av hormoner. Dessa mönster tyder på att utan TBL/R1 dör inte betaceller nödvändigtvis; istället driver de bort från sin specialiserade identitet mot ett mer primitivt eller blandat tillstånd som inte kan upprätthålla normal insulinproduktion.
Ett molekylärt samarbete mellan PAX6 och TBL/R1
För att förstå den underliggande mekanismen kartlade forskarna vilka nukleära proteiner som fysiskt interagerar med TBL/R1 i betacellinjer. Bland många partner identifierade de PAX6, en välkänd regulator av öutveckling och funktion. De visade att PAX6 och TBL/R1 båda sitter på insulin-genens kontrollregion tillsammans med ett annat protein, HDAC3, och bildar ett reglerande team direkt på DNA. När TBL/R1 experimentellt minskades kunde PAX6 inte längre förstärka insulin‑genens aktivitet, och insulinproduktion och frisättning sjönk. Att hämma HDAC3 försvagade också aktiveringen av insulingenen på ett sätt som var beroende av TBL/R1, vilket antyder att denna trio fungerar som en strömbrytare som främjar insulingenen samtidigt som den håller andra, olämpliga gener i schack.
Från musmekanism till mänsklig risk
Viktigt är att detta regleringssystem inte är begränsat till gnagare. I en mänsklig betacellinje hittades TBL1X, TBL1XR1 och PAX6 alla vid den mänskliga insulin‑genen och bildade liknande komplex med HDAC3. Att minska TBL/R1 i dessa celler sänkte insulingens aktivitet och insulinfrisättning. Teamet undersökte sedan mänskliga donatoröar och fann att lägre uttryck av TBL1X var kopplat till högre långtidsblodsockernivåer, mätt som HbA1c. Storskaliga genetiska studier i tiotusentals människor visade dessutom att vanliga DNA‑varianter nära TBL1X‑ och TBL1XR1‑generna är kopplade till högre HbA1c och slumpmässigt blodglukos, vilket knyter detta regleringslager till diabetesrisk i befolkningen.
Varför dessa fynd betyder något för framtida terapier
Sammantaget visar studien att TBL1X och TBL1XR1 fungerar som avgörande väktare av betacellsidentitet genom att samarbeta med PAX6 och associerade komplex för att hålla insulingener aktiva och olämpliga gener tysta. När detta kontrollager sviktar glömmer betaceller gradvis vem de är, vilket leder till för lite insulin och stigande blodsocker. Eftersom förlust av betacellsidentitet kan vara reversibel kan riktade insatser mot detta TBL/R1‑centrerade nätverk — antingen för att skydda befintliga betaceller eller för att förbättra mognaden av laboratorieodlade celler för transplantation — öppna nya, mer precisa behandlingsstrategier för typ 2‑diabetes.
Citering: Walth-Hummel, A.A., Jouffe, C., Weber, P. et al. TBL1X/TBL1XR1 govern β-cell identity through a PAX6-containing gene regulatory network. Nat Commun 17, 3736 (2026). https://doi.org/10.1038/s41467-026-72077-5
Nyckelord: betacellsidentitet, insulinreglering, transkriptionskofaktorer, typ 2‑diabetes, PAX6‑nätverk