Clear Sky Science · fr
TBL1X/TBL1XR1 gouvernent l’identité des cellules β via un réseau de régulation génique contenant PAX6
Pourquoi le diabète peut être un problème d’identité cellulaire
La plupart des gens associent le diabète à une maladie du sucre sanguin, mais dans le pancréas l’enjeu est avant tout une question d’identité. Les cellules spécialisées appelées cellules β détectent normalement l’élévation du glucose et libèrent de l’insuline. Dans le diabète de type 2, nombre de ces cellules perdent leur caractère mature et cessent de remplir correctement leur fonction. Cette étude révèle une couche de contrôle jusqu’ici manquante qui aide les cellules β à rester fidèles à leur identité, et montre comment sa défaillance peut faire basculer l’organisme vers le diabète.
Les gardiens au sein des cellules β
Les cellules β vivent en petits amas dans le pancréas, appelés îlots, et sont responsables de la fabrication et de la sécrétion d’insuline. Leur identité est imposée par des « interrupteurs maîtres » dans l’ADN, les facteurs de transcription, qui activent les bons gènes et répriment les mauvais. Mais ces interrupteurs ne fonctionnent pas seuls ; ils s’appuient sur des protéines auxiliaires qui ajustent finement l’activation ou la répression des gènes. Les auteurs se concentrent sur deux de ces aides, TBL1X et TBL1XR1 (collectivement appelés TBL/R1), pour savoir si elles sont essentielles au maintien de la fonctionnalité des cellules β et si elles ont une importance pour le diabète humain.
Que se passe-t-il quand les gardiens sont supprimés
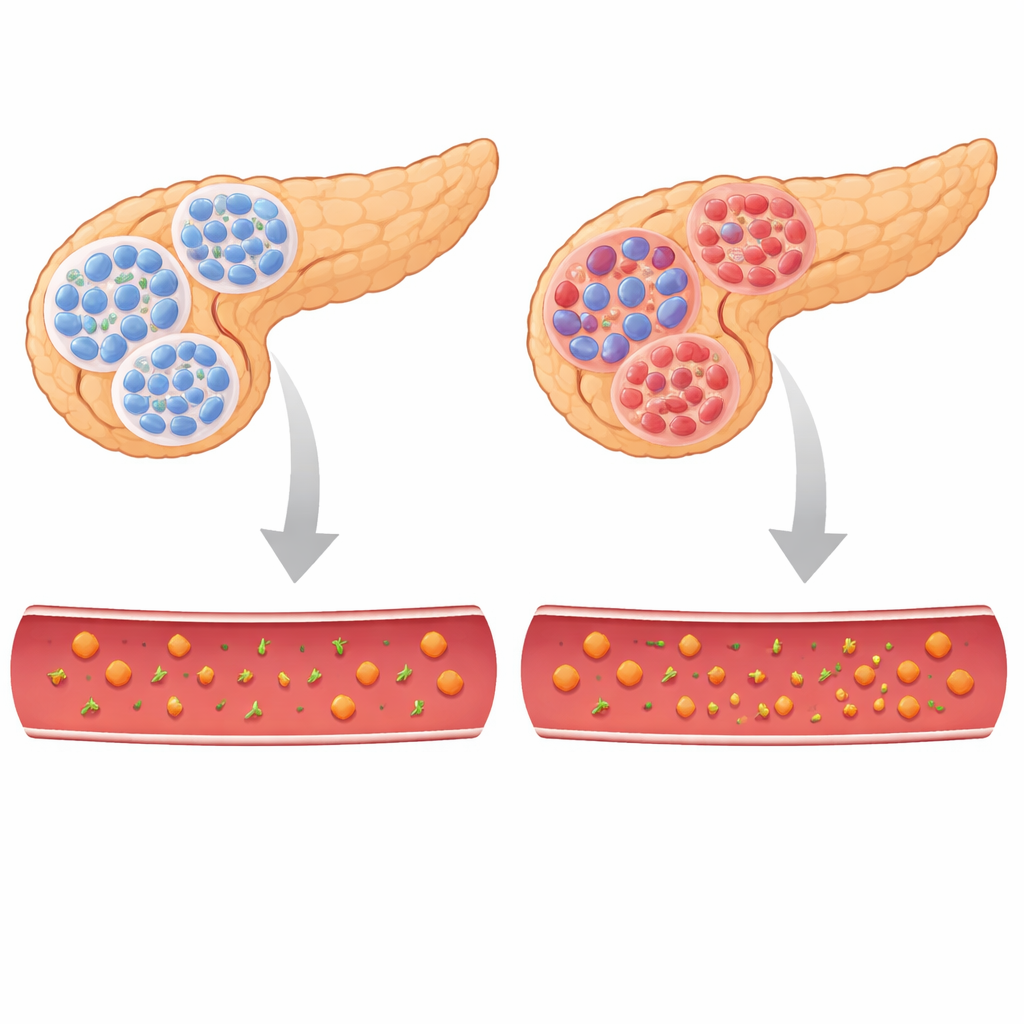
Pour tester le rôle de TBL/R1, les chercheurs ont généré des souris chez lesquelles ces protéines auxiliaires étaient supprimées uniquement dans les cellules β. Au début, les jeunes animaux semblaient normaux, mais rapidement ils ont développé une hyperglycémie marquée et une perte de poids, un tableau classique évoquant le diabète. Leur organisme n’était pas résistant à l’insuline ; c’est plutôt le pancréas qui produisait insuffisamment d’insuline. Les mesures ont montré de faibles taux d’insuline dans le sang et des réserves d’insuline réduites dans le pancréas, tandis que les taux de glucagon, l’hormone qui augmente la glycémie, étaient accrus. Avant même l’élévation de la glycémie, la structure des îlots était déjà perturbée : il y avait moins de cellules β, des cellules α dispersées dans les îlots, et l’équilibre entre ces types cellulaires rappelait celui observé chez des animaux diabétiques.
Des cellules qui oublient qui elles sont
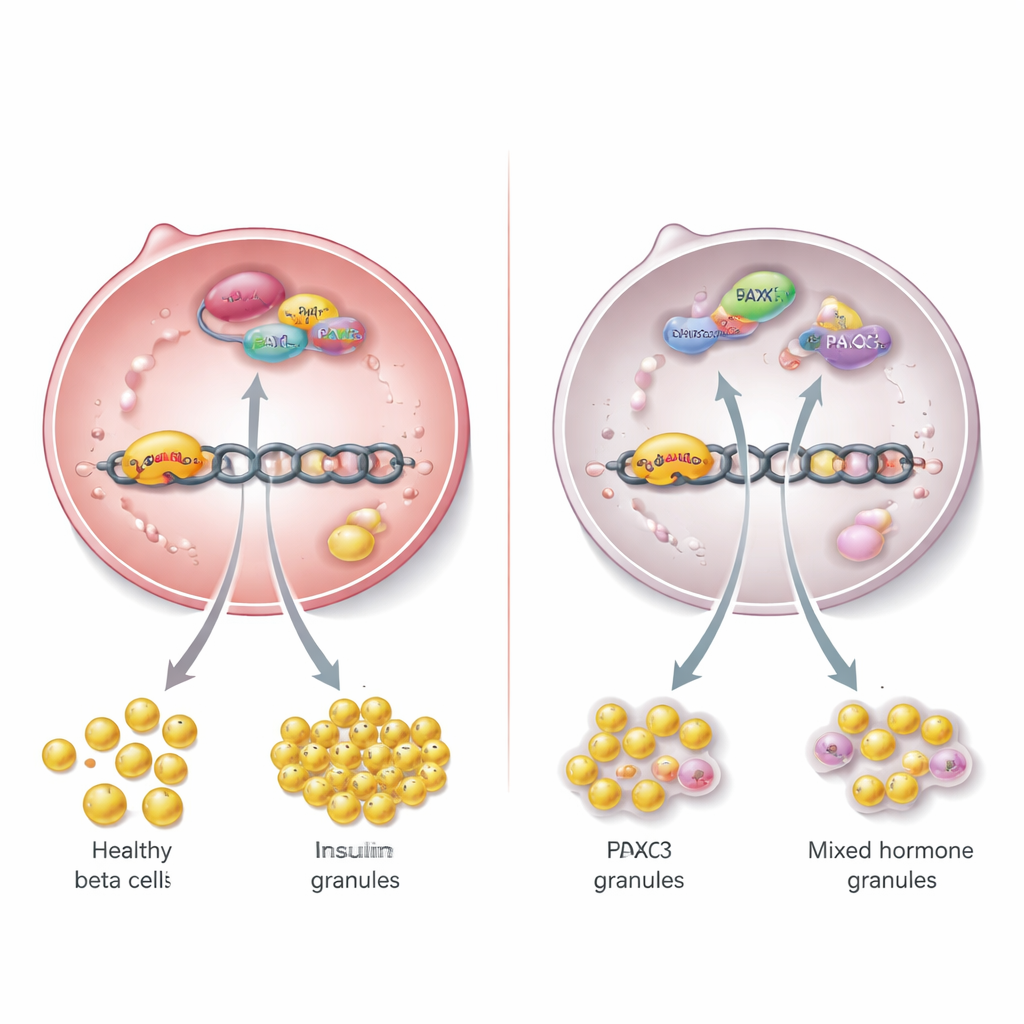
En examinant plus en détail l’activité génique dans les îlots, l’équipe a observé des changements profonds. Des milliers de gènes ont modifié leur comportement en l’absence de TBL/R1. Les marqueurs clés des cellules β matures, y compris les gènes codant l’insuline et les protéines nécessaires à la détection et au métabolisme du glucose, étaient réprimés. Parallèlement, des gènes normalement « interdits » dans les cellules β saines, ainsi que des marqueurs de cellules d’îlots immatures ou alternatives, étaient activés. Le séquençage ARN monocellulaire, qui profile des cellules individuelles, a confirmé que les véritables cellules β étaient perdues et remplacées par des cellules moins matures et de rares cellules « polyhormonales » produisant des mélanges d’hormones. Ces schémas indiquent que sans TBL/R1, les cellules β ne meurent pas nécessairement ; elles dérivent plutôt de leur identité spécialisée vers un état plus primitif ou mixte qui ne peut soutenir une production d’insuline normale.
Une coopération moléculaire entre PAX6 et TBL/R1
Pour comprendre le mécanisme sous-jacent, les chercheurs ont cartographié les protéines nucléaires interagissant physiquement avec TBL/R1 dans des lignées de cellules β. Parmi de nombreux partenaires, ils ont identifié PAX6, un régulateur bien connu du développement et de la fonction des îlots. Ils ont montré que PAX6 et TBL/R1 se trouvent tous deux sur la région régulatrice du gène de l’insuline, conjointement avec une autre protéine, HDAC3, formant une équipe régulatrice directement sur l’ADN. Lorsque TBL/R1 étaient expérimentablement réduits, PAX6 ne pouvait plus stimuler l’activité du gène de l’insuline, et la production ainsi que la libération d’insuline diminuaient. L’inhibition de HDAC3 affaiblissait également l’activation du gène de l’insuline de manière dépendante de TBL/R1, ce qui suggère que ce trio agit comme un interrupteur promouvant l’expression du gène de l’insuline tout en contribuant à réprimer d’autres gènes inappropriés.
Du mécanisme murin au risque humain
Il est important que ce système régulateur ne soit pas limité aux rongeurs. Dans une lignée de cellules β humaines, TBL1X, TBL1XR1 et PAX6 ont été retrouvés au niveau du gène humain de l’insuline et formaient des complexes similaires avec HDAC3. Réduire TBL/R1 dans ces cellules diminuait l’activité du gène de l’insuline et la sécrétion d’insuline. L’équipe a ensuite examiné des îlots provenant de donneurs humains et constaté qu’une expression plus faible de TBL1X était associée à des niveaux plus élevés de glycémie à long terme, mesurés par l’HbA1c. Des études génétiques à grande échelle, portant sur des dizaines de milliers de personnes, ont en outre montré que des variants communs situés près des gènes TBL1X et TBL1XR1 sont liés à une HbA1c plus élevée et à une glycémie aléatoire plus élevée, reliant ainsi cette couche régulatrice au risque de diabète au niveau de la population.
Pourquoi ces découvertes comptent pour les thérapies futures
Pris ensemble, ces résultats révèlent que TBL1X et TBL1XR1 agissent comme des gardiens cruciaux de l’identité des cellules β en s’associant à PAX6 et à des complexes associés pour maintenir actifs les gènes de l’insuline et réprimer les gènes inappropriés. Lorsque cette couche de contrôle faiblit, les cellules β oublient progressivement qui elles sont, conduisant à une insuffisance d’insuline et à une élévation de la glycémie. Parce que la perte d’identité des cellules β peut être réversible, cibler ce réseau centré sur TBL/R1 — soit pour protéger les cellules β existantes, soit pour améliorer la maturation de cellules cultivées en laboratoire pour la transplantation — pourrait ouvrir la voie à des stratégies thérapeutiques plus précises pour le diabète de type 2.
Citation: Walth-Hummel, A.A., Jouffe, C., Weber, P. et al. TBL1X/TBL1XR1 govern β-cell identity through a PAX6-containing gene regulatory network. Nat Commun 17, 3736 (2026). https://doi.org/10.1038/s41467-026-72077-5
Mots-clés: identité des cellules bêta, régulation de l’insuline, cofacteurs transcriptionnels, diabète de type 2, réseau PAX6