Clear Sky Science · nl
TBL1X/TBL1XR1 bepalen de identiteit van β-cellen via een PAX6-bevattend genregulatienetwerk
Waarom diabetes een probleem van celidentiteit kan zijn
De meeste mensen zien diabetes als een aandoening van de bloedsuiker, maar diep in de alvleesklier gaat het in feite om identiteit. Gespecialiseerde bèta‑cellen herkennen stijgende suikerwaarden en geven insuline af. Bij type 2 diabetes verliezen veel van deze cellen hun volwassen karakter en stoppen ze hun taak goed te vervullen. Deze studie onthult een eerder ontbrekende regelingslaag die helpt dat bèta‑cellen trouw blijven aan hun identiteit, en toont hoe het falen daarvan het lichaam richting diabetes kan duwen.
De bewakers binnenin bèta‑cellen
Bèta‑cellen leven in kleine klompjes in de alvleesklier, de zogenaamde eilandjes, en zijn verantwoordelijk voor de productie en secretie van insuline. Hun identiteit wordt bewaakt door “meesterschakelaars” in het DNA, de transcriptiefactoren, die de juiste genen aan en de verkeerde uit zetten. Maar deze meesterschakelaars opereren niet alleen; ze vertrouwen op hulp-eiwitten die fijnafstellen wanneer genen geactiveerd of stilgelegd worden. De auteurs richten zich op twee van zulke helpers, TBL1X en TBL1XR1 (samen TBL/R1 genoemd), en vragen of ze essentieel zijn om bèta‑cellen functioneel te houden en of ze van betekenis zijn voor menselijke diabetes.
Wat er gebeurt als de bewakers verdwijnen
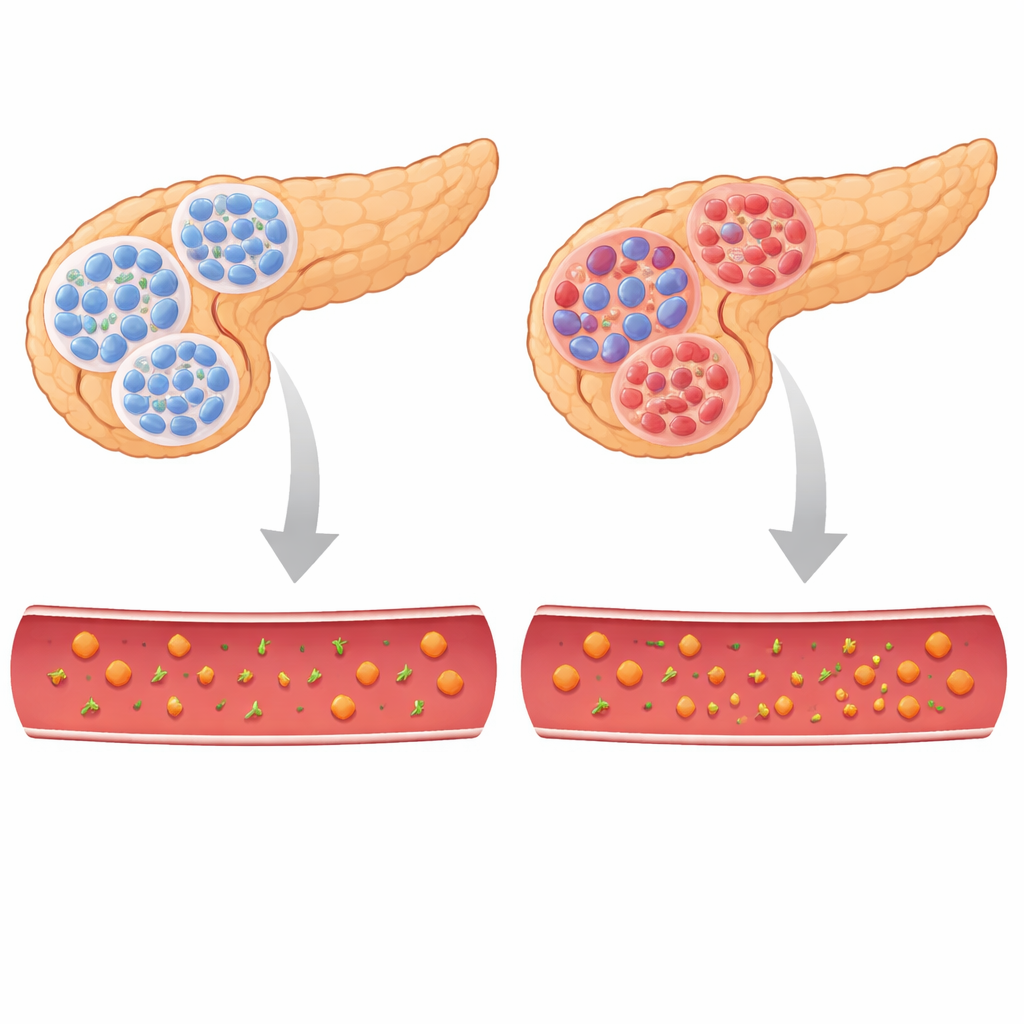
Om de rol van TBL/R1 te testen, maakten de onderzoekers muizen waarbij deze helpers alleen in bèta‑cellen werden verwijderd. Aanvankelijk leken jonge dieren normaal, maar al snel ontwikkelden ze zeer hoge bloedsuikers en gewichtsverlies, een klassiek beeld dat op diabetes wijst. Hun lichaam was niet resistent tegen insuline; de alvleesklier maakte simpelweg onvoldoende insuline aan. Metingen lieten lage insulinewaarden in het bloed zien en verminderde insulinevoorraden in de alvleesklier, terwijl niveaus van het hormoon glucagon, dat de bloedsuiker verhoogt, waren toegenomen. Zelfs voordat de bloedsuiker steeg, was de structuur van de eilandjes al verstoord: er waren minder bèta‑cellen, alfa‑cellen waren verspreid door de eilandjes en de balans tussen deze celtypen leek op die van diabetesdiermodellen.
Cellen die vergeten wie ze zijn
Een nadere blik op genactiviteit in de eilandjes toonde ingrijpende veranderingen. Duizenden genen veranderden hun gedrag toen TBL/R1 ontbraken. Belangrijke merkers van volwassen bèta‑cellen, waaronder de genen die insuline coderen en eiwitten die nodig zijn voor het detecteren en verwerken van glucose, werden naar beneden bijgesteld. Tegelijkertijd werden genen die in gezonde bèta‑cellen normaal gesproken “niet toegestaan” zijn, evenals merkers van onrijpere of alternatieve eilandceltypen, juist geactiveerd. Single‑cell RNA‑sequencing, waarmee individuele cellen worden geprofileerd, bevestigde dat echte bèta‑cellen verloren gingen en werden vervangen door minder rijpe cellen en zeldzame “polyhormonale” cellen die mengsels van hormonen produceerden. Deze patronen duiden erop dat zonder TBL/R1 bèta‑cellen niet per se afsterven; in plaats daarvan drijven ze weg van hun gespecialiseerde identiteit naar een meer primitieve of gemengde staat die normaal insuline‑uitvoer niet kan volhouden.
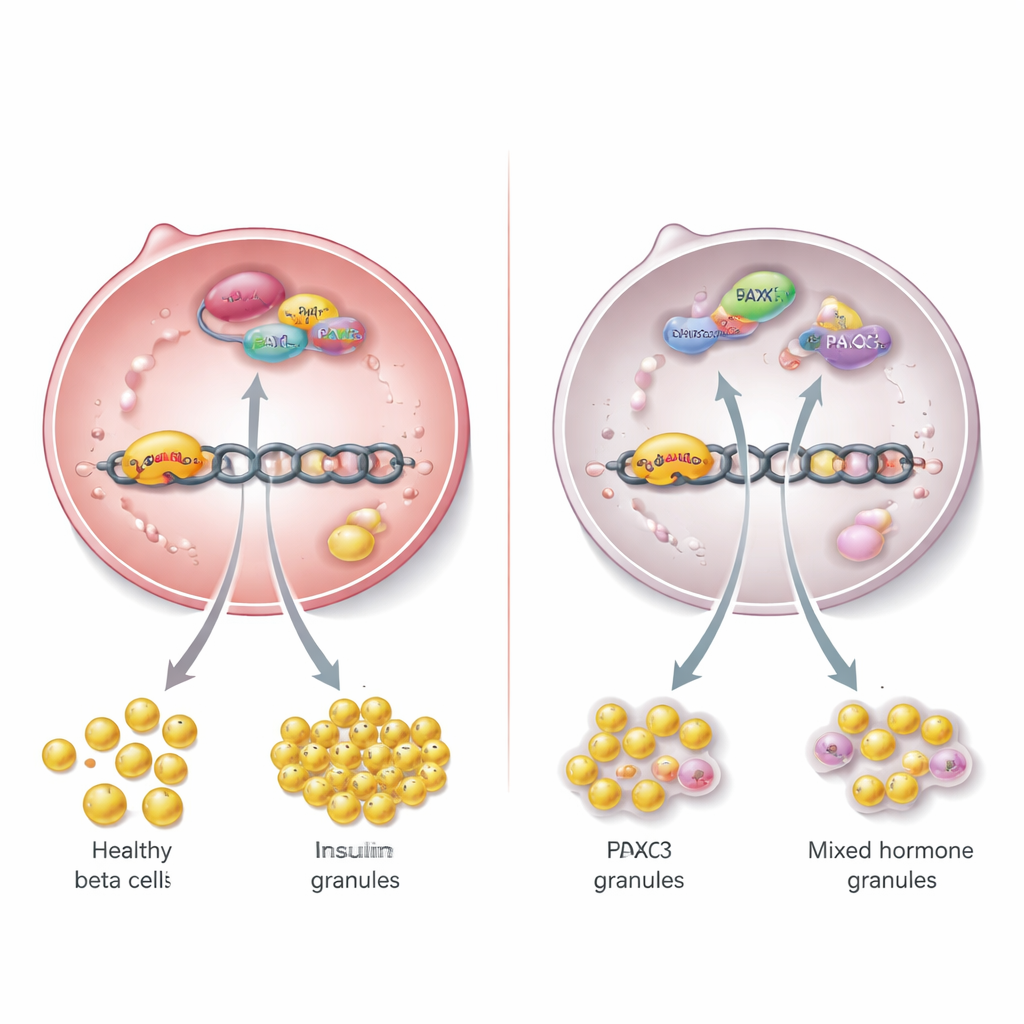
Een moleculair samenspel tussen PAX6 en TBL/R1
Om het onderliggende mechanisme te begrijpen, brachten de onderzoekers in kaart welke nucleaire eiwitten fysiek met TBL/R1 interageren in bèta‑cellijnen. Tussen talrijke partners identificeerden ze PAX6, een bekende regulator van eilandontwikkeling en -functie. Ze toonden aan dat PAX6 en TBL/R1 beide plaatsnemen op het controlegebied van het insulinegen, samen met een ander eiwit, HDAC3, en zo een regulerend team vormen direct op het DNA. Wanneer TBL/R1 experimenteel werden verminderd, kon PAX6 het insulinegen niet langer versterken, en daalden insulineproductie en -afgifte. Het remmen van HDAC3 verzwakte ook de activatie van het insulinegen op een manier die afhankelijk was van TBL/R1, wat suggereert dat dit trio fungeert als een schakelaar die de expressie van het insulinegen bevordert en tegelijkertijd ongepaste genen onderdrukt.
Van muismechanisme naar menselijke risico’s
Belangrijk is dat dit regelingssysteem zich niet beperkt tot knaagdieren. In een menselijke bèta‑cellijn werden TBL1X, TBL1XR1 en PAX6 allemaal gevonden bij het menselijke insulinegen en vormden ze vergelijkbare complexen met HDAC3. Het verlagen van TBL/R1 in deze cellen verminderde de activiteit van het insulinegen en de insulinesecretie. Het team bekeek vervolgens menselijke donor‑eilandjes en vond dat lagere TBL1X‑expressie geassocieerd was met hoger langetermijnbloedsuiker, gemeten via HbA1c. Grootschalige genetische studies bij tienduizenden mensen lieten bovendien zien dat veelvoorkomende DNA‑varianten nabij de TBL1X‑ en TBL1XR1‑genen samenhangen met hogere HbA1c‑waarden en hogere random bloedsuiker, waarmee deze regelingslaag wordt verbonden aan het bevolkingsrisico op diabetes.
Waarom deze bevindingen belangrijk zijn voor toekomstige therapieën
Samengevoegd onthult de studie dat TBL1X en TBL1XR1 fungeren als cruciale bewakers van bèta‑celidentiteit door samen te werken met PAX6 en geassocieerde complexen om insulinegenen actief te houden en ongepaste genen stil te leggen. Wanneer deze controlelaag faalt, vergeten bèta‑cellen geleidelijk wie ze zijn, wat leidt tot te weinig insuline en stijgende bloedsuiker. Omdat verlies van bèta‑celidentiteit mogelijk omkeerbaar is, kan het richten op dit TBL/R1‑gecentreerde netwerk — hetzij om bestaande bèta‑cellen te beschermen of om de rijping van in het laboratorium gekweekte cellen voor transplantatie te verbeteren — nieuwe, preciezere behandelstrategieën voor type 2 diabetes openen.
Bronvermelding: Walth-Hummel, A.A., Jouffe, C., Weber, P. et al. TBL1X/TBL1XR1 govern β-cell identity through a PAX6-containing gene regulatory network. Nat Commun 17, 3736 (2026). https://doi.org/10.1038/s41467-026-72077-5
Trefwoorden: beta cel identiteit, insulinemodulatie, transcriptionele cofactors, type 2 diabetes, PAX6-netwerk