Clear Sky Science · sv
Tumörspecifik lncRNA IGF1R-AS1 reglerar trans-kromatininteraktioner kopplade till onkogent MYC-signalering
Hur en dold RNA-strömbrytare kan driva vissa cancerformer
Varför växer vissa prostata- och lungcancerformer så aggressivt, och kan vi hitta strömbrytare som bara finns i tumörceller för att kontrollera dem? Denna studie avslöjar en tidigare förbiseddd del av RNA som är nästan exklusiv för tumörer och som verkar hjälpa till att slå på MYC, en av de mest kraftfulla tillväxtdrivarna i cancer. Att förstå hur detta RNA fungerar kan öppna nya sätt att upptäcka och möjligen oskadliggöra farliga cancerformer utan att skada frisk vävnad. 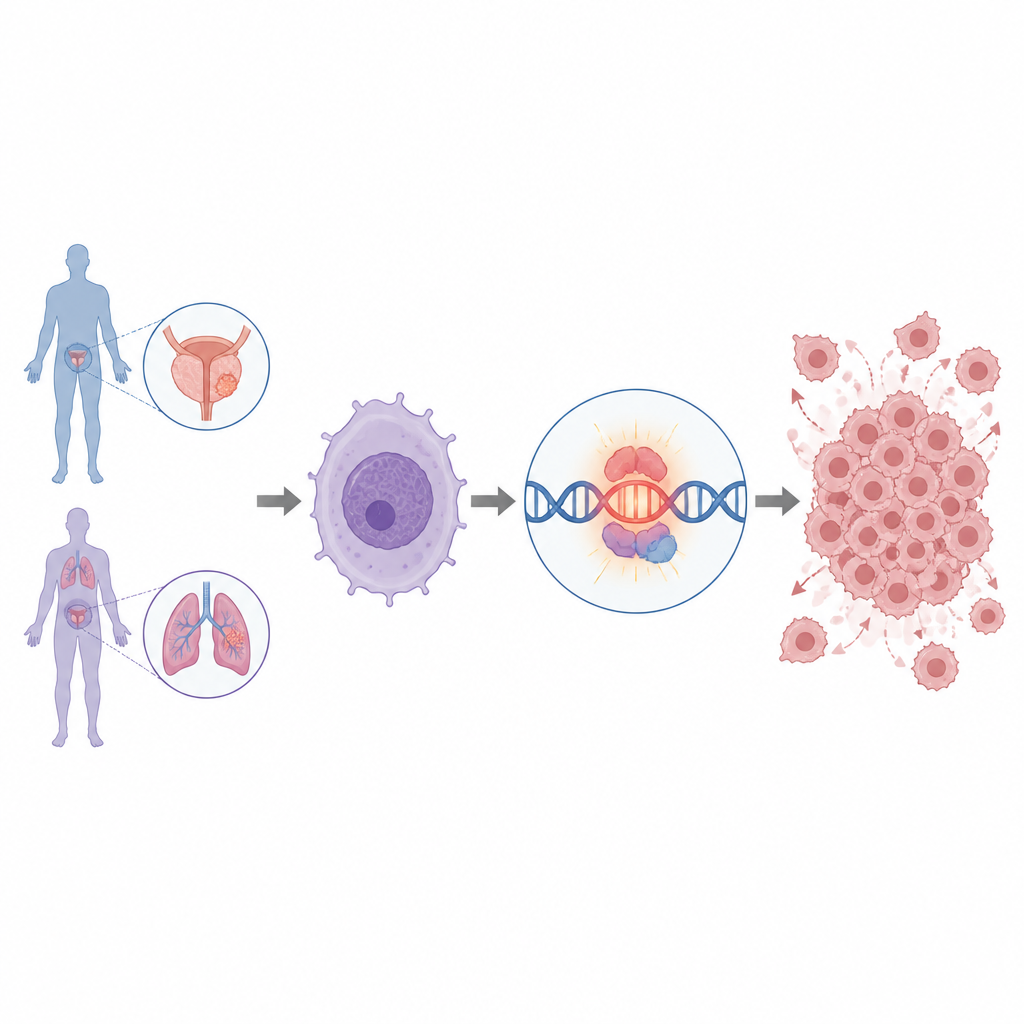
En tumör-endast signal i prostata- och lungcancer
Forskarna började med att sålla igenom RNA-data från män med avancerad, behandlingsresistent prostatacancer. De fokuserade på långa icke-kodande RNA, en klass av RNA-molekyler som inte kodar för proteiner men som ändå kan påverka geners beteende kraftigt. Genom att kombinera patientdata med kartor över DNA-kontrollregioner kallade super-enhancers identifierade de mer än tusen långa icke-kodande RNA. Ett av dessa, kallat IGF1R-AS1, stack ut eftersom det var tätt kopplat till en kraftfull super-enhancer och var påslaget nästan uteslutande i tumörer, särskilt i avancerad prostatacancer och i vissa lungcancerformer, medan det var nästan tyst i normal vävnad.
Från RNA-upptäckt till cancerns beteende
Att hitta ett tumör-specifikt RNA är intressant, men spelar det faktiskt någon roll för cancerstillväxt? För att testa detta använde teamet molekylära verktyg för att minska nivåerna av IGF1R-AS1 i prostata- och lungcancerceller odlade i laboratoriet. När detta RNA slogs ner växte cellerna långsammare, rörde sig mindre och hade sämre förmåga att invadera genom en barriär — alla kännetecken för minskad canceraggressivitet. I möss som hade fått mänskliga prostatacancerceller implanterade växte tumörer utan IGF1R-AS1 långsammare och djuren överlevde längre. Dessa experiment visade att IGF1R-AS1 inte bara är en åskådningsfaktor utan spelar en aktiv roll som främjar cancer.
En ny väg för att slå på onkogenen MYC
När forskarna grävde djupare tittade de på vilka gener som förändrades när IGF1R-AS1 togs bort. Ett tydligt mönster framträdde: många gener som kontrolleras av MYC skruvades ned, och MYC själv minskade både på RNA- och proteinnivå. Däremot förändrades den närliggande IGF1R-genen, som ligger intill IGF1R-AS1 i genomet, knappt alls. Det betydde att IGF1R-AS1 inte bara justerade sin granne, som många liknande RNA gör. Istället agerade det på distans för att förstärka MYC, en huvudregulator av celldelning. I patienttumörer korrelerade hög aktivitet i det IGF1R-AS1-kopplade gen-nätverket och hög MYC-aktivitet med sämre överlevnad, särskilt i avancerad prostatacancer. 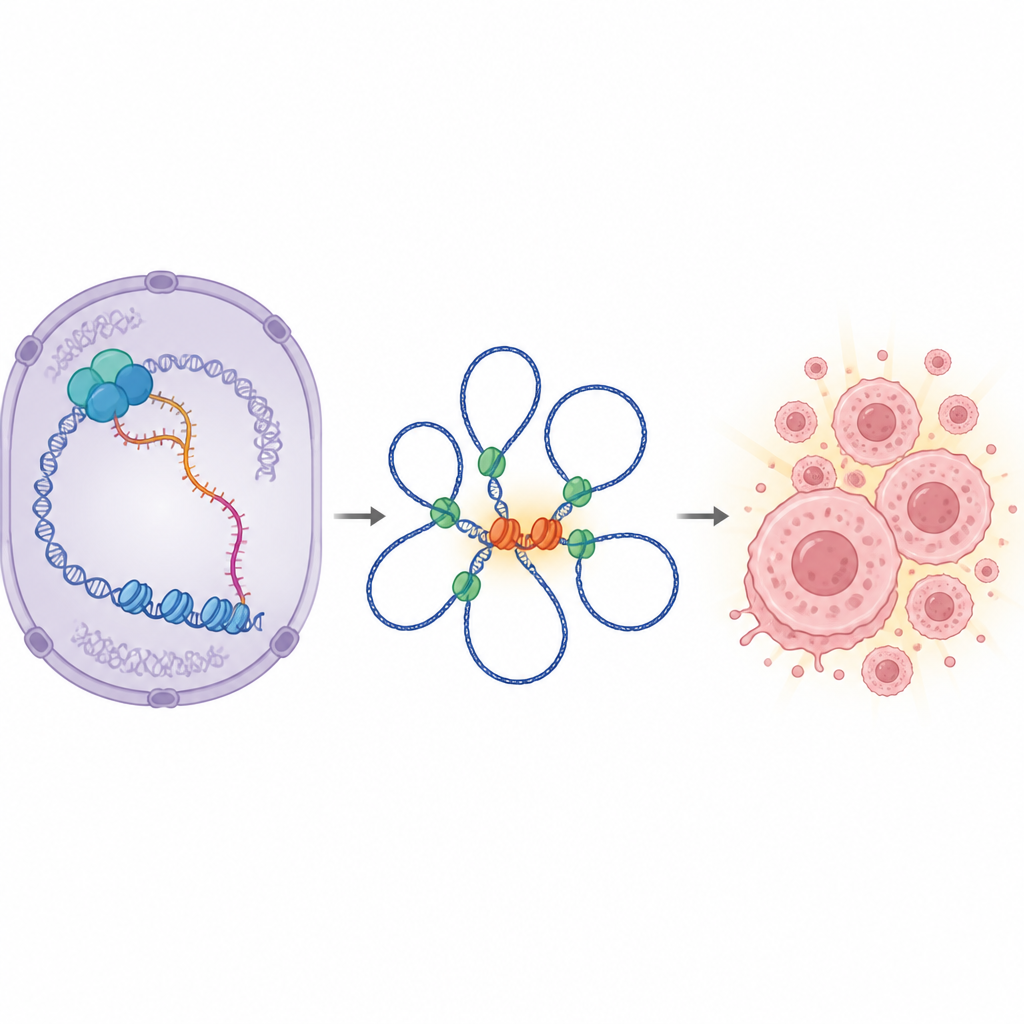
Formar det tredimensionella genomet för att gynna cancerstillväxt
Hur kan en RNA-molekyl som ligger långt från MYC öka dess aktivitet? Svaret ligger i DNA:s tredimensionella vikning inne i kärnan. Teamet visade att IGF1R-AS1 huvudsakligen finns i kärnan och fysiskt binder till kromatinombyggnadsproteiner (såsom SMARCA4 och SMARCA1) och till det arkitektoniska proteinet CTCF, som hjälper till att bilda DNA-loopar. Dessa loopar för samman avlägsna enhancer-regioner med MYC-genen. När IGF1R-AS1 minskades blev många enhancer-ställen mindre tillgängliga, och långräckviddiga DNA-loopar som kopplar samman viktiga enhancer-nav med MYC-promotorn försvagades eller försvann. Särskilt en välkänd enhancer-region nära ett annat RNA kallat CCAT1 tappade kontakten med MYC i prostatacellinjer som är beroende av IGF1R-AS1. Data stöder en modell där IGF1R-AS1 fungerar som ett byggnadsställning, som hjälper kromatinombyggare och CTCF att samarbeta för att bibehålla loopar som håller MYC påslaget.
Varför detta dolda RNA betyder något för patienter
För icke-experter är slutsatsen att denna studie avslöjar ett tumörspecifikt RNA som hjälper till att omforma DNA-arkitekturen inne i cancerceller för att hålla ett kraftfullt tillväxtgen, MYC, i ett "på"-läge. Eftersom IGF1R-AS1 till stora delar saknas i normal vävnad men är viktig för tumörtillväxt och spridning kan det fungera som en markör för att identifiera högriskcancer och som ett potentiellt mål för terapier som selektivt angriper cancerceller. Mer generellt visar arbetet hur icke-kodande RNA kan organisera genomet i 3D för att påverka vilka gener som är aktiva, vilket lägger till ett viktigt nytt lager i vår förståelse av hur cancer uppstår och fortskrider.
Citering: Yang, Y., Wang, TY., Fry, J. et al. Tumor-specific lncRNA IGF1R-AS1 trans-regulates chromatin interactions associated with oncogenic MYC signaling. Nat Commun 17, 4171 (2026). https://doi.org/10.1038/s41467-026-70814-4
Nyckelord: prostatacancer, lång icke-kodande RNA, MYC-signalering, kromatinloopning, tumörbiomarkörer