Clear Sky Science · nl
Tumor-specifieke lncRNA IGF1R-AS1 reguleert trans-chromatine-interacties die samenhangen met oncogene MYC-signaleringsroutes
Hoe een verborgen RNA-schakelaar bepaalde kankers kan aanwakkeren
Waarom groeien sommige prostaat- en longkankers zo agressief, en kunnen we schakelaars vinden die uitsluitend in tumorcellen bestaan om ze te beheersen? In deze studie wordt een eerder onopgemerkt RNA-element onthuld dat bijna exclusief in tumoren voorkomt en lijkt mee te helpen MYC aan te zetten, een van de krachtigste groeidrivers in kanker. Inzicht in hoe dit RNA werkt kan nieuwe mogelijkheden openen om gevaarlijke kankers te detecteren en mogelijk uit te schakelen zonder gezond weefsel te beschadigen. 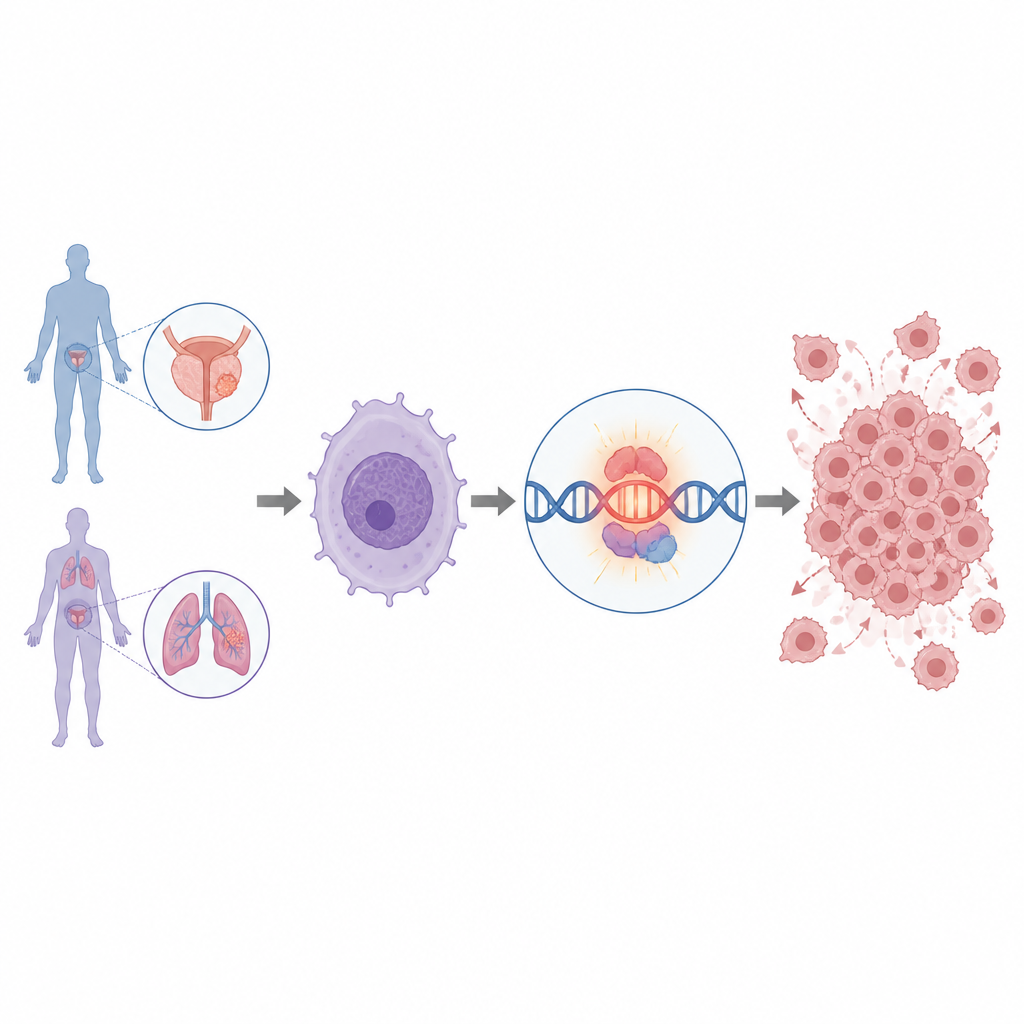
Een tumor-specifiek signaal in prostaat- en longkanker
De onderzoekers begonnen met het doorzoeken van RNA-gegevens van mannen met gevorderde, therapieresistente prostaatkanker. Ze richtten zich op lange niet-coderende RNA's, een klasse RNA-moleculen die geen eiwitten produceren maar wel sterk kunnen beïnvloeden hoe genen zich gedragen. Door patiëntgegevens te combineren met kaarten van DNA-controlegebieden, zogenoemde super-enhancers, identificeerden ze meer dan duizend lange niet-coderende RNA's. Een daarvan, IGF1R-AS1 genaamd, sprong eruit omdat het nauw verbonden was met een krachtige super-enhancer en vrijwel alleen in tumoren was aangeschakeld, vooral in gevorderde prostaatkanker en in sommige longkankers, terwijl het in normaal weefsel vrijwel stil bleef.
Van RNA-ontdekking naar kankergedrag
Het vinden van een tumor-specifiek RNA is intrigerend, maar is het ook relevant voor kankergroei? Om dit te testen gebruikten de onderzoekers moleculaire middelen om IGF1R-AS1-niveaus te verminderen in in vitro gekweekte prostaat- en longkankercellen. Wanneer dit RNA werd onderdrukt, groeiden de cellen langzamer, bewogen minder en waren zij minder in staat om door een barrière heen te dringen—allemaal kenmerken van verminderde kankeragressiviteit. In muizen die waren geïmplanteerd met menselijke prostaatkankercellen groeiden tumoren zonder IGF1R-AS1 langzamer en leefden de dieren langer. Deze experimenten toonden aan dat IGF1R-AS1 geen bijstander is maar een actieve, kankerveroorzakende rol vervult.
Een nieuwe route om het MYC-oncogen aan te zetten
Dieper gravend bekeken de wetenschappers welke genen veranderden wanneer IGF1R-AS1 werd verwijderd. Er verscheen een duidelijk patroon: veel door MYC gecontroleerde genen werden naar beneden bijgesteld en MYC zelf daalde zowel op RNA- als eiwitniveau. Het dichtstbijzijnde gen, IGF1R, dat naast IGF1R-AS1 in het genoom ligt, veranderde nauwelijks. Dit wees erop dat IGF1R-AS1 niet simpelweg zijn buurgene fijnregelt, zoals veel vergelijkbare RNA's doen. In plaats daarvan werkte het op afstand om MYC te versterken, een meesterregelaar van celdeling. In patiënttumoren gingen hoge activiteit van het IGF1R-AS1-gekoppelde genennetwerk en hoge MYC-activiteit gepaard met slechtere overleving, vooral bij gevorderde prostaatkanker. 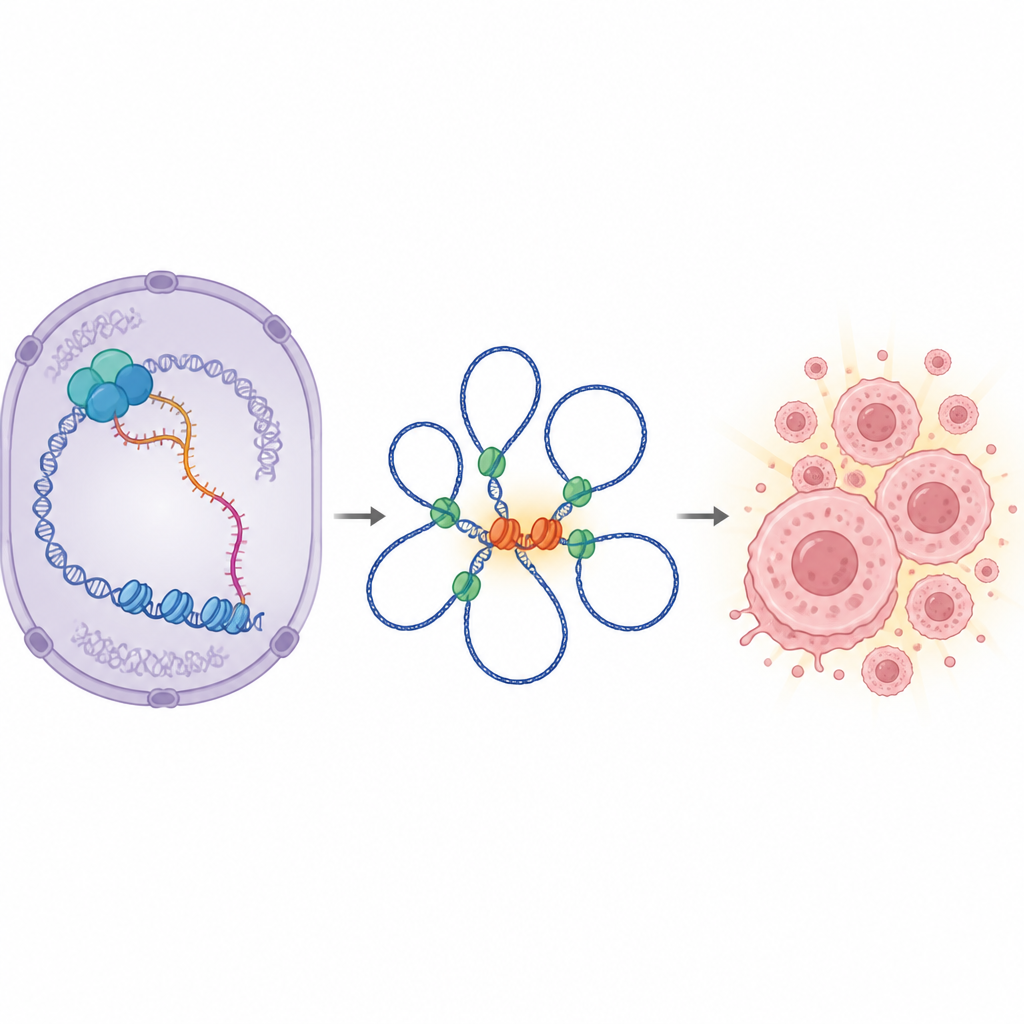
De 3D-genoomstructuur vormen ten gunste van kankergroei
Hoe kan een RNA-molecuul ver van MYC af zijn activiteit opvoeren? Het antwoord ligt in de driedimensionale vouwing van DNA in de celkern. Het team toonde aan dat IGF1R-AS1 voornamelijk in de kern zit en fysiek bindt aan chromatineremodelerende eiwitten (zoals SMARCA4 en SMARCA1) en aan het architecturale eiwit CTCF, dat helpt bij het vormen van DNA-lussen. Deze lussen brengen verre enhancerregio's in contact met het MYC-gen. Wanneer IGF1R-AS1 werd verminderd, werden veel enhancerlocaties minder toegankelijk en verzwakten of verdwenen langeafstandslussen die belangrijke enhancerhubs met de MYC-promoter verbinden. In het bijzonder verloor een bekende enhancerregio nabij een ander RNA, CCAT1, het contact met MYC in prostaatkankercellen die afhankelijk zijn van IGF1R-AS1. De gegevens ondersteunen een model waarin IGF1R-AS1 fungeert als een scaffold, die chromatineremodelers en CTCF helpt samenwerken om lussen te behouden die MYC ingeschakeld houden.
Waarom dit verborgen RNA van belang is voor patiënten
Voor niet-specialisten is de kernboodschap dat deze studie een tumor-specifiek RNA onthult dat de DNA-architectuur in kankercellen helpt herschikken om een krachtige groeigen, MYC, in een "aan"-stand te houden. Omdat IGF1R-AS1 grotendeels afwezig is in normaal weefsel maar belangrijk is voor tumorgroei en -verspreiding, kan het dienen als marker om hoogrisicokankers te identificeren en als potentieel aanknopingspunt voor therapieën die gericht zijn op kankercellen. Meer in het algemeen laat dit werk zien hoe niet-coderende RNA's de 3D-structuur van het genoom kunnen organiseren om te beïnvloeden welke genen actief zijn, en voegt daarmee een belangrijke laag toe aan ons begrip van hoe kankers ontstaan en voortschrijden.
Bronvermelding: Yang, Y., Wang, TY., Fry, J. et al. Tumor-specific lncRNA IGF1R-AS1 trans-regulates chromatin interactions associated with oncogenic MYC signaling. Nat Commun 17, 4171 (2026). https://doi.org/10.1038/s41467-026-70814-4
Trefwoorden: prostaatkanker, lange niet-coderende RNA, MYC-signalisatie, chromatine-lusvorming, tumormarkers