Clear Sky Science · pl
Nowotworowo-specyficzne lncRNA IGF1R-AS1 trans-reguluje interakcje chromatyny związane z onkogennym sygnalizowaniem MYC
Jak ukryty przełącznik RNA może zasilać niektóre nowotwory
Dlaczego niektóre raki prostaty i płuca rosną tak agresywnie i czy można znaleźć przełączniki obecne wyłącznie w komórkach nowotworowych, które je kontrolują? To badanie ujawnia wcześniej nieznany fragment RNA, prawie wyłącznie obecny w guzach, który wydaje się pomagać uruchamiać MYC — jeden z najsilniejszych regulatorów wzrostu w nowotworach. Zrozumienie mechanizmu działania tego RNA może otworzyć nowe sposoby wykrywania i potencjalnego unieszkodliwiania groźnych guzów bez uszkadzania zdrowych tkanek. 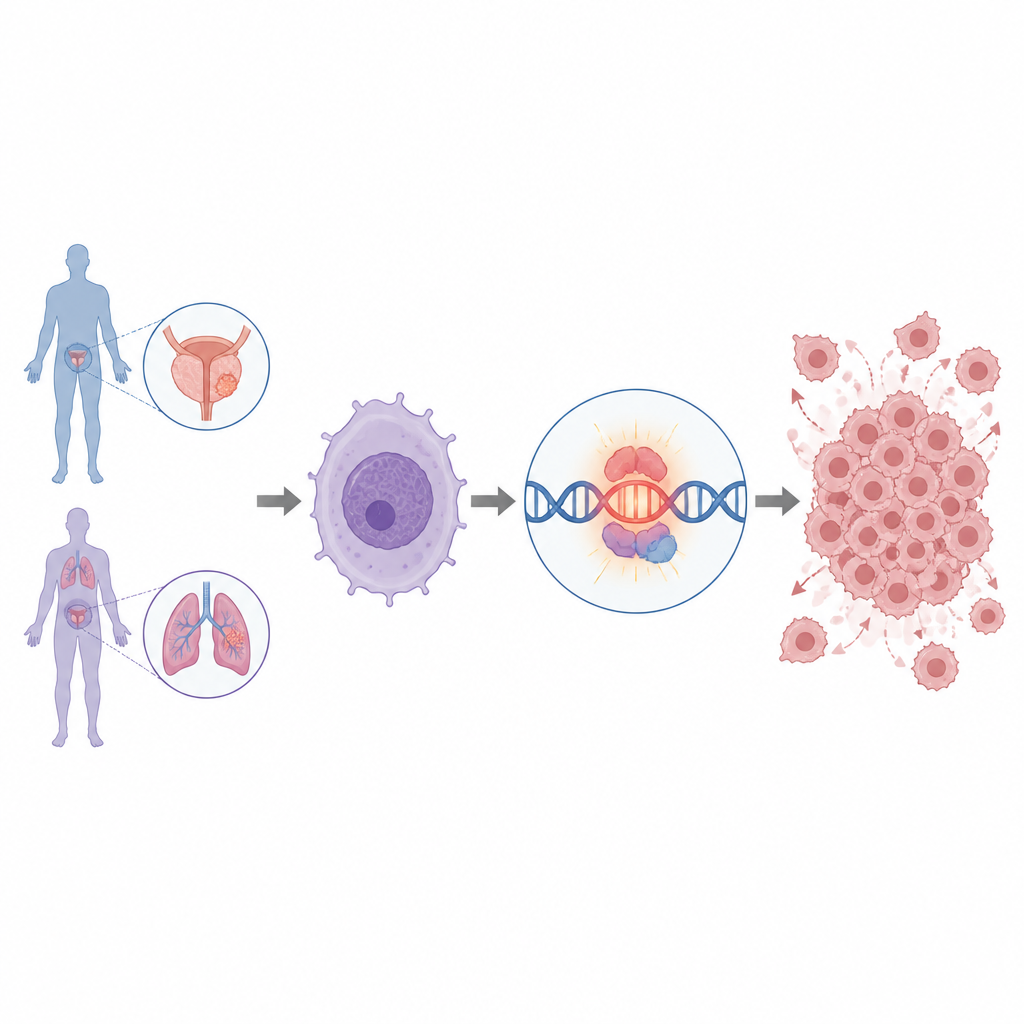
Sygnal zarezerwowany dla nowotworu w raku prostaty i płuca
Naukowcy zaczęli od przeszukania danych RNA od mężczyzn z zaawansowanym, opornym na leczenie rakiem prostaty. Skupili się na długich niekodujących RNA — klasie cząsteczek RNA, które nie kodują białek, ale mogą silnie wpływać na aktywność genów. Łącząc dane pacjentów z mapami regionów kontrolnych DNA zwanych super-wzmacniaczami, zidentyfikowali ponad tysiąc długich niekodujących RNA. Jedno z nich, nazwane IGF1R-AS1, wyróżniało się tym, że było ściśle powiązane z potężnym super-wzmacniaczem i aktywowało się prawie wyłącznie w guzach — szczególnie w zaawansowanym raku prostaty i w niektórych rakach płuca — podczas gdy w tkankach normalnych było niemal nieaktywne.
Od odkrycia RNA do zachowania nowotworu
Odkrycie RNA występującego tylko w guzie jest intrygujące, ale czy ma rzeczywiste znaczenie dla wzrostu nowotworu? Aby to przetestować, zespół użył narzędzi molekularnych do obniżenia poziomu IGF1R-AS1 w komórkach raka prostaty i płuca hodowanych w laboratorium. Po zablokowaniu tego RNA komórki rosły wolniej, poruszały się mniej i miały mniejszą zdolność inwazji przez barierę — wszystkie te cechy wskazują na zmniejszoną agresywność nowotworu. U myszy, którym przeszczepiono ludzkie komórki raka prostaty, guzy pozbawione IGF1R-AS1 rosły wolniej, a zwierzęta przeżywały dłużej. Eksperymenty te wykazały, że IGF1R-AS1 nie jest jedynie biernym obserwatorem, lecz pełni aktywną, sprzyjającą nowotworowi rolę.
Nowa droga włączania onkogenu MYC
Pogłębiając badania, naukowcy przyjrzeli się genom, aby zobaczyć, które geny zmieniają się po usunięciu IGF1R-AS1. Pojawił się wyraźny wzorzec: wiele genów regulowanych przez MYC zostało wyciszonych, a sam MYC spadł zarówno na poziomie RNA, jak i białka. Tymczasem sąsiedni gen IGF1R, znajdujący się obok IGF1R-AS1 w genomie, wykazywał niewielkie zmiany. To sugerowało, że IGF1R-AS1 nie działa jedynie lokalnie na sąsiada, jak robi to wiele podobnych RNA, lecz działa z dystansu, wzmacniając MYC — główny regulator podziału komórkowego. W tkankach pacjentów wysoka aktywność sieci genów związanych z IGF1R-AS1 oraz wysoka aktywność MYC korelowały z gorszym przeżyciem, szczególnie w zaawansowanym raku prostaty. 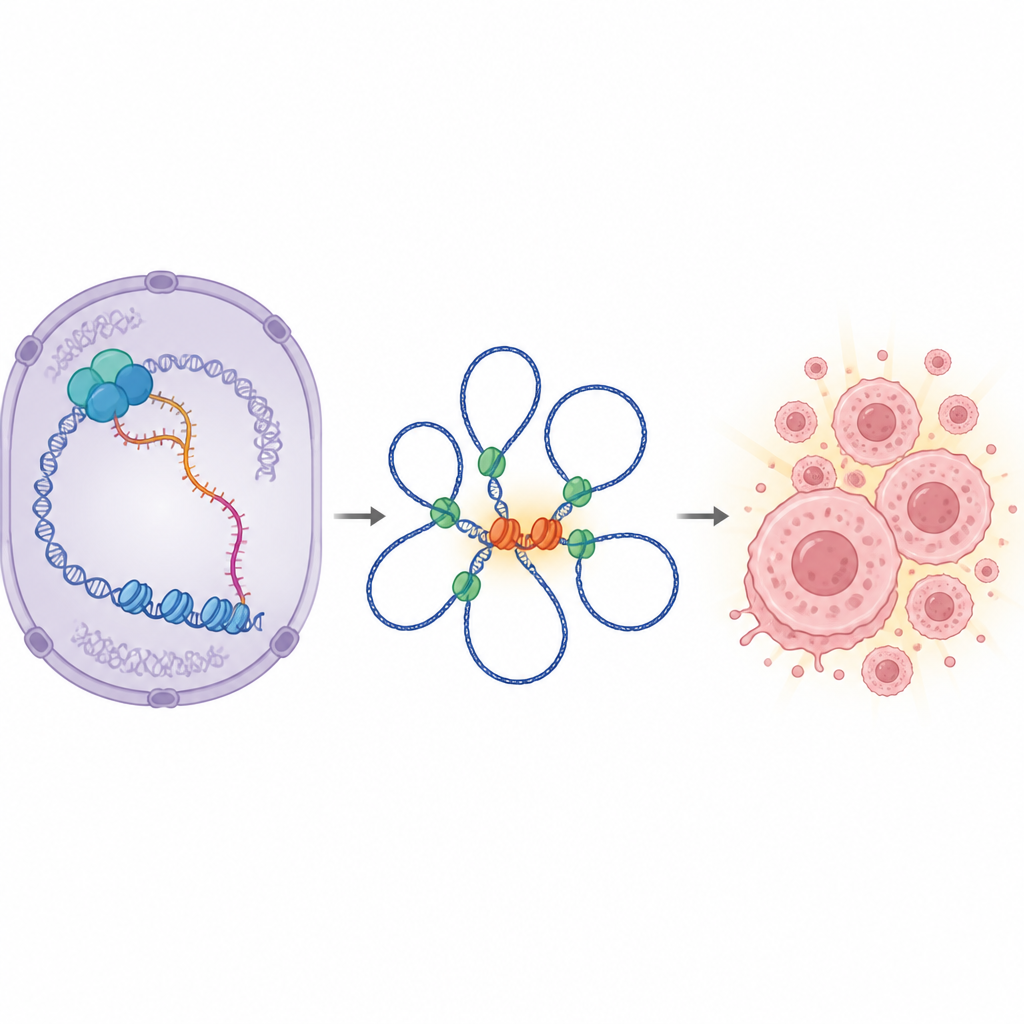
Modelowanie 3D genomu na korzyść wzrostu nowotworu
Jak cząsteczka RNA z odległego miejsca może zwiększać aktywność MYC? Odpowiedź leży w trójwymiarowym upakowaniu DNA w jądrze komórkowym. Zespół wykazał, że IGF1R-AS1 znajduje się głównie w jądrze i fizycznie wiąże białka remodelujące chromatynę (takie jak SMARCA4 i SMARCA1) oraz białko architektoniczne CTCF, które pomaga tworzyć pętle DNA. Te pętle zbliżają odległe regiony wzmacniające do genu MYC. Po obniżeniu poziomu IGF1R-AS1 wiele miejsc wzmacniających stało się mniej dostępnych, a długodystansowe pętle DNA łączące kluczowe węzły wzmacniaczy z promotorem MYC osłabły lub zanikły. W szczególności znany region wzmacniający w pobliżu innego RNA o nazwie CCAT1 stracił kontakt z MYC w komórkach raka prostaty zależnych od IGF1R-AS1. Dane wspierają model, w którym IGF1R-AS1 działa jak rusztowanie, ułatwiając współpracę remodelerów chromatyny i CTCF w utrzymywaniu pętli, które utrzymują MYC w stanie „włączonym”.
Dlaczego to ukryte RNA ma znaczenie dla pacjentów
Dla czytelników niebędących specjalistami główny wniosek jest taki: badanie ujawnia nowotworowo-specyficzne RNA, które pomaga przekształcać architekturę DNA w komórkach nowotworowych, utrzymując potężny gen wzrostu MYC w pozycji „włączonej”. Ponieważ IGF1R-AS1 jest w dużej mierze nieobecne w tkankach normalnych, a jednocześnie istotne dla wzrostu i rozprzestrzeniania się guza, może służyć jako marker identyfikujący nowotwory wysokiego ryzyka oraz jako potencjalny cel terapii selektywnie atakującej komórki nowotworowe. Szerzej rzecz biorąc, praca ta pokazuje, jak niekodujące RNA mogą organizować trójwymiarową strukturę genomu, wpływając na to, które geny są aktywne, i dodaje ważną warstwę do naszego zrozumienia powstawania i postępu nowotworów.
Cytowanie: Yang, Y., Wang, TY., Fry, J. et al. Tumor-specific lncRNA IGF1R-AS1 trans-regulates chromatin interactions associated with oncogenic MYC signaling. Nat Commun 17, 4171 (2026). https://doi.org/10.1038/s41467-026-70814-4
Słowa kluczowe: rak prostaty, długie niekodujące RNA, sygnalizowanie MYC, pętlowanie chromatyny, markery nowotworowe