Clear Sky Science · fr
Le lncRNA spécifique aux tumeurs IGF1R-AS1 régule en trans les interactions chromatiniennes associées à la signalisation oncogénique MYC
Comment un interrupteur ARN caché peut alimenter certains cancers
Pourquoi certains cancers de la prostate et du poumon croissent-ils si agressivement, et peut-on identifier des interrupteurs présents uniquement dans les cellules tumorales pour les contrôler ? Cette étude met au jour un fragment d’ARN jusque-là méconnu, presque exclusif aux tumeurs, qui semble contribuer à l’activation de MYC, l’un des moteurs de croissance les plus puissants en cancérologie. Comprendre le fonctionnement de cet ARN pourrait ouvrir de nouvelles voies pour détecter et éventuellement neutraliser des cancers dangereux sans endommager les tissus sains. 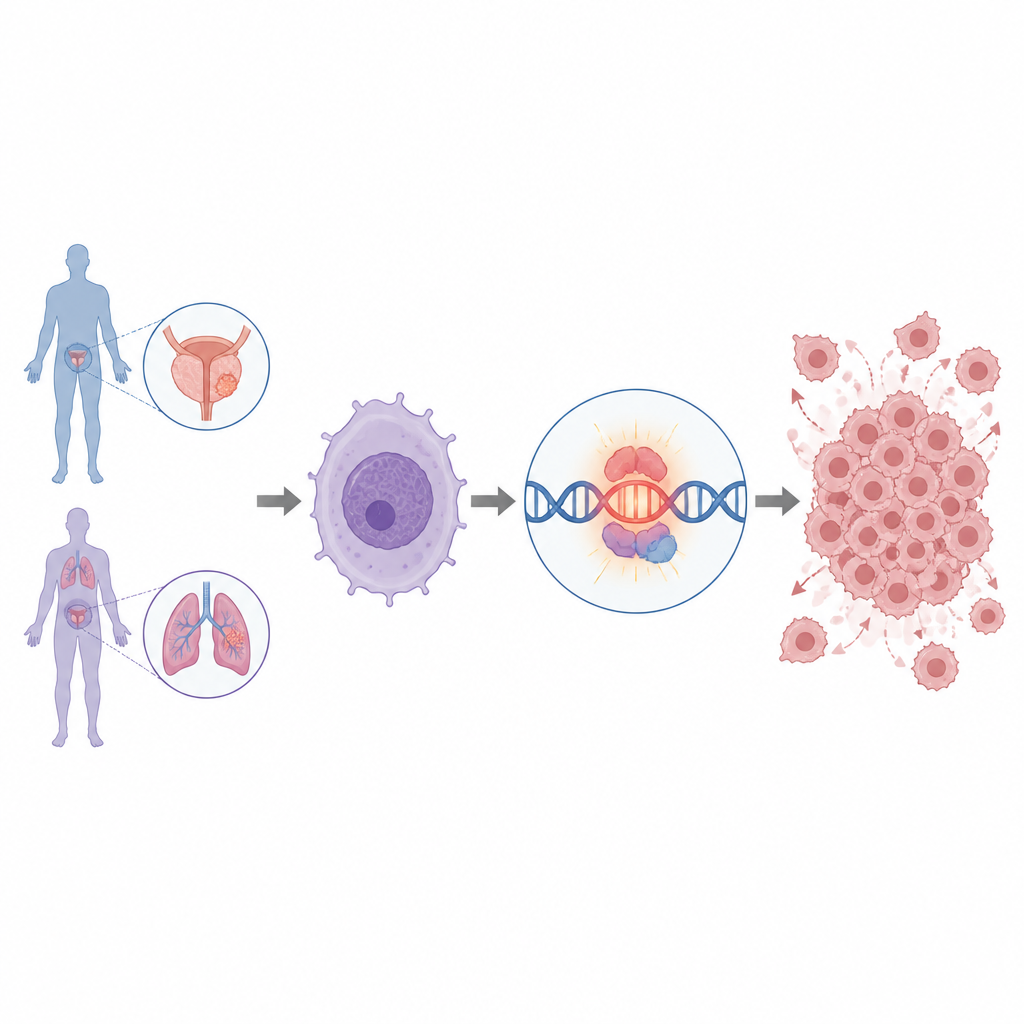
Un signal présent uniquement dans les tumeurs de la prostate et du poumon
Les chercheurs ont commencé par examiner des données d’ARN provenant d’hommes atteints d’un cancer de la prostate avancé et résistant au traitement. Ils se sont concentrés sur les ARN non codants longs, une classe d’ARN qui ne code pas pour des protéines mais peut fortement influencer l’expression génique. En combinant les données des patients avec des cartes des régions régulatrices de l’ADN appelées super-enhancers, ils ont identifié plus d’un millier d’ARN non codants longs. L’un d’eux, nommé IGF1R-AS1, s’est distingué car il était étroitement lié à un super-enhancer puissant et s’exprimait presque exclusivement dans les tumeurs, en particulier dans les cancers de la prostate avancés et certains cancers du poumon, tout en étant quasi silencieux dans les tissus normaux.
De la découverte d’un ARN à son impact sur le comportement tumoral
Découvrir un ARN spécifique aux tumeurs est intrigant, mais influence-t-il réellement la croissance cancéreuse ? Pour le tester, l’équipe a utilisé des outils moléculaires pour réduire les niveaux d’IGF1R-AS1 dans des lignées de cellules de cancer de la prostate et du poumon cultivées en laboratoire. Lors de l’inhibition de cet ARN, les cellules proliféraient moins, migraient moins et étaient moins capables d’envahir à travers une barrière, autant de signes d’une agressivité tumorale réduite. Chez des souris implantées avec des cellules humaines de cancer de la prostate, les tumeurs dépourvues d’IGF1R-AS1 croissaient plus lentement et les animaux survivaient plus longtemps. Ces expériences montrent qu’IGF1R-AS1 n’est pas un simple témoin, mais joue un rôle actif dans la promotion tumorale.
Une nouvelle voie pour activer l’oncogène MYC
En creusant davantage, les scientifiques ont observé quels gènes changeaient lorsque IGF1R-AS1 était supprimé. Un schéma net est apparu : de nombreux gènes régulés par MYC étaient réprimés, et MYC lui-même diminuait au niveau de l’ARN et de la protéine. En revanche, le gène voisin IGF1R, situé à côté d’IGF1R-AS1 dans le génome, changeait à peine. Cela signifie qu’IGF1R-AS1 n’agissait pas simplement sur son voisin immédiat, comme le font beaucoup d’ARN similaires. Au contraire, il agissait à distance pour stimuler MYC, un régulateur maître de la division cellulaire. Dans les tumeurs de patients, une forte activité du réseau génique lié à IGF1R-AS1 et une activité élevée de MYC étaient associées à une survie plus faible, surtout dans le cancer de la prostate avancé. 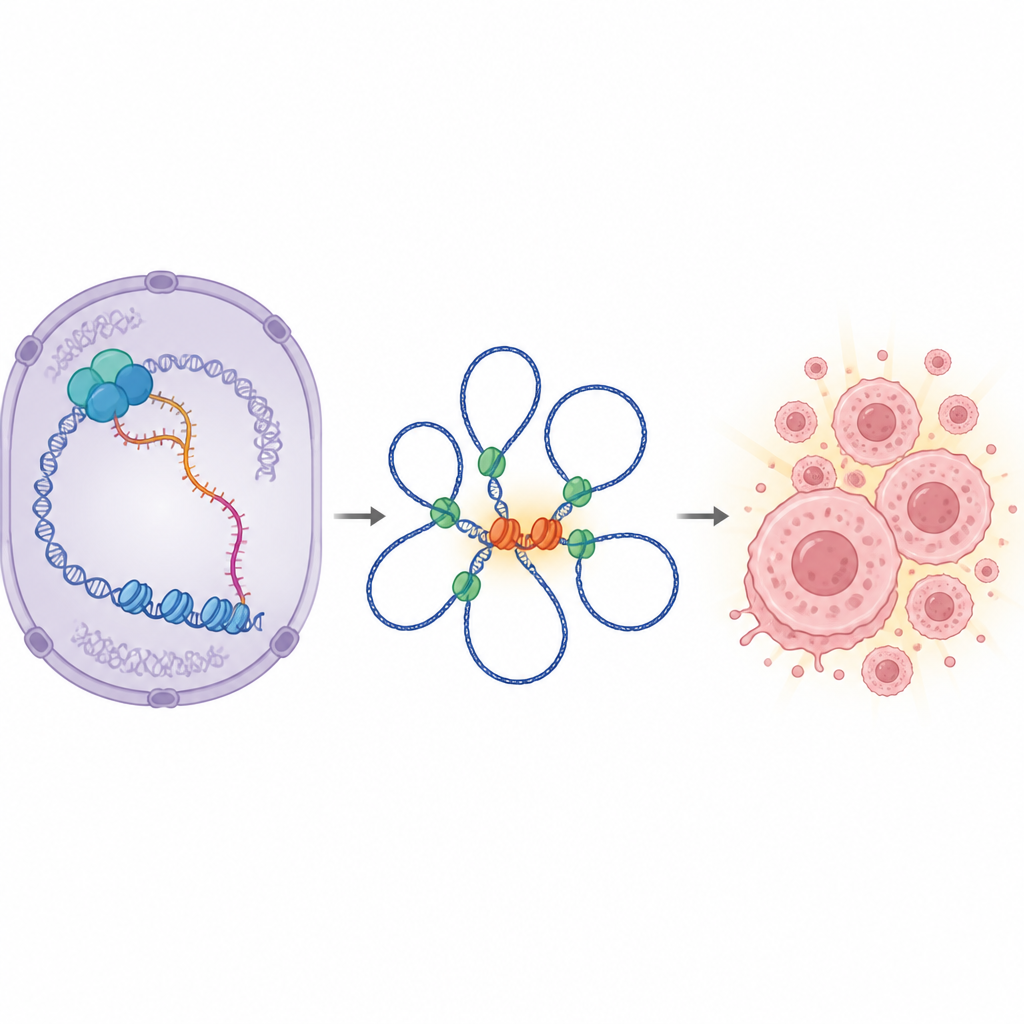
Façonner le génome 3D pour favoriser la croissance tumorale
Comment un ARN situé loin de MYC peut-il augmenter son activité ? La réponse réside dans le repliement tridimensionnel de l’ADN à l’intérieur du noyau. L’équipe a montré qu’IGF1R-AS1 se trouve principalement dans le noyau et se lie physiquement à des protéines remodelant la chromatine (telles que SMARCA4 et SMARCA1) et à la protéine architecturale CTCF, qui participe à la formation de boucles d’ADN. Ces boucles rapprochent des régions enhancers distantes du gène MYC. Lorsque IGF1R-AS1 était réduit, de nombreux sites enhanceurs devenaient moins accessibles, et des boucles d’ADN à longue portée qui connectent des hubs enhanceurs clés au promoteur de MYC s’affaiblissaient ou disparaissaient. En particulier, une région enhancere bien connue proche d’un autre ARN appelé CCAT1 perdait le contact avec MYC dans les cellules de prostate dépendantes d’IGF1R-AS1. Les données soutiennent un modèle dans lequel IGF1R-AS1 agit comme une échafaudage, aidant les remodelleurs de chromatine et CTCF à coopérer pour maintenir des boucles qui gardent MYC activé.
Pourquoi cet ARN caché compte pour les patients
Pour un public non spécialiste, l’essentiel est que cette étude révèle un ARN spécifique aux tumeurs qui contribue à remodeler l’architecture de l’ADN dans les cellules cancéreuses afin de maintenir un gène de croissance puissant, MYC, en position « activée ». Parce qu’IGF1R-AS1 est largement absent des tissus normaux mais important pour la croissance et la dissémination tumorales, il pourrait servir de marqueur pour identifier les cancers à haut risque et d’outil thérapeutique pour cibler sélectivement les cellules cancéreuses. Plus largement, ce travail montre comment les ARN non codants peuvent organiser la structure 3D du génome pour influencer l’activité génique, ajoutant une couche importante à notre compréhension de l’apparition et de la progression des cancers.
Citation: Yang, Y., Wang, TY., Fry, J. et al. Tumor-specific lncRNA IGF1R-AS1 trans-regulates chromatin interactions associated with oncogenic MYC signaling. Nat Commun 17, 4171 (2026). https://doi.org/10.1038/s41467-026-70814-4
Mots-clés: cancer de la prostate, ARN non codant long, signalisation MYC, bouclage de la chromatine, biomarqueurs tumoraux