Clear Sky Science · de
Tumorspezifische lncRNA IGF1R-AS1 reguliert trans-chromosomale Wechselwirkungen, die mit dem onkogenen MYC-Signalweg verbunden sind
Wie ein verborgenes RNA-Schalterchen bestimmte Krebserkrankungen antreiben könnte
Warum wachsen manche Prostata- und Lungenkrebse so aggressiv, und lassen sich Schalter finden, die nur in Tumorzellen existieren und sie kontrollieren? Diese Studie enthüllt ein zuvor unentdecktes RNA-Fragment, das fast ausschließlich in Tumoren vorkommt und offenbar dazu beiträgt, MYC einzuschalten — einen der stärksten Wachstumsförderer bei Krebs. Zu verstehen, wie diese RNA wirkt, könnte neue Wege eröffnen, gefährliche Tumoren zu erkennen und vielleicht gezielt zu schwächen, ohne gesundes Gewebe zu schädigen. 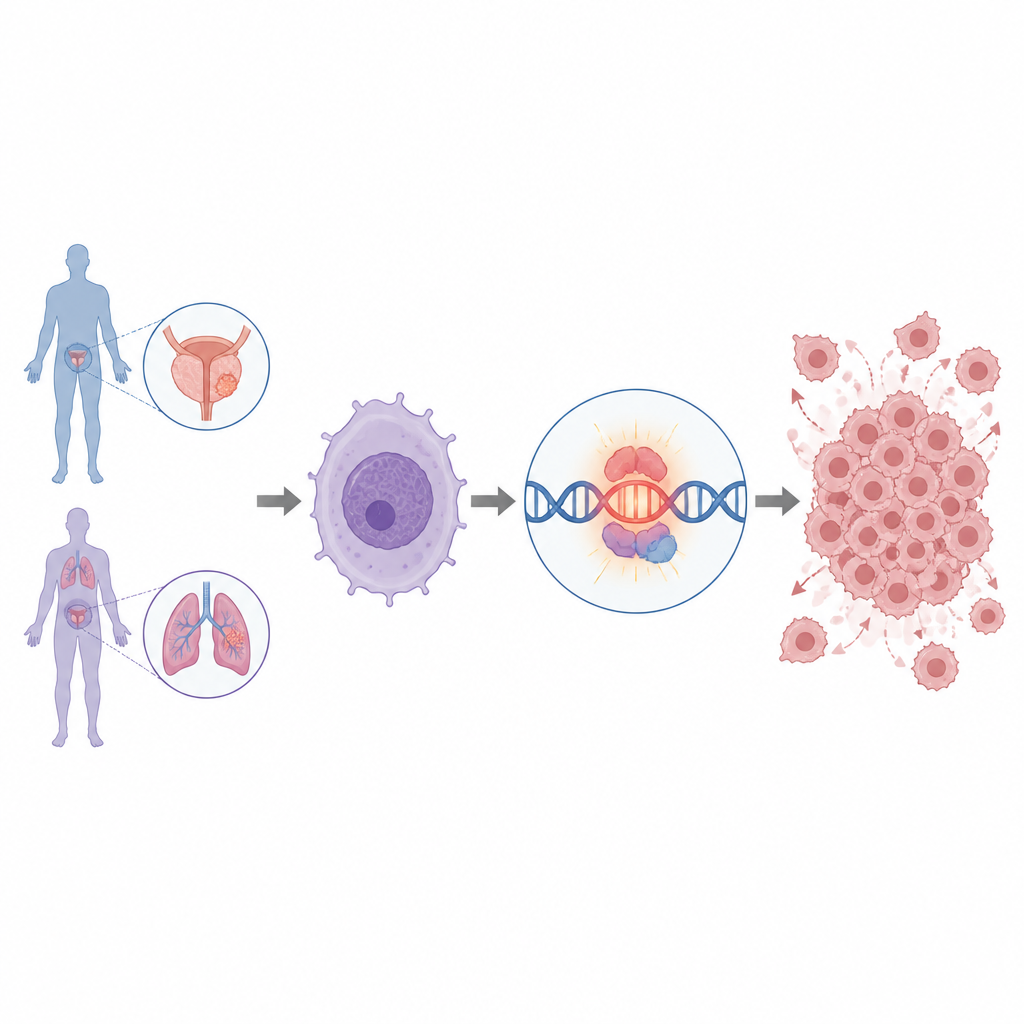
Ein tumorspezifisches Signal in Prostata- und Lungenkrebs
Die Forschenden begannen damit, RNA-Daten von Männern mit fortgeschrittenem, therapieresistentem Prostatakrebs zu durchforsten. Sie konzentrierten sich auf lange nicht-kodierende RNAs, eine Klasse von RNA-Molekülen, die keine Proteine produzieren, aber stark beeinflussen können, wie Gene reguliert werden. Durch die Verknüpfung von Patientendaten mit Karten von DNA-Regionskontrollen, sogenannten Super-Enhancern, identifizierten sie mehr als tausend lange nicht-kodierende RNAs. Eine davon, IGF1R-AS1 genannt, fiel besonders auf, weil sie eng mit einem mächtigen Super-Enhancer verbunden war und nahezu ausschließlich in Tumoren aktiviert war — insbesondere im fortgeschrittenen Prostatakrebs und in einigen Lungenkrebsen — während sie in normalem Gewebe nahezu stillgelegt war.
Von der RNA-Entdeckung zum Krebsverhalten
Eine nur im Tumor vorkommende RNA zu finden ist spannend, aber hat sie wirklich Bedeutung für das Tumorwachstum? Um das zu prüfen, verwendete das Team molekulare Werkzeuge, um IGF1R-AS1 in in vitro kultivierten Prostata- und Lungenkrebszellen zu reduzieren. Nach Herunterregulierung dieser RNA wuchsen die Zellen langsamer, bewegten sich weniger und waren weniger invasiv — typische Merkmale verminderter Tumoraggressivität. In Mäusen, die mit menschlichen Prostatakrebszellen transplantiert wurden, wuchsen Tumore ohne IGF1R-AS1 langsamer und die Tiere überlebten länger. Diese Experimente zeigten, dass IGF1R-AS1 nicht nur ein Beiwerk ist, sondern eine aktive, tumorfördernde Rolle spielt.
Ein neuer Weg, das Onkogen MYC einzuschalten
Bei näherer Untersuchung schauten die Wissenschaftlerinnen und Wissenschaftler, welche Gene sich veränderten, wenn IGF1R-AS1 entfernt wurde. Ein klares Muster zeigte sich: Viele MYC-gesteuerte Gene waren herunterreguliert, und MYC selbst sank sowohl auf RNA- als auch auf Proteinebene. Das in der Nähe liegende IGF1R-Gen, das adjazent zu IGF1R-AS1 im Genom sitzt, blieb dagegen weitgehend unverändert. Das deutete darauf hin, dass IGF1R-AS1 nicht einfach sein Nachbargen feinjustiert, wie viele ähnliche RNAs, sondern aus der Distanz MYC stärkt — einen zentralen Regulator der Zellteilung. In Patiententumoren korrelierten hohe Aktivität des IGF1R-AS1-gebundenen Gen-Netzwerks und hohe MYC-Aktivität mit schlechterer Überlebensprognose, besonders beim fortgeschrittenen Prostatakrebs. 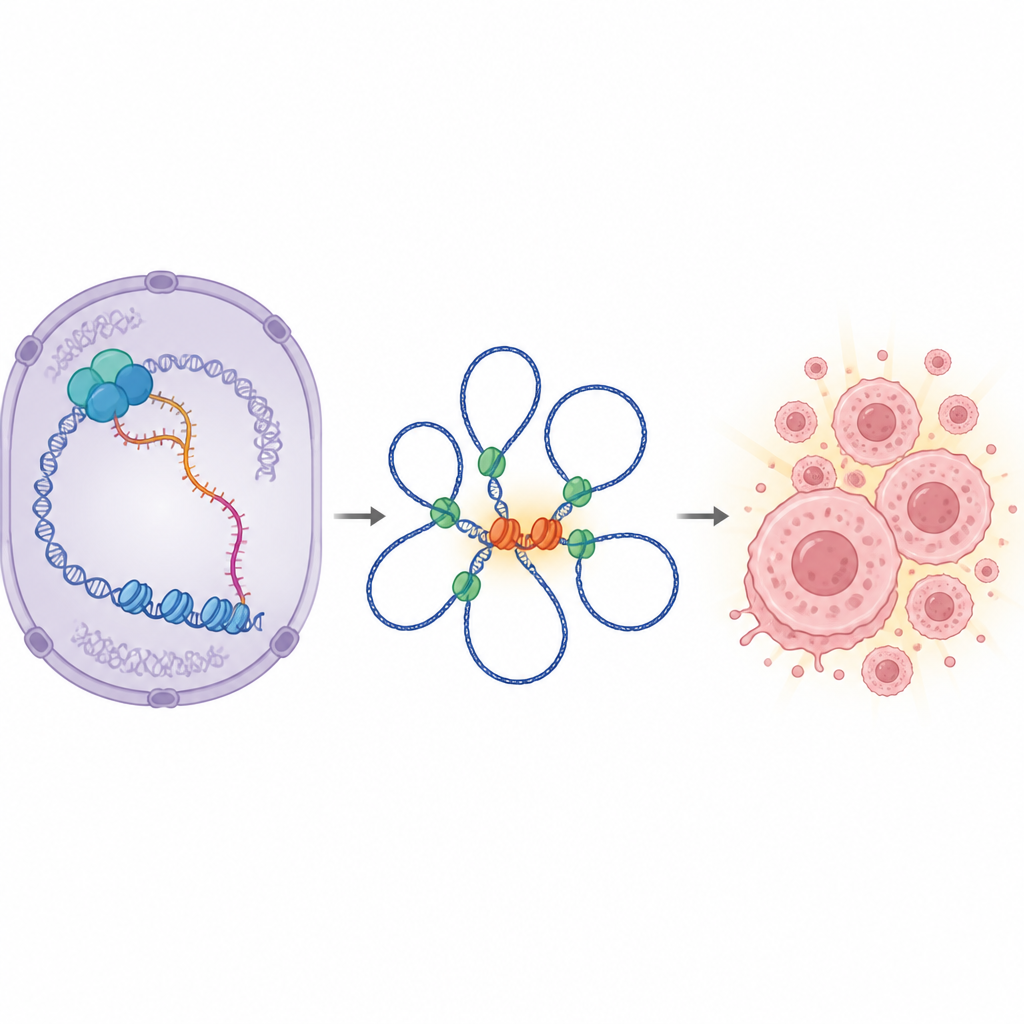
Die 3D-Genomstruktur so formen, dass Krebs profitiert
Wie kann ein weit entferntes RNA-Molekül MYC stärker ankurbeln? Die Antwort liegt in der dreidimensionalen Faltung der DNA im Zellkern. Das Team zeigte, dass IGF1R-AS1 überwiegend im Zellkern lokalisiert und physisch an Chromatin-Remodelling-Proteine (etwa SMARCA4 und SMARCA1) sowie an das architektonische Protein CTCF bindet, das beim Bilden von DNA-Schleifen hilft. Diese Schleifen bringen entfernte Enhancer-Regionen in Kontakt mit dem MYC-Gen. Wenn IGF1R-AS1 reduziert wurde, wurden viele Enhancer-Stellen weniger zugänglich, und langreichweitige DNA-Schleifen, die zentrale Enhancer-Hubs mit dem MYC-Promotor verbinden, schwächten sich oder verschwanden. Besonders eine bekannte Enhancer-Region in der Nähe einer anderen RNA namens CCAT1 verlor den Kontakt zu MYC in Prostatakrebszellen, die von IGF1R-AS1 abhängig sind. Die Daten stützen ein Modell, in dem IGF1R-AS1 wie ein Gerüst wirkt und Chromatin-Remodeller und CTCF kooperieren lässt, um Schleifen aufrechtzuerhalten, die MYC eingeschaltet halten.
Warum diese verborgene RNA für Patientinnen und Patienten wichtig ist
Für Leserinnen und Leser ohne Fachwissen lautet die Kernbotschaft: Die Studie zeigt eine tumorspezifische RNA, die die DNA-Architektur in Krebszellen umgestaltet, sodass ein mächtiges Wachstumsgen, MYC, dauerhaft aktiviert bleibt. Da IGF1R-AS1 in normalem Gewebe weitgehend fehlt, aber für Tumorwachstum und -ausbreitung wichtig ist, könnte sie sowohl als Marker zur Identifikation von Hochrisiko-Tumoren dienen als auch als potenzielles Ziel für Therapien, die selektiv Krebszellen angreifen. Allgemeiner veranschaulicht die Arbeit, wie nicht-kodierende RNAs die 3D-Struktur des Genoms organisieren können, um zu bestimmen, welche Gene aktiv sind — und fügt damit eine wichtige neue Ebene zum Verständnis von Entstehung und Fortschreiten von Krebs hinzu.
Zitation: Yang, Y., Wang, TY., Fry, J. et al. Tumor-specific lncRNA IGF1R-AS1 trans-regulates chromatin interactions associated with oncogenic MYC signaling. Nat Commun 17, 4171 (2026). https://doi.org/10.1038/s41467-026-70814-4
Schlüsselwörter: Prostatakrebs, lange nicht-kodierende RNA, MYC-Signalweg, Chromatin-Looping, Tumor-Biomarker