Clear Sky Science · sv
Strukturen hos en pH-känslig pentamer ligandstyrd jonkanal från skabbdjuret Sarcoptes scabiei
Varför små kvalster och deras dolda brytare spelar roll
Skabb är en vanlig men ofta förbisedd hudsjukdom som ger intensiv klåda och kan leda till allvarliga komplikationer om den inte behandlas. Den orsakas av det mikroskopiska kvalstret Sarcoptes scabiei, och läkare förlitar sig i stor utsträckning på läkemedlet ivermektin för att kontrollera den. Tecken på växande läkemedelsresistens håller dock på att visa sig. Denna studie avslöjar den detaljerade 3D-strukturen och beteendet hos ett nyckelprotein i kvalstrets nervsystem — en pH-känslig kloridkanal kallad SsCl — och visar exakt hur ivermektin interagerar med den. Genom att förstå denna molekylära brytare hoppas forskare kunna utforma nästa generations behandlingar som förblir effektiva även när resistens ökar.
En särskild jonkanal i en besvärlig parasit
SsCl tillhör en familj proteiner som bildar porer, eller kanaler, över cellmembran för att låta laddade partiklar passera in och ut. Dessa jonrörelser ligger till grund för elektrisk signalering i nerver och muskler. Till skillnad från klassiska receptorer som svarar på specifika kemiska budbärare reagerar SsCl på förändringar i surhetsgraden eller alkaliniteten (pH) runt cellen. När omgivningen blir mer alkalisk öppnar SsCl normalt och släpper igenom kloridjoner, vilket hjälper kvalstrets celler att bibehålla balans och kommunicera. Eftersom pH-känsliga kloridkanaler huvudsakligen finns i ryggradslösa djur är de attraktiva mål för läkemedel som dödar parasiter utan att skada människor. Ändå visste forskare fram till nu inte hur SsCl känner av pH eller hur ivermektin förändrar dess aktivitet.
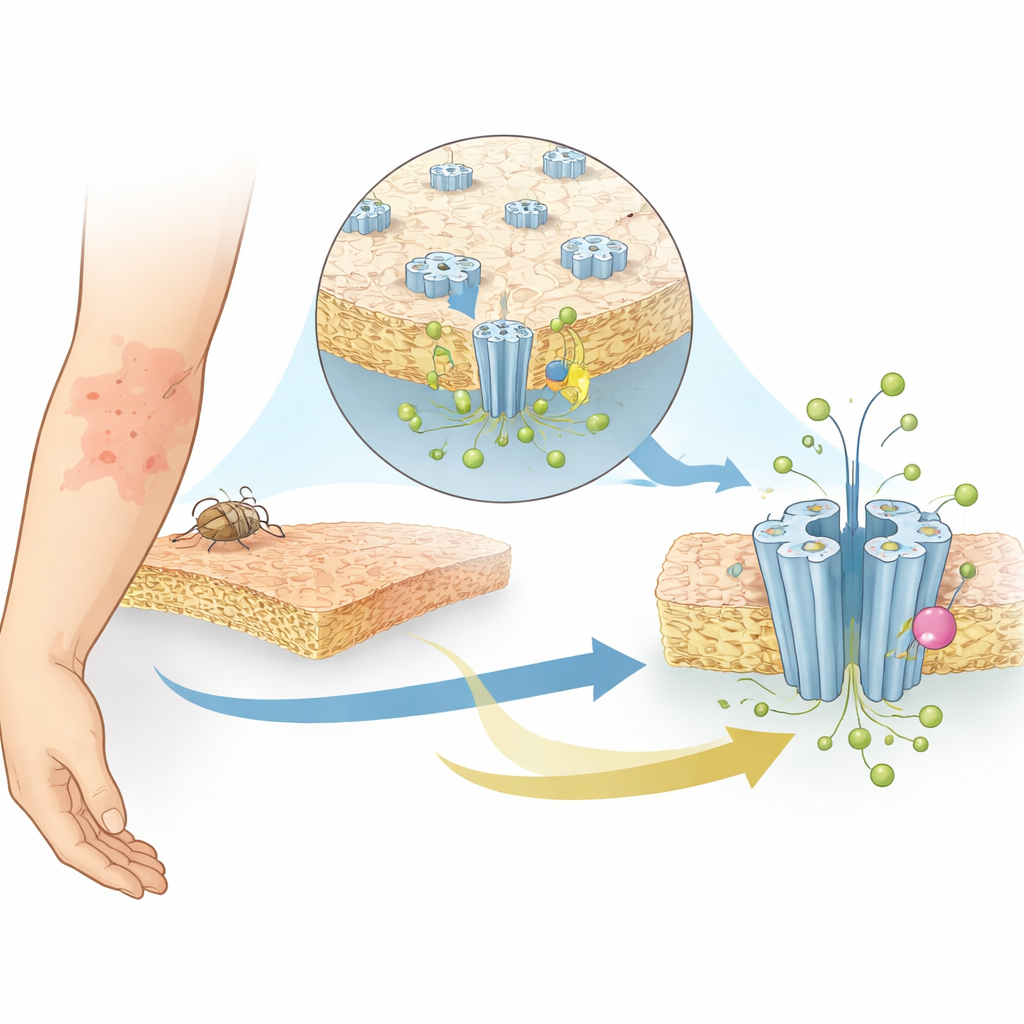
Fånga kanalen i arbete med kryo-EM
Forskarna använde single-particle kryo-elektronmikroskopi, en teknik som blixtfryser proteiner och avbildar dem i nära atomupplösning, för att fånga SsCl i fyra olika former, eller tillstånd. De studerade kanalen vid ett svagt surt pH (6,5), där den är stängd, och vid ett mer basiskt pH (9), där den borde vara aktiv men istället antar en ”desensitiserad” form som inte längre leder joner efter långvarig stimulering. De bestämde också strukturer av SsCl vid båda pH-nivåerna i närvaro av ivermektin. I samtliga fall bildar proteinet en femdelad ring som formar en central por. Överraskande nog antar poren i de stängda och desensitiserade tillstånden en timglasliknande form, med den smalaste punkten i mitten av membranet — mer likt kanaler som leder positivt laddade joner än andra kända kloridkanaler.
Hur pH och ivermektin omformar poren
Genom att mäta porens storlek i varje struktur kunde gruppen koppla form till funktion. Vid pH 6,5 utan läkemedel är den centrala förträngningen för smal för att kloridjoner ska kunna passera, vilket stämmer med det icke-ledande tillståndet. Vid pH 9 utan läkemedel är poren fortfarande för trång i mitten, även om omgivningen normalt skulle gynna kanalöppning. Denna konfiguration tolkas som ett desensitiserat tillstånd som uppstår efter långvarig exponering för basiska förhållanden. När ivermektin kilas in mellan segment av intilliggande subenheter i den membranövergående regionen lirkas helixarna isär och poren vidgas. Vid pH 6,5 skapar denna expansion en delvis öppen väg som fortfarande begränsar jonflödet nära selektivitetsfiltret i porens botten, i linje med läkemedlets långsamma och måttliga aktivering av kanalen. Vid pH 9 med ivermektin blir poren tillräckligt vid längs större delen av sin längd för att stödja robust kloridledning, vilket överensstämmer med starka elektriska strömmar som registrerats i funktionella experiment.
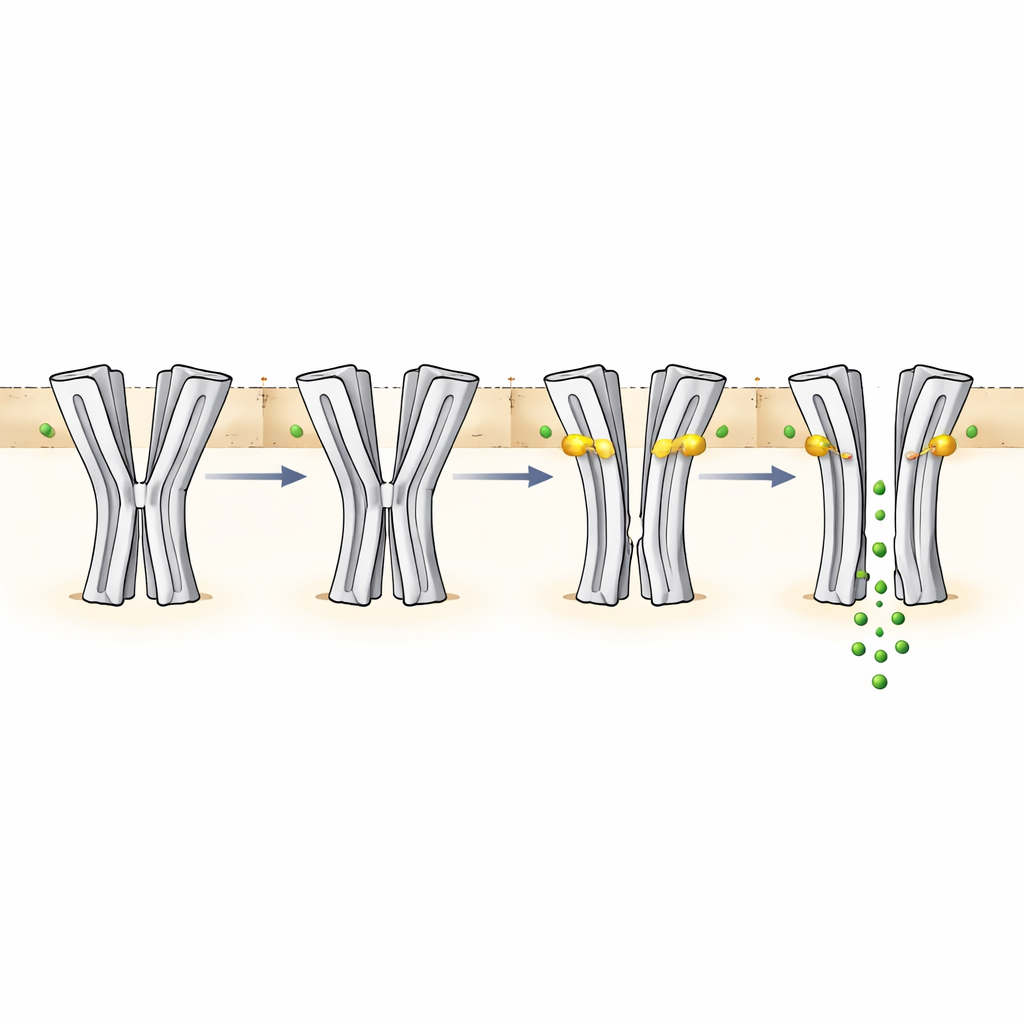
Den dolda pH-sensorn och ett bredare kontrollnätverk
För att kunna peka ut hur SsCl känner av pH kombinerade författarna beräkningsbaserade förutsägelser med strukturella jämförelser och mutagenes. De identifierade en klunga aminosyror — särskilt flera histidiner och glutaminsyror — i den yttre, vattenexponerade delen av proteinet, nära en region som i släktingreceptorer vanligtvis binder kemiska budbärare. Ett nyckelpar, en histidin (H206) och en glutaminsyra (E146), kan bilda eller bryta ett joniskt bind depending på pH. Vid lägre pH hjälper detta bind att låsa vissa strukturella element på plats; vid högre pH försvagas bindningen och tillåter en subtil vridning i detta område att fortplantas ned till de membranövergående helixarna som bildar poren. Mutation av H206 eller E146 ändrade det pH-intervall över vilket kanalen aktiveras, medan dubbelmutationer kunde störa pH-känsligheten men ändå låta ivermektin utlösa strömmar. Ytterligare rester nära en flexibel slinga vid kanalens mynning påverkade också hur proteinet svarar på pH-förändringar, vilket stöder idén om ett distribuerat pH-känsornätverk snarare än en enda av-och-på-brytare.
Från molekylär insikt till bättre skabbbehandlingar
Sammanfattningsvis visar arbetet hur en skabbkvalsters jonkanal känner av sin kemiska omgivning och hur ivermektin stabiliserar särskilda kanaltillstånd för att främja eller förstärka öppning. SsCl visar sig vara en ovanlig kloridkanal vars desensitiserade form liknar den hos kanaler för positivt laddade joner och vars laddningsfördelning längs poren är fint inställd för att leda kloridjoner. Genom att lösa kanalens strukturer i flera funktionella tillstånd och kartlägga de rester som justerar pH- och läkemedelskänslighet ger studien en ritning för att designa nya antiparasitära föreningar. Dessa nästa generations läkemedel skulle kunna fästa vid liknande platser eller utnyttja samma pH-sensormekanismer, vilket erbjuder nya alternativ för att bekämpa skabb i en värld där nuvarande behandlingar i allt högre grad riskerar att förlora sin effekt.
Citering: Kleiz-Ferreira, J., Brams, M., Harrison, P.J. et al. Structure of a pH-sensitive pentameric ligand-gated ion channel from the Sarcoptes scabies mite. Nat Commun 17, 3392 (2026). https://doi.org/10.1038/s41467-026-70575-0
Nyckelord: skabb, jonkanaler, ivermektin, kryo-elektronmikroskopi, parasitreducering