Clear Sky Science · pt
Estrutura de um canal iônico pentamérica sensível ao pH do ácaro Sarcoptes scabiei
Por que ácaros minúsculos e seus interruptores ocultos importam
A sarna é uma doença de pele comum, mas frequentemente negligenciada, que causa coceira intensa e pode levar a complicações graves se não tratada. É causada pelo minúsculo ácaro Sarcoptes scabiei, e os médicos dependem fortemente do fármaco ivermectina para controlá‑la. No entanto, há sinais de crescente resistência ao medicamento. Este estudo revela a estrutura 3D detalhada e o comportamento de uma proteína-chave no sistema nervoso do ácaro — um canal de cloreto sensível ao pH chamado SsCl — e mostra exatamente como a ivermectina interage com ele. Ao entender esse interruptor molecular, os cientistas esperam projetar tratamentos de nova geração que permaneçam eficazes mesmo com o aumento da resistência.
Um canal iônico especial em um parasita problemático
O SsCl pertence a uma família de proteínas que formam poros, ou canais, através das membranas celulares para permitir a passagem de partículas carregadas. Esses movimentos de íons sustentam a sinalização elétrica em nervos e músculos. Ao contrário de receptores clássicos que respondem a mensageiros químicos específicos, o SsCl responde a mudanças na acidez ou alcalinidade (pH) ao redor da célula. Quando o ambiente se torna mais alcalino, o SsCl normalmente se abre para permitir o fluxo de íons cloreto, ajudando as células do ácaro a manter o equilíbrio e a comunicar‑se. Como canais de cloreto sensíveis ao pH são encontrados principalmente em invertebrados, eles são alvos atraentes para drogas que eliminem parasitas sem prejudicar humanos. Ainda assim, até agora os cientistas não sabiam como o SsCl detecta o pH nem como a ivermectina altera sua atividade.
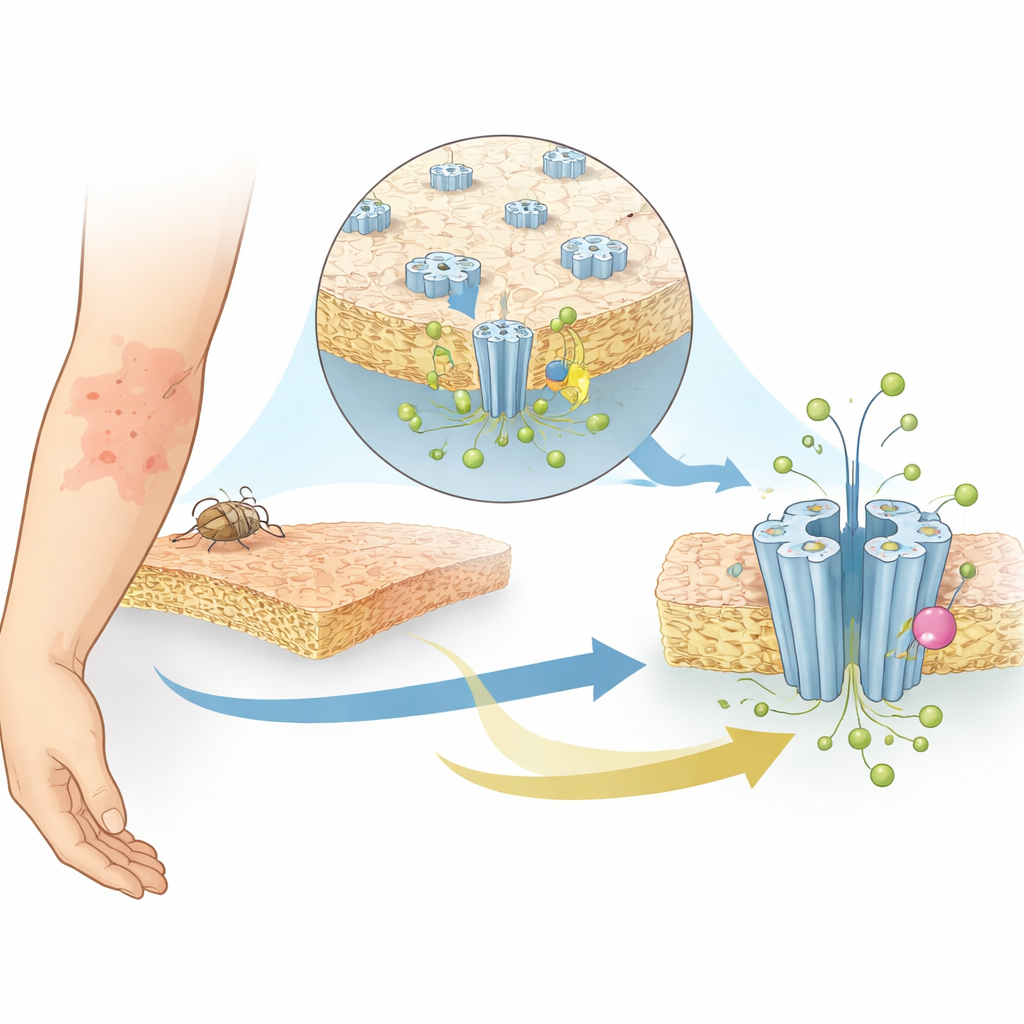
Capturando o canal em ação com cryo‑EM
Os pesquisadores usaram criomicroscopia eletrônica de partículas isoladas, uma técnica que congela rapidamente proteínas e as imagina em resolução quase atômica, para capturar o SsCl em quatro formas diferentes, ou estados. Estudaram o canal em pH levemente ácido (6,5), onde ele está fechado, e em pH mais alcalino (9), onde deveria estar ativo, mas assume em vez disso uma forma “dessensibilizada” que não conduz íons após estimulação prolongada. Também determinaram as estruturas do SsCl em ambos os níveis de pH na presença de ivermectina. Em todos os casos, a proteína se monta como um anel de cinco partes formando um poro central. Surpreendentemente, o poro nos estados fechado e dessensibilizado adota uma forma de ampulheta, com o ponto mais estreito no meio da membrana — mais reminiscentes de canais que conduzem íons positivamente carregados do que de outros canais de cloreto conhecidos.
Como o pH e a ivermectina remodelam o poro
Ao medir o tamanho do poro em cada estrutura, a equipe pôde relacionar forma e função. Em pH 6,5 sem droga, a constrição central é estreita demais para a passagem de íons cloreto, compatível com o estado não condutor. Em pH 9 sem droga, o poro ainda está demasiado apertado no meio, embora o ambiente normalmente favoreça a abertura do canal. Essa configuração é interpretada como um estado dessensibilizado que resulta da exposição prolongada a condições alcalinas. Quando a ivermectina se aloja entre segmentos de subunidades vizinhas na região transmembrana, ela afasta as hélices e alarga o poro. Em pH 6,5, essa expansão cria um caminho parcialmente aberto que ainda restringe o fluxo de íons perto do filtro de seletividade na base do poro, consistente com a ativação lenta e modesta promovida pela droga. Em pH 9 com ivermectina, o poro torna‑se suficientemente largo ao longo da maior parte de seu comprimento para suportar uma condução robusta de cloreto, em consonância com fortes correntes elétricas registradas em experimentos funcionais.
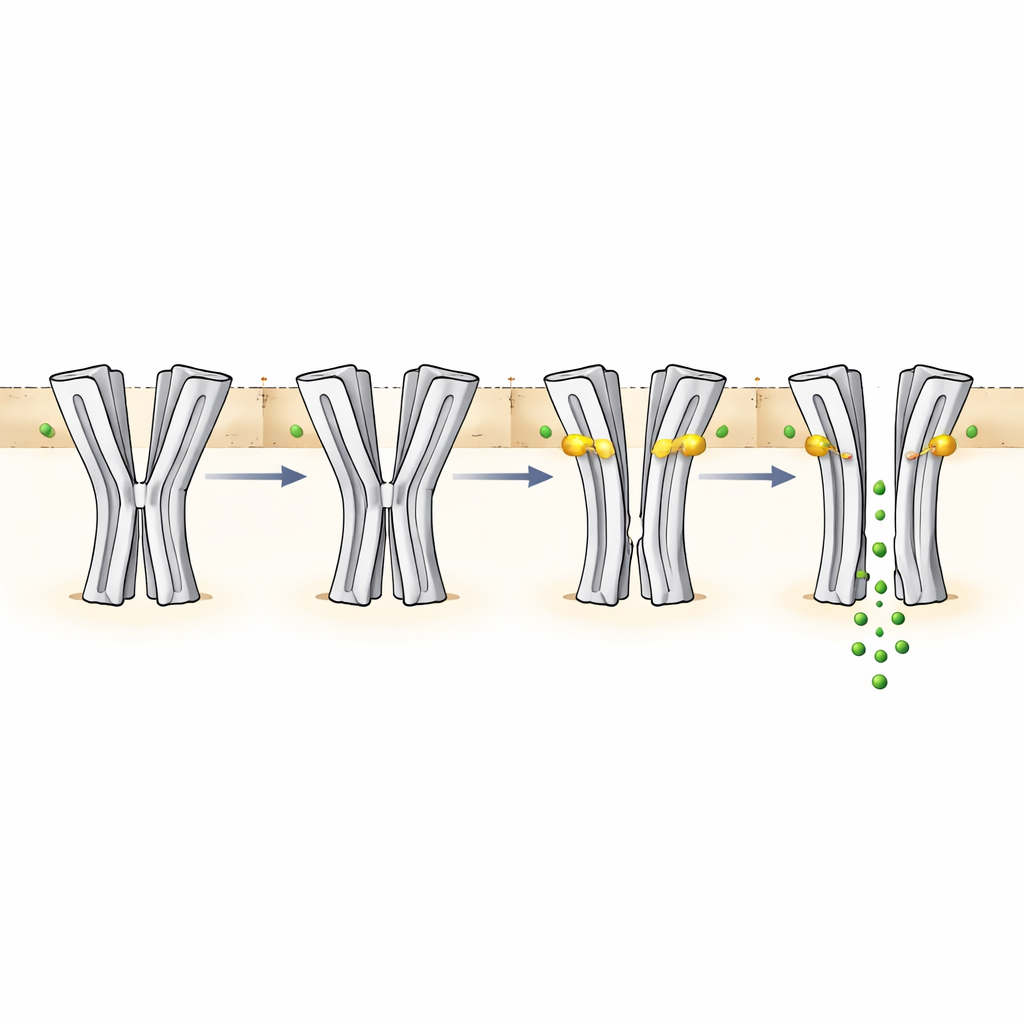
O sensor oculto de pH e uma rede de controle mais ampla
Para localizar como o SsCl detecta o pH, os autores combinaram previsões computacionais com comparações estruturais e mutagênese. Identificaram um aglomerado de aminoácidos — particularmente várias histidinas e ácidos glutâmicos — na parte externa exposta à água da proteína, perto de uma região que em receptores relacionados normalmente liga mensageiros químicos. Um par chave, uma histidina (H206) e um ácido glutâmico (E146), pode formar ou romper uma ligação iônica dependendo do pH. Em pH mais baixo, essa ligação ajuda a travar certos elementos estruturais; em pH mais alto, a ligação enfraquece, permitindo que uma torção sutil nessa área se propague até as hélices transmembrana que formam o poro. Mutar H206 ou E146 alterou a faixa de pH na qual o canal é ativado, enquanto mutações duplas podiam perturbar a sensibilidade ao pH e ainda permitir que a ivermectina provocasse correntes. Resíduos adicionais perto de uma alça flexível na entrada do canal também influenciaram como a proteína responde a mudanças de pH, sustentando a ideia de uma rede de detecção de pH distribuída em vez de um único interruptor liga‑desliga.
Do insight molecular a melhores tratamentos para a sarna
De modo geral, o trabalho mostra como um canal iônico do ácaro da sarna detecta seu ambiente químico e como a ivermectina estabiliza formas particulares do canal para promover ou reforçar a abertura. O SsCl revela‑se um canal de cloreto incomum cuja forma dessensibilizada se assemelha à de canais para íons positivamente carregados e cuja distribuição de cargas ao longo do poro é finamente ajustada para guiar íons cloreto. Ao resolver as estruturas do canal em múltiplos estados funcionais e mapear os resíduos que ajustam a sensibilidade ao pH e ao fármaco, o estudo fornece um roteiro para projetar novos compostos antiparasitários. Esses medicamentos de próxima geração poderiam ligar‑se a sítios semelhantes ou explorar a mesma maquinaria sensora de pH, oferecendo opções renovadas para combater a sarna em um mundo onde os tratamentos atuais correm crescente risco de perder eficácia.
Citação: Kleiz-Ferreira, J., Brams, M., Harrison, P.J. et al. Structure of a pH-sensitive pentameric ligand-gated ion channel from the Sarcoptes scabies mite. Nat Commun 17, 3392 (2026). https://doi.org/10.1038/s41467-026-70575-0
Palavras-chave: sarna, canais iônicos, ivermectina, criomicroscopia eletrônica, controle de parasitas