Clear Sky Science · nl
Structuur van een pH-gevoelige pentamere ligand-gestuurde ionenpoort van de Sarcoptes scabiei-mijt
Waarom piepkleine mijten en hun verborgen schakelaars ertoe doen
Schurft is een veelvoorkomende maar vaak over het hoofd geziene huidaandoening die intense jeuk veroorzaakt en, als ze onbehandeld blijft, tot ernstige complicaties kan leiden. Ze wordt veroorzaakt door de microscopische mijt Sarcoptes scabiei, en artsen steunen sterk op het middel ivermectine om de aandoening te bestrijden. Er verschijnen echter aanwijzingen voor toenemende resistentie tegen geneesmiddelen. Deze studie onthult de gedetailleerde 3D-structuur en het gedrag van een sleutelproteïne in het zenuwstelsel van de mijt — een pH-gevoelig chloridekanaal dat SsCl wordt genoemd — en toont precies hoe ivermectine ermee interageert. Door deze moleculaire schakelaar te begrijpen, hopen wetenschappers behandelmethoden van de volgende generatie te ontwerpen die effectief blijven, zelfs als resistentie toeneemt.
Een speciaal ionenkanaal in een lastige parasiet
SsCl behoort tot een familie van eiwitten die poriën, of kanalen, in celmembranen vormen om geladen deeltjes in en uit te laten. Deze ionenbewegingen liggen ten grondslag aan elektrische signalering in zenuwen en spieren. In tegenstelling tot klassieke receptoren die op specifieke chemische boodschappers reageren, reageert SsCl op veranderingen in zuurgraad of alkaliteit (pH) rondom de cel. Wanneer de omgeving meer basisch wordt, opent SsCl normaal gesproken om chloride-ionen te laten stromen, wat de cellen van de mijt helpt balans te houden en te communiceren. Omdat pH-gevoelige chloridekanalen voornamelijk in ongewervelden voorkomen, zijn ze aantrekkelijke doelwitten voor middelen die parasieten doden zonder de mens te schaden. Tot nu toe wisten wetenschappers echter niet hoe SsCl pH waarneemt of hoe ivermectine zijn activiteit verandert.
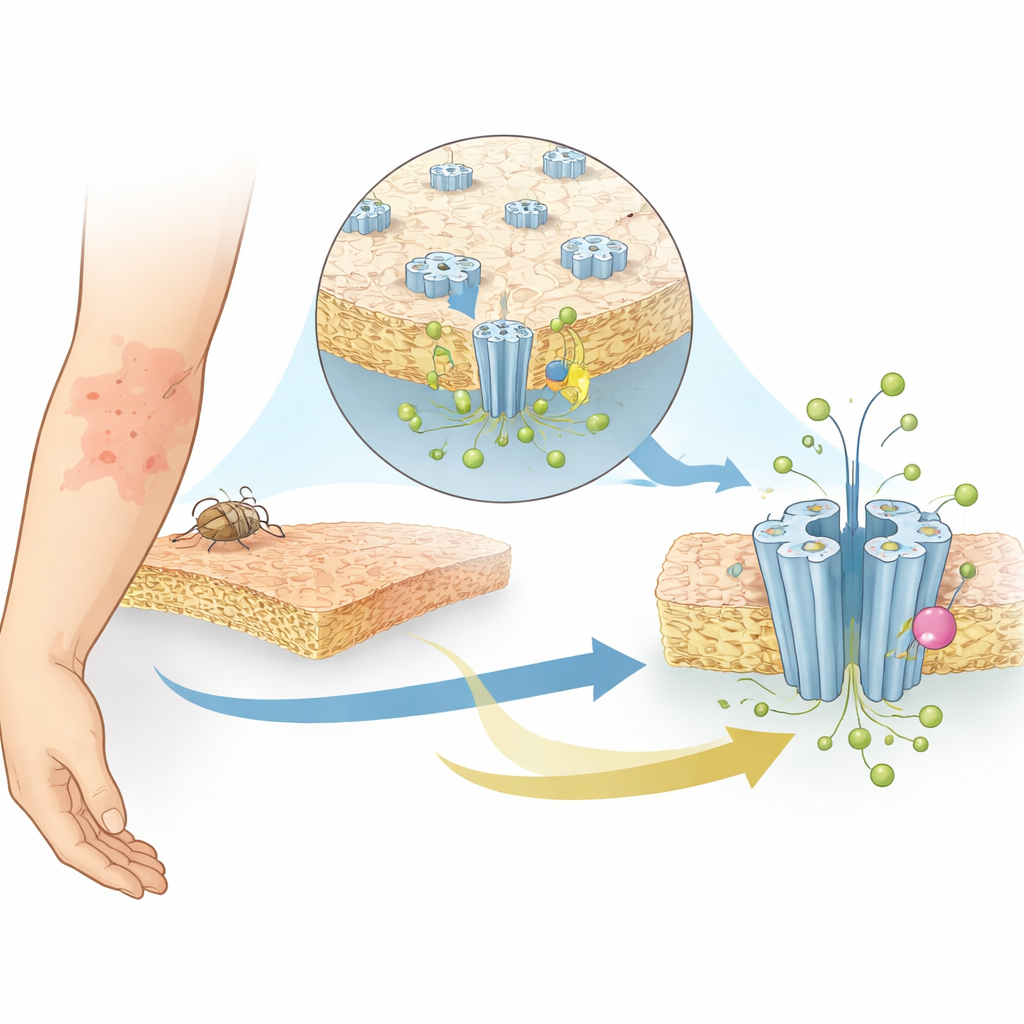
Het kanaal vastleggen in actie met cryo-EM
De onderzoekers gebruikten single-particle cryo-elektronenmicroscopie, een techniek die eiwitten snel invriest en ze afbeeldt op bijna-atomaire resolutie, om SsCl in vier verschillende vormen, of toestanden, vast te leggen. Ze bestudeerden het kanaal bij een licht zure pH (6,5), waarin het gesloten is, en bij een meer basische pH (9), waarin het actief zou moeten zijn maar in plaats daarvan een "gedesensitiseerde" vorm aanneemt die na langdurige stimulatie geen ionen meer geleidt. Ze bepaalden ook structuren van SsCl bij beide pH-waarden in aanwezigheid van ivermectine. In alle gevallen assembleert het eiwit als een vijfdelige ring die een centraal pore vormt. Verrassend genoeg neemt de pore in de gesloten en gedesensitiseerde toestanden een zandloperachtige vorm aan, met het smalste punt in het midden van het membraan — meer herinnerend aan kanalen die positief geladen ionen geleiden dan aan andere bekende chloridekanalen.
Hoe pH en ivermectine de pore hervormen
Door de grootte van de pore in elke structuur te meten, kon het team vorm aan functie relateren. Bij pH 6,5 zonder geneesmiddel is de centrale vernauwing te smal voor chloride-ionen om te passeren, overeenkomend met de niet-geleidende toestand. Bij pH 9 zonder geneesmiddel is de pore nog steeds te krap in het midden, zelfs al zou de omgeving normaal gesproken de opening van het kanaal bevorderen. Deze configuratie wordt geïnterpreteerd als een gedesensitiseerde staat die ontstaat na langdurige blootstelling aan basische omstandigheden. Wanneer ivermectine zich tussen segmenten van aangrenzende subunits in het membraan-spannende gebied klemt, wrikt het de helixen uit elkaar en verwijdt het de pore. Bij pH 6,5 veroorzaakt deze uitzetting een gedeeltelijk open pad dat nog steeds de ionenstroom beperkt nabij het selectiviteitsfilter aan de onderkant van de pore, wat overeenkomt met de langzame en bescheiden activatie van het kanaal door het middel. Bij pH 9 met ivermectine wordt de pore over het grootste deel van haar lengte wijd genoeg om robuuste chloridegeleiding te ondersteunen, in lijn met sterke elektrische stromen die in functionele experimenten zijn geregistreerd.
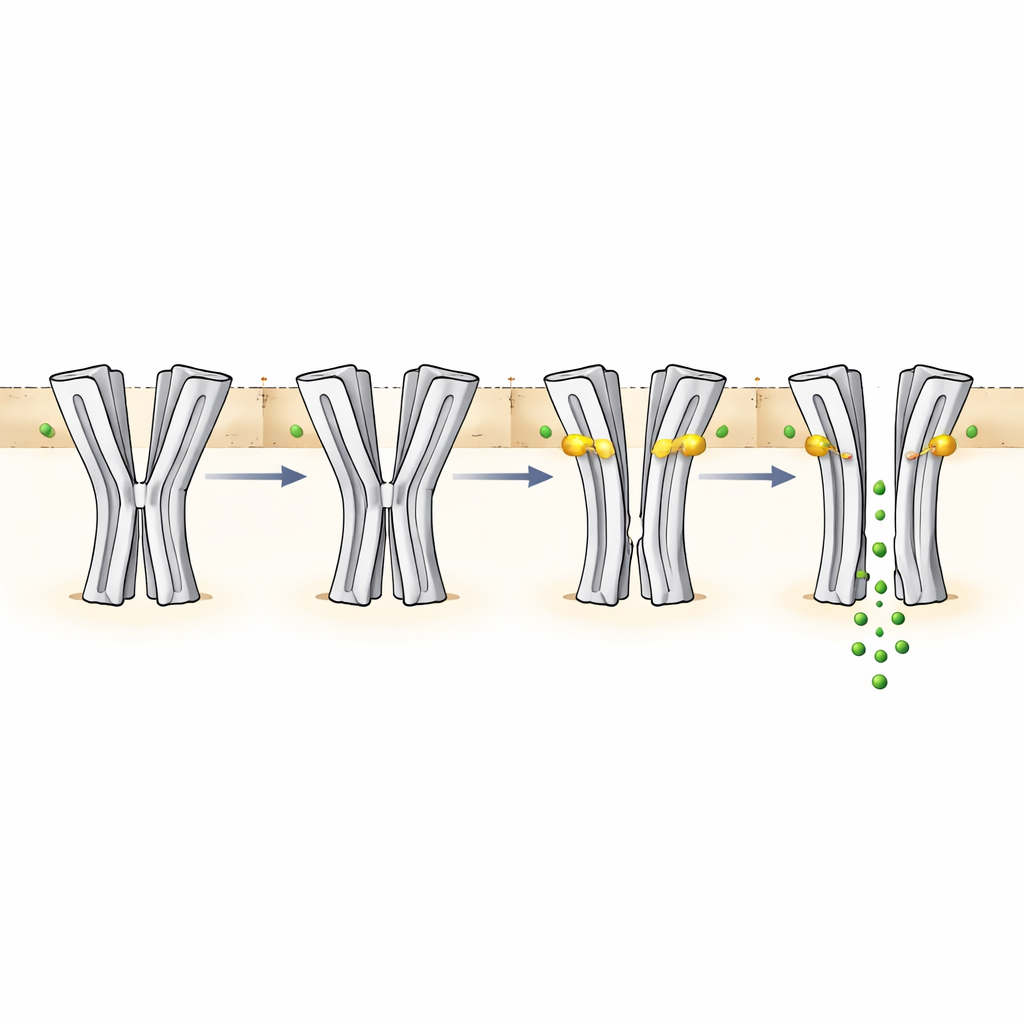
De verborgen pH-sensor en een breder controlesysteem
Om vast te stellen hoe SsCl pH detecteert, combineerden de auteurs computationele voorspellingen met structurele vergelijkingen en mutagenese. Ze identificeerden een cluster aminozuren — met name meerdere histidines en glutaminezuren — in het buitenste, met water blootgestelde deel van het eiwit, dichtbij een regio die bij verwante receptoren gewoonlijk chemische boodschappers bindt. Een sleutelpaar, een histidine (H206) en een glutaminezuur (E146), kan afhankelijke van de pH een ionische binding vormen of verbreken. Bij lagere pH helpt deze binding bepaalde structurele elementen op hun plaats te vergrendelen; bij hogere pH verzwakt de binding, waardoor een subtiele draai in dit gebied zich kan voortplanten naar de membraan-spannende helixen die de pore vormen. Het muteren van H206 of E146 veranderde het pH-bereik waarin het kanaal activeert, terwijl dubbele mutaties de pH-gevoeligheid konden verstoren maar ivermectine nog steeds toestonden stromen teweeg te brengen. Extra residuen nabij een flexibele lus bij de ingang van het kanaal beïnvloedden ook hoe het eiwit op pH-veranderingen reageert, wat het idee ondersteunt van een verspreid pH-gevoelersysteem in plaats van één enkele aan/uit-schakelaar.
Van moleculair inzicht naar betere schurftbehandelingen
Al met al toont het werk hoe een ionenkanaal van de schurftmijt zijn chemische omgeving waarneemt en hoe ivermectine bepaalde vormen van het kanaal stabiliseert om openen te bevorderen of te versterken. SsCl blijkt een ongewone chloridekanaal te zijn waarvan de gedesensitiseerde vorm lijkt op die van kanalen voor positief geladen ionen en waarvan de ladingsverdeling langs de pore fijn is afgestemd om chloride-ionen te geleiden. Door de structuren van het kanaal in meerdere functionele toestanden te bepalen en de residuen in kaart te brengen die pH- en geneesmiddelgevoeligheid afstellen, biedt de studie een blauwdruk voor het ontwerpen van nieuwe antiparasitaire verbindingen. Deze geneesmiddelen van de volgende generatie zouden zich op soortgelijke plaatsen kunnen vastzetten of hetzelfde pH-gevoelige mechanisme kunnen benutten, en zo nieuwe opties bieden om schurft te bestrijden in een wereld waar huidige behandelingen steeds meer het risico lopen hun doeltreffendheid te verliezen.
Bronvermelding: Kleiz-Ferreira, J., Brams, M., Harrison, P.J. et al. Structure of a pH-sensitive pentameric ligand-gated ion channel from the Sarcoptes scabies mite. Nat Commun 17, 3392 (2026). https://doi.org/10.1038/s41467-026-70575-0
Trefwoorden: schurft, ionkanalen, ivermectine, kruis-elektronenmicroscopie, parasietbestrijding