Clear Sky Science · fr
Structure d’un canal ionique pentamérique sensible au pH chez l’acarien Sarcoptes scabiei
Pourquoi de minuscules acariens et leurs commutateurs cachés comptent
La gale est une maladie de la peau fréquente mais souvent négligée, provoquant des démangeaisons intenses et pouvant entraîner des complications graves si elle n’est pas traitée. Elle est causée par l’acarien microscopique Sarcoptes scabiei, et les médecins dépendent largement du médicament ivermectine pour la contrôler. Cependant, des signes d’une résistance croissante aux médicaments commencent à apparaître. Cette étude révèle la structure 3D détaillée et le comportement d’une protéine clé du système nerveux de l’acarien — un canal au chlorure sensible au pH appelé SsCl — et montre exactement comment l’ivermectine interagit avec lui. En comprenant cet interrupteur moléculaire, les chercheurs espèrent concevoir des traitements de nouvelle génération qui restent efficaces même face à l’augmentation de la résistance.
Un canal ionique particulier dans un parasite problématique
SsCl appartient à une famille de protéines qui forment des pores, ou canaux, à travers les membranes cellulaires pour laisser passer des particules chargées. Ces mouvements d’ions sous-tendent la signalisation électrique dans les nerfs et les muscles. Contrairement aux récepteurs classiques qui répondent à des messagers chimiques spécifiques, SsCl réagit aux variations d’acidité ou d’alcalinité (pH) autour de la cellule. Lorsque l’environnement devient plus alcalin, SsCl s’ouvre normalement pour laisser passer des ions chlorure, aidant les cellules de l’acarien à maintenir leur équilibre et à communiquer. Parce que les canaux au chlorure sensibles au pH se trouvent principalement chez les invertébrés, ils constituent des cibles attractives pour des médicaments qui tuent les parasites sans nuire aux humains. Pourtant, jusqu’à présent, les scientifiques ne savaient pas comment SsCl détecte le pH ni comment l’ivermectine modifie son activité.
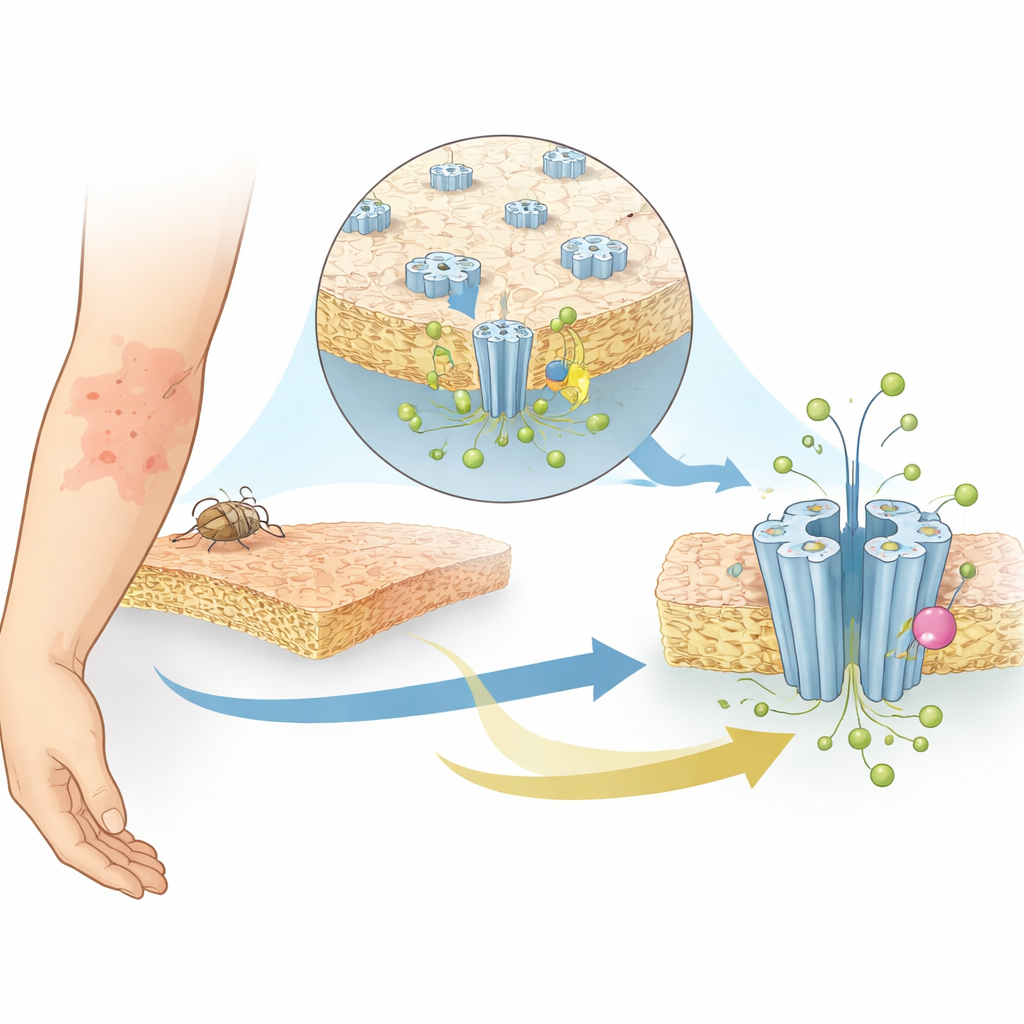
Capturer le canal en action par cryo‑EM
Les chercheurs ont utilisé la cryo‑microscopie électronique en particules uniques, une technique qui congèle rapidement les protéines et les image à une résolution proche de l’atomique, pour capturer SsCl dans quatre configurations différentes, ou états. Ils ont étudié le canal à un pH légèrement acide (6,5), où il est fermé, et à un pH plus alcalin (9), où il devrait être actif mais adopte instead une forme « désensibilisée » qui ne conduit plus les ions après une stimulation prolongée. Ils ont aussi déterminé les structures de SsCl aux deux niveaux de pH en présence d’ivermectine. Dans tous les cas, la protéine s’assemble en un anneau à cinq parties formant un pore central. De façon surprenante, le pore dans les états fermé et désensibilisé prend une forme de sablier, avec le point le plus étroit au milieu de la membrane — plus proche des canaux qui conduisent des ions positifs que des autres canaux au chlorure connus.
Comment le pH et l’ivermectine remodelent le pore
En mesurant la taille du pore dans chaque structure, l’équipe a pu relier la forme à la fonction. Au pH 6,5 sans médicament, la constriction centrale est trop étroite pour que les ions chlorure passent, ce qui correspond à l’état non conductible. Au pH 9 sans médicament, le pore reste trop serré au milieu, même si l’environnement favoriserait normalement l’ouverture du canal. Cette configuration est interprétée comme un état désensibilisé résultant d’une exposition prolongée à des conditions alcalines. Lorsque l’ivermectine se loge entre les segments de sous‑unités voisines dans la région transmembranaire, elle écarte les hélices et élargit le pore. À pH 6,5, cette expansion crée un passage partiellement ouvert qui restreint encore le flux d’ions près du filtre de sélectivité à la base du pore, cohérent avec l’activation lente et modeste du canal par le médicament. À pH 9 avec ivermectine, le pore devient suffisamment large sur la majeure partie de sa longueur pour permettre une conduction robuste des ions chlorure, en accord avec les forts courants électriques enregistrés dans les expériences fonctionnelles.
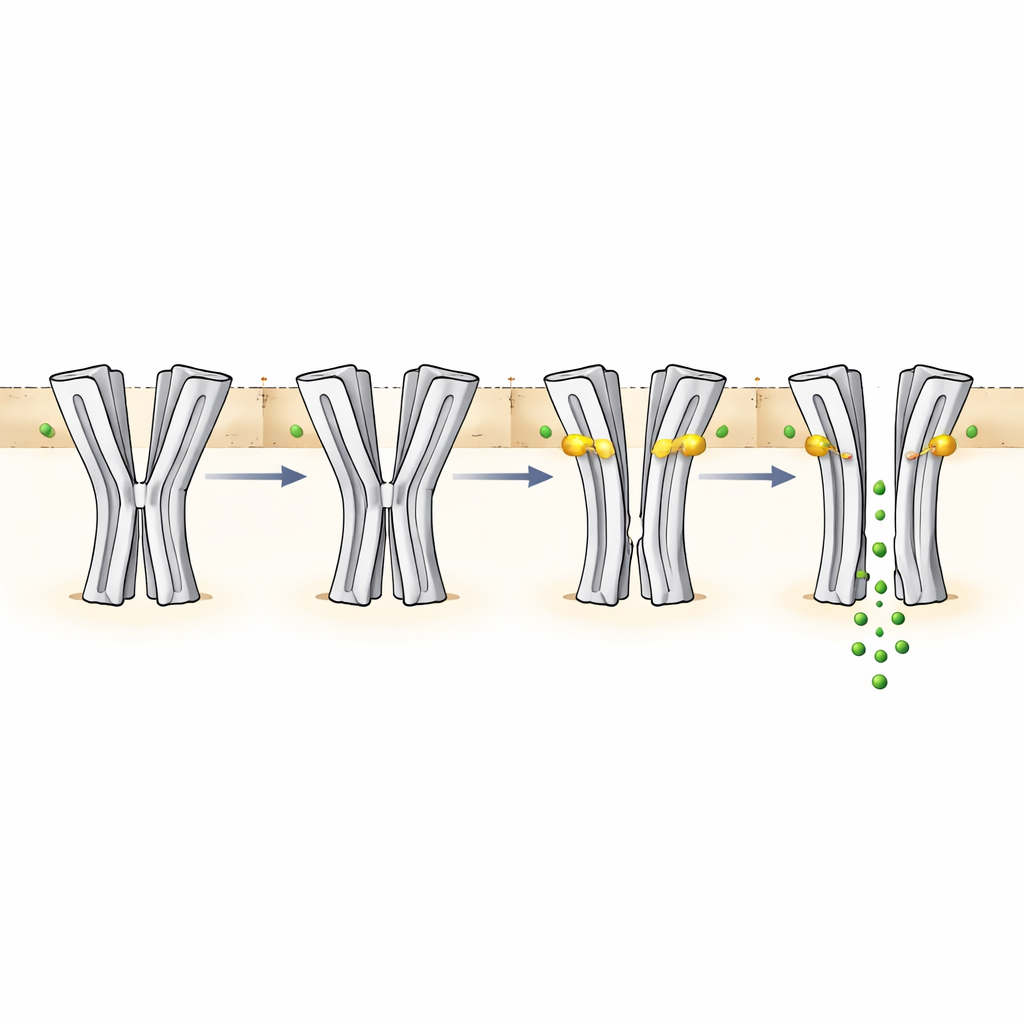
Le capteur de pH caché et un réseau de contrôle plus étendu
Pour identifier comment SsCl détecte le pH, les auteurs ont combiné des prédictions computationnelles avec des comparaisons structurelles et des mutagenèses. Ils ont repéré un regroupement d’acides aminés — en particulier plusieurs histidines et acides glutamiques — dans la partie externe exposée à l’eau de la protéine, près d’une région qui, chez des récepteurs apparentés, lie habituellement des messagers chimiques. Une paire clé, une histidine (H206) et un acide glutamique (E146), peut former ou rompre une liaison ionique selon le pH. À pH plus bas, cette liaison contribue à verrouiller certains éléments structurels ; à pH plus élevé, la liaison s’affaiblit, permettant une torsion subtile de cette zone qui se propage jusqu’aux hélices transmembranaires formant le pore. La mutation de H206 ou de E146 a modifié la plage de pH à laquelle le canal s’active, tandis que des doubles mutations pouvaient perturber la sensibilité au pH tout en laissant l’ivermectine déclencher des courants. D’autres résidus proches d’une boucle flexible à l’entrée du canal ont également influencé la réponse de la protéine aux variations de pH, soutenant l’idée d’un réseau sensible au pH distribué plutôt que d’un simple interrupteur tout‑ou‑rien.
De l’éclairage moléculaire à de meilleurs traitements contre la gale
Globalement, ce travail montre comment un canal ionique de l’acarien de la gale détecte son environnement chimique et comment l’ivermectine stabilise des conformations particulières du canal pour favoriser ou renforcer son ouverture. SsCl se révèle être un canal au chlorure inhabituel dont la forme désensibilisée ressemble à celle de canaux pour ions positifs et dont la répartition des charges le long du pore est finement réglée pour guider les ions chlorure. En résolvant les structures du canal dans plusieurs états fonctionnels et en cartographiant les résidus qui modulant le pH et la sensibilité au médicament, l’étude fournit une feuille de route pour concevoir de nouveaux composés antiparasitaires. Ces médicaments de nouvelle génération pourraient se fixer sur des sites similaires ou exploiter le même mécanisme de détection du pH, offrant de nouvelles options pour lutter contre la gale dans un monde où les traitements actuels risquent de perdre de leur efficacité.
Citation: Kleiz-Ferreira, J., Brams, M., Harrison, P.J. et al. Structure of a pH-sensitive pentameric ligand-gated ion channel from the Sarcoptes scabies mite. Nat Commun 17, 3392 (2026). https://doi.org/10.1038/s41467-026-70575-0
Mots-clés: gale, canaux ioniques, ivermectine, cryo-microscopie électronique, lutte contre les parasites