Clear Sky Science · de
Struktur eines pH-empfindlichen pentameren ligandengesteuerten Ionenkanals aus der Sarcoptes scabiei-Räude
Warum winzige Milben und ihre verborgenen Schalter wichtig sind
Krätze ist eine weit verbreitete, aber oft übersehene Hautkrankheit, die starken Juckreiz verursacht und unbehandelt zu schweren Komplikationen führen kann. Verursacht wird sie von der mikroskopischen Milbe Sarcoptes scabiei; Ärzte sind bei der Bekämpfung stark auf das Medikament Ivermectin angewiesen. Es mehren sich jedoch Hinweise auf zunehmende Wirkstoffresistenz. Diese Studie legt die detaillierte 3D-Struktur und das Verhalten eines Schlüsselproteins im Nervensystem der Milbe offen – eines pH-empfindlichen Chloridkanals namens SsCl – und zeigt genau, wie Ivermectin damit interagiert. Durch das Verständnis dieses molekularen Schalters hoffen Wissenschaftler, Wirkstoffe der nächsten Generation zu entwickeln, die auch bei steigendem Resistenzeniveau wirksam bleiben.
Ein besonderer Ionenkanal in einem lästigen Parasiten
SsCl gehört zu einer Familie von Proteinen, die Poren bzw. Kanäle in Zellmembranen bilden, durch die geladene Teilchen ein- und ausströmen können. Diese Ionenbewegungen sind die Grundlage elektrischer Signale in Nerven und Muskeln. Anders als klassische Rezeptoren, die auf spezifische chemische Botenstoffe reagieren, spricht SsCl auf Änderungen der Säure-Base-Bedingungen (pH) in der Umgebung der Zelle an. Wenn die Umgebung alkalischer wird, öffnet SsCl normalerweise und lässt Chloridionen passieren, was den Zellen der Milbe hilft, ihr Gleichgewicht zu halten und zu kommunizieren. Da pH-empfindliche Chloridkanäle überwiegend in wirbellosen Tieren vorkommen, sind sie attraktive Ziele für Wirkstoffe, die Parasiten abtöten, ohne Menschen zu schaden. Bislang war jedoch unklar, wie SsCl pH erkennt und wie Ivermectin seine Aktivität verändert.
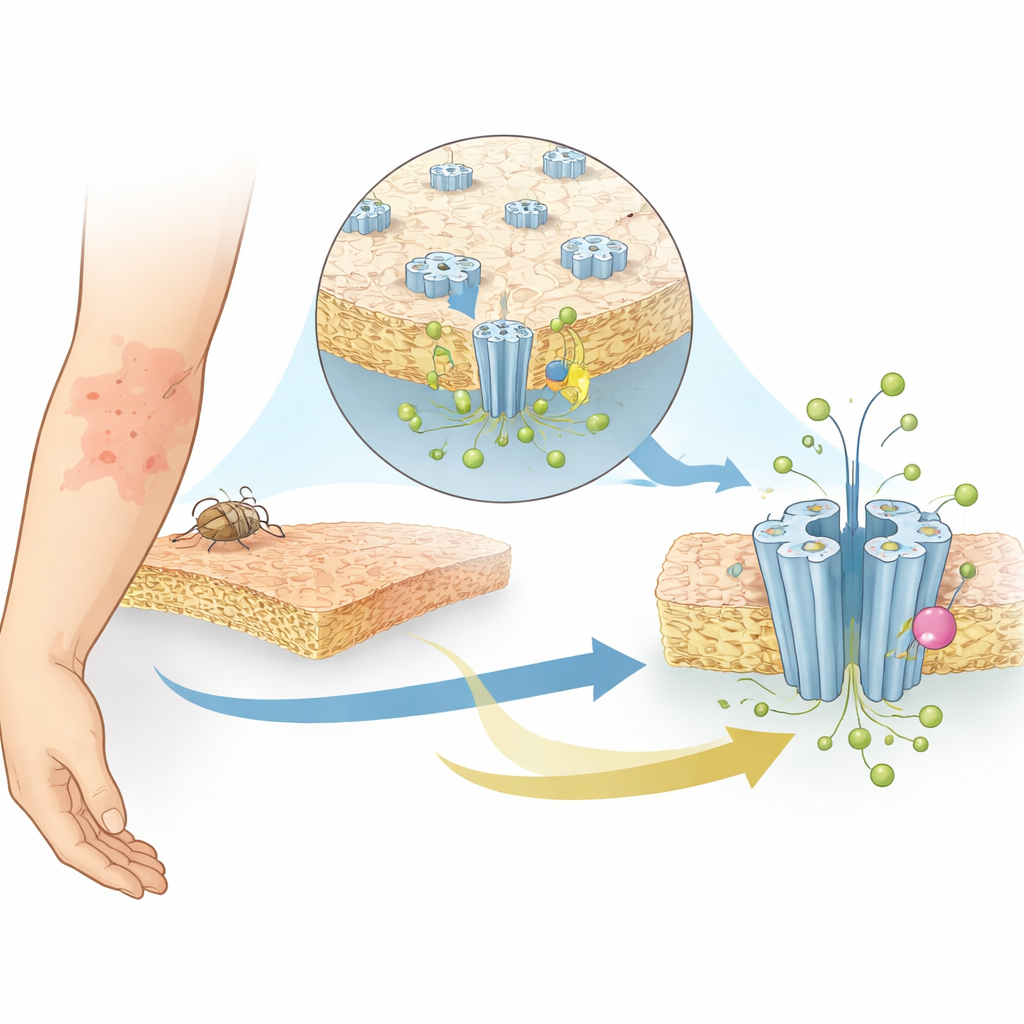
Den Kanal in Aktion einfangen mit Kryo-EM
Die Forscher verwendeten Einzelpartikel-Kryo-Elektronenmikroskopie, eine Technik, die Proteine blitzschnell einfriert und sie in nahezu atomarer Auflösung abbildet, um SsCl in vier verschiedenen Formen bzw. Zuständen zu erfassen. Sie untersuchten den Kanal bei leicht saurem pH (6,5), wo er geschlossen ist, und bei stärker alkalischem pH (9), wo er eigentlich aktiv sein sollte, aber stattdessen eine „desensibilisierte“ Form annimmt, die nach längerer Reizung keine Ionen mehr leitet. Außerdem bestimmten sie die Strukturen von SsCl in beiden pH-Bedingungen in Gegenwart von Ivermectin. In allen Fällen assembliert das Protein zu einem fünfteiligen Ring, der einen zentralen Porus bildet. Überraschenderweise nimmt der Porus in den geschlossenen und desensibilisierten Zuständen eine sanduhrartige Form an, mit der engsten Stelle in der Mitte der Membran – eher erinnernd an Kanäle für positiv geladene Ionen als an andere bekannte Chloridkanäle.
Wie pH und Ivermectin den Porus umformen
Durch Messung der Porengröße in jeder Struktur konnten die Autoren Form und Funktion in Beziehung setzen. Bei pH 6,5 ohne Wirkstoff ist die zentrale Engstelle zu eng für Chloridionen und entspricht damit dem nicht-leitenden Zustand. Bei pH 9 ohne Wirkstoff bleibt der Porus in der Mitte zu eng, obwohl die Umgebung normalerweise eine Öffnung begünstigen würde. Diese Konfiguration wird als desensibilisierter Zustand interpretiert, der durch längere Exposition gegenüber alkalischen Bedingungen entsteht. Wenn sich Ivermectin zwischen Segmente benachbarter Untereinheiten im membranspannenden Bereich einkeilt, drückt es die Helices auseinander und erweitert den Porus. Bei pH 6,5 erzeugt diese Erweiterung einen teilweise offenen Kanal, der den Ionendurchfluss am Selektivfilter am unteren Ende des Porus weiterhin einschränkt – im Einklang mit der langsamen und moderaten Aktivierung durch das Medikament. Bei pH 9 mit Ivermectin wird der Porus über den Großteil seiner Länge hin breit genug, um eine robuste Chloridleitung zu ermöglichen, was mit starken elektrischen Strömen übereinstimmt, die in funktionellen Experimenten gemessen wurden.
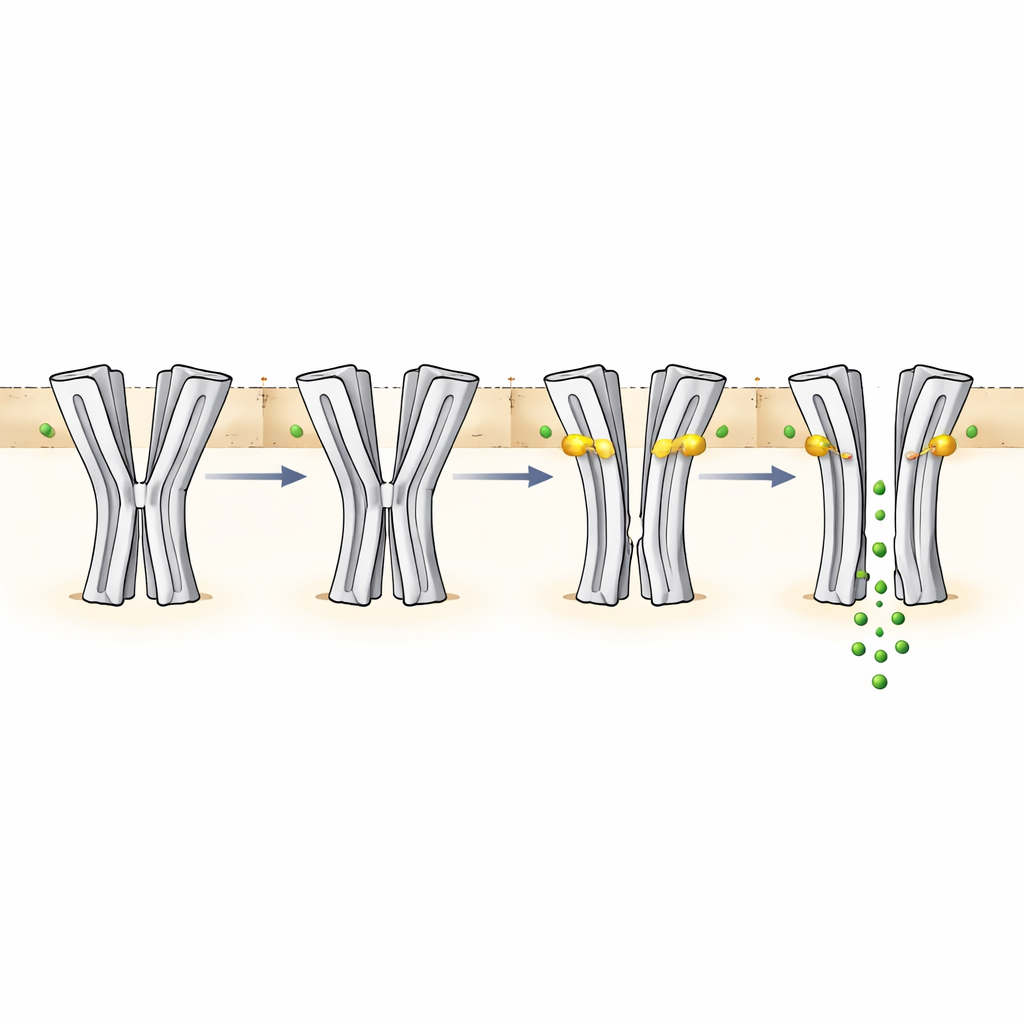
Der verborgene pH-Sensor und ein größeres Kontrollnetzwerk
Um herauszufinden, wie SsCl pH wahrnimmt, kombinierten die Autoren computerbasierte Vorhersagen mit strukturellen Vergleichen und Mutagenese-Experimenten. Sie identifizierten eine Gruppe von Aminosäuren – insbesondere mehrere Histidine und Glutaminsäuren – im äußeren, wasserexponierten Teil des Proteins, nahe einer Region, die in verwandten Rezeptoren üblicherweise chemische Botenstoffe bindet. Ein wichtiges Paar, ein Histidin (H206) und eine Glutaminsäure (E146), kann je nach pH eine ionische Bindung ausbilden oder lösen. Bei niedrigerem pH stabilisiert diese Bindung bestimmte Strukturelemente; bei höherem pH schwächt sie sich, wodurch eine feine Verdrehung in diesem Bereich entsteht, die sich bis zu den membranspannenden Helices fortpflanzt, die den Porus bilden. Mutation von H206 oder E146 verschob den pH-Bereich, in dem der Kanal aktiviert wird, während Doppelmutationen die pH-Empfindlichkeit stören konnten, Ivermectin aber dennoch Ströme auslösen ließ. Weitere Residuen in der Nähe einer flexiblen Schleife am Eingang des Kanals beeinflussten ebenfalls die pH-Reaktion des Proteins und stützen die Vorstellung eines verteilten pH-Sensorsystems statt eines einzelnen Ein-/Ausschalters.
Von molekularen Einsichten zu besseren Krätzebehandlungen
Insgesamt zeigt die Arbeit, wie ein Ionenkanal der Krätzmilbe seine chemische Umgebung erkennt und wie Ivermectin bestimmte Kanalzustände stabilisiert, um Öffnung zu fördern oder zu verstärken. SsCl erweist sich als ungewöhnlicher Chloridkanal, dessen desensibilisierte Gestalt der von Kanälen für positiv geladene Ionen ähnelt und dessen Ladungsverteilung entlang des Porus fein abgestimmt ist, um Chloridionen zu führen. Durch die Bestimmung der Kanalstrukturen in mehreren funktionellen Zuständen und die Kartierung der Rückstände, die pH- und Wirkstoffempfindlichkeit einstellen, liefert die Studie eine Blaupause für die Entwicklung neuer antiparasitärer Verbindungen. Diese Wirkstoffe der nächsten Generation könnten an ähnliche Stellen andocken oder die gleiche pH-Sensormaschinerie ausnutzen und so neue Optionen bieten, um Krätze in einer Welt zu bekämpfen, in der bestehende Behandlungen zunehmend ihre Wirkung zu verlieren drohen.
Zitation: Kleiz-Ferreira, J., Brams, M., Harrison, P.J. et al. Structure of a pH-sensitive pentameric ligand-gated ion channel from the Sarcoptes scabies mite. Nat Commun 17, 3392 (2026). https://doi.org/10.1038/s41467-026-70575-0
Schlüsselwörter: Krätze, Ionenkanäle, Ivermectin, Cryo-Elektronenmikroskopie, Parasitenbekämpfung