Clear Sky Science · sv
En enskild mutation i icke-strukturprotein 1 är avgörande för influensa B-virusets adaptiva evolution
Varför den här influensahistorien är viktig
Influenza B betraktas ofta som den "mildare släktingen" till de mer kända influensa A‑virusen, men den orsakar ändå tyst en stor andel av säsongens influensafall, särskilt bland barn. Denna studie ställer en till synes enkel men långtgående fråga: hur har influensa B förändrats över tid för att bli bättre på att leva i människor? Författarna spårar den förändringen till en enda aminosyra i ett viralt protein och visar hur den lilla förändringen hjälper viruset att smita förbi ett av våra cellers tidigaste larmssystem.
Närmare om en tyst besvärlig aktör
Influensa B-virus har cirkulerat bland människor i minst 80 år och delas nu in i två huvudgrupper, kallade Yamagata och Victoria. Epidemiologiska studier visar att influensa B vissa säsonger kan orsaka upp till hälften av alla influensainfektioner och en betydande del av vårdkostnaderna, särskilt bland skolbarn. Jämfört med influensa A vet vi dock mycket mindre om hur influensa B anpassar sig till den mänskliga värden. Tidigare arbete antydde att ett viralt protein, kallat NS1, utvecklas snabbt och kan hjälpa viruset att undvika vår medfödda immunförsvar, men vilka exakta förändringar som spelar roll var okänt.
Nyare virus överlistar våra tidiga försvar
Forskarna jämförde äldre influensa B-stammar, inklusive ett klassiskt 1940‑virus och ett isolat från 1988, med en nyare stam från 2018. I humana lungceller och i möss replikerade 2018‑viruset till högre nivåer, orsakade mer lungsönderfall och utlöste en lägre produktion av interferoner—molekyler som fungerar som kroppens snabba antivirala larm—och interferonstimulerade gener. Infekterade möss förlorade mer i vikt, hade högre dödlighet och uppvisade mer uttalad lungskada när de utsattes för den moderna stammen. Dessa observationer pekade på ett tydligt mönster: nyare influensa B‑virus har blivit bättre på att undertrycka värdens tidiga larmsystem, vilket ger dem mer tid och utrymme att föröka sig.
Den dolda städhacken inne i cellerna
För att förstå hur detta sker zoomade teamet in på NS1, ett multifunktionellt viralt protein som redan var känt för att störa immunsignalering. De upptäckte att NS1 från 2018‑stammen har en särskild förmåga: det utlöser en form av cellulär "självrengöring" riktad mot mitokondrierna, de energiproducerande strukturer som också fungerar som nav för antivirala signaler. Denna väg, kallad mitofagi, paketerar skadade mitokondrier i dubbelmembranösa säckar som smälter samman med nedbrytande kompartiment. När NS1 från den nyare stammen finns närvarande leder det till att viktiga mitokondriella proteiner, inklusive MAVS—en central förmedlare i interferonlarmsvägen—dras in i denna avfallsrutt och degraderas. När MAVS‑nivåerna sjunker kollapsar cellens förmåga att sända ut antivirala interferonsignaler, samtidigt som viruset replikerar mer effektivt.
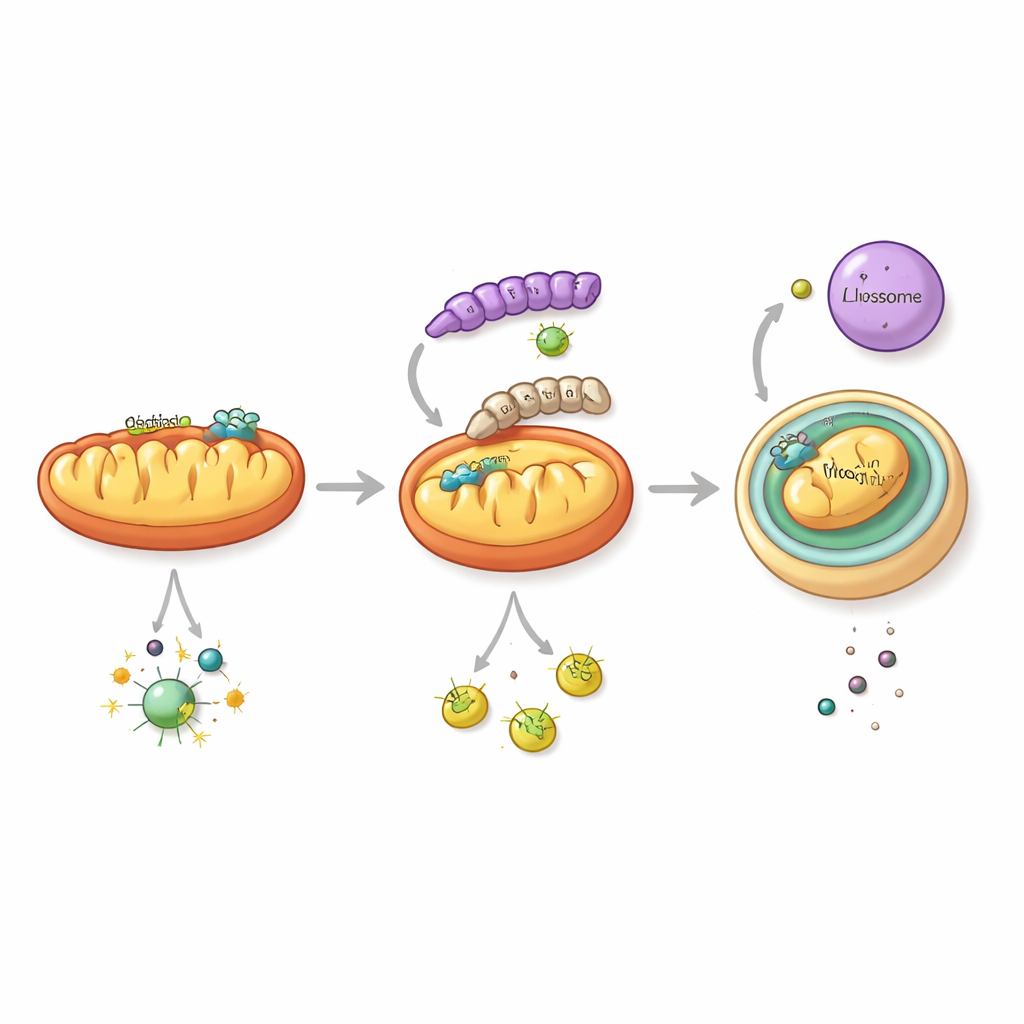
En enda molekylär växling med stort genomslag
Vad gör den moderna NS1 så skicklig på att kapa mitofagi? Genom att analysera tusentals virussekvenser identifierade forskarna en återkommande förändring på en specifik plats i NS1: aminosyra 247. I äldre stammar upptas denna position av fenylalanin, men under de senaste två decennierna har den i stor utsträckning ersatts av leucin. Strukturell modellering och biokemiska tester visade att denna leucin gör att NS1 kan binda tätare till LC3B, en nyckelmarkör på membranen som bildar autofagosomer, och till TUFM, ett mitokondriellt protein som hjälper till att organisera mitofagi. Tillsammans för dessa interaktioner NS1 till mitokondrier och in i de bildande autofagosomerna, vilket främjar selektiv borttagning av MAVS‑bärande mitokondrier. När forskarna genetiskt ändrade ett nyare virus så att det "gick tillbaka" till den gamla aminosyran (leucin tillbaka till fenylalanin) inducerade det förändrade viruset mindre mitofagi, sparade fler MAVS, utlöste starkare interferonsvar och orsakade lindrigare sjukdom hos möss.
Vad detta betyder för framtida influensasäsonger
Detta arbete visar att influensa B:s långsiktiga framgång hos människor inte bara handlar om förändringar i ytliga proteiner som hjälper viruset att undkomma antikroppar, utan också om subtil fininställning av dess förmåga att tysta våra tidigaste antivirala försvar. En enda aminosyraförändring i NS1 har gett nyare virus ett kraftfullt sätt att montera ner cellens larmsystem genom att omdirigera mitokondrier in i cellens ”skräpväg”. För allmänheten innebär budskapet att virus kan bli skickligare inte bara på att infektera oss, utan även på att gömma sig från våra immunsystem på allt mer förfinade sätt. För forskare och folkhälsotjänster kan övervakning av sådana adaptiva förändringar i interna virala proteiner som NS1 vara lika viktig som att följa mutationer i ytproteiner när man förutser framtida influensathot och utformar bättre vacciner och behandlingar.
Citering: Jiao, P., Jia, X., Bai, X. et al. A single mutation in nonstructural protein 1 is critical for the adaptive evolution of influenza B virus. Nat Commun 17, 3353 (2026). https://doi.org/10.1038/s41467-026-70211-x
Nyckelord: influensa B-virus, medfödd immunitet, virusets evolution, autofagi och mitofagi, mutation i NS1-proteinet