Clear Sky Science · fr
Une seule mutation dans la protéine non structurale 1 est critique pour l’évolution adaptative du virus grippal B
Pourquoi cette histoire de grippe importe
La grippe B est souvent perçue comme le « cousin plus doux » des mieux connus virus de la grippe A, mais elle est responsable silencieusement d’une part importante des cas saisonniers, en particulier chez les enfants. Cette étude pose une question apparemment simple mais aux implications majeures : comment la grippe B a-t-elle évolué au fil du temps pour mieux s’adapter à l’homme ? Les auteurs retracent ce changement jusqu’à un seul acide aminé dans une protéine virale et montrent comment ce léger ajustement aide le virus à contourner l’un des premiers systèmes d’alerte de nos cellules.
Un regard approfondi sur un fauteur de troubles discret
Les virus de la grippe B circulent chez l’homme depuis au moins 80 ans et se répartissent aujourd’hui en deux grandes familles, appelées Yamagata et Victoria. Des études épidémiologiques montrent que certaines saisons la grippe B peut causer jusqu’à la moitié des infections grippales et représenter une part substantielle des coûts hospitaliers, en particulier chez les enfants d’âge scolaire. Pourtant, comparée à la grippe A, on sait beaucoup moins comment la grippe B s’adapte à l’organisme humain. Des travaux antérieurs suggéraient qu’une protéine virale, appelée NS1, évolue rapidement et pourrait aider le virus à échapper à nos défenses innées, mais les modifications précises ayant un effet restaient inconnues.
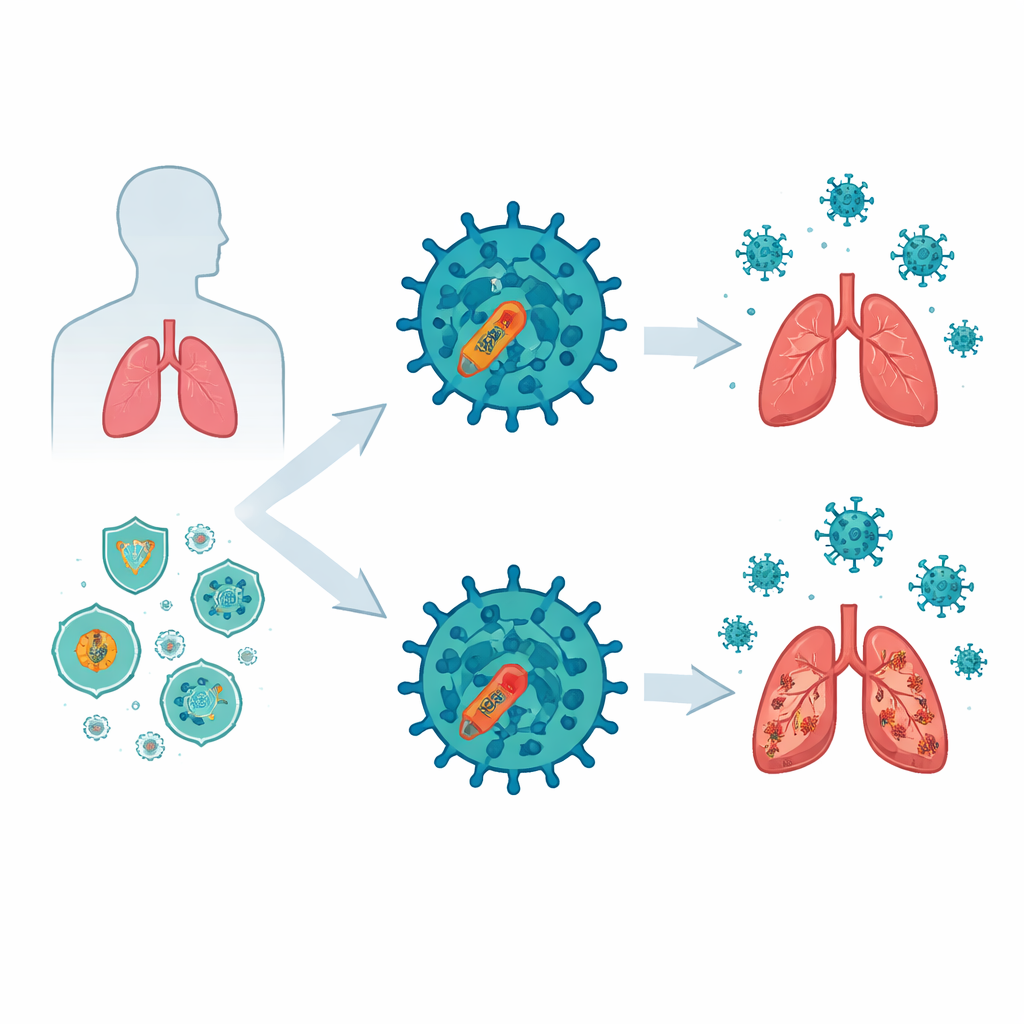
Les virus récents surpassent nos défenses précoces
Les chercheurs ont comparé des souches de grippe B plus anciennes, dont un virus classique de 1940 et un isolat de 1988, avec une souche récente de 2018. Dans des cellules pulmonaires humaines et chez la souris, le virus de 2018 a répliqué à des niveaux plus élevés, provoqué davantage de lésions pulmonaires et induit une production moindre d’interférons — des molécules jouant le rôle d’alarmes antivirales à réponse rapide — et des gènes stimulés par les interférons. Les souris infectées ont perdu plus de poids, présenté des taux de mortalité plus élevés et montré des lésions pulmonaires plus graves avec la souche moderne. Ces observations dessinent un schéma net : les virus grippaux B récents sont devenus meilleurs pour supprimer le système d’alerte précoce de l’hôte, ce qui leur laisse plus de temps et d’espace pour se multiplier.
Le tour de nettoyage caché à l’intérieur des cellules
Pour comprendre comment cela se produit, l’équipe s’est focalisée sur NS1, une protéine virale multifonctionnelle déjà connue pour perturber la signalisation immunitaire. Ils ont découvert que la NS1 de la souche 2018 possède une capacité particulière : elle déclenche une forme d’« auto-nettoyage » cellulaire ciblant les mitochondries, les organites producteurs d’énergie qui servent également de plateformes pour la signalisation antivirale. Cette voie, appelée mitophagie, englobe les mitochondries endommagées dans des vésicules à double membrane qui fusionnent avec des compartiments digestifs. Lorsque la NS1 de la souche récente est présente, elle entraîne des protéines mitochondriales clés, dont MAVS — un relais central dans la voie d’alerte des interférons — vers cette voie d’élimination pour être dégradées. À mesure que les niveaux de MAVS chutent, la capacité de la cellule à émettre des signaux interféron antiviraux s’effondre, tandis que le virus réplique plus efficacement.
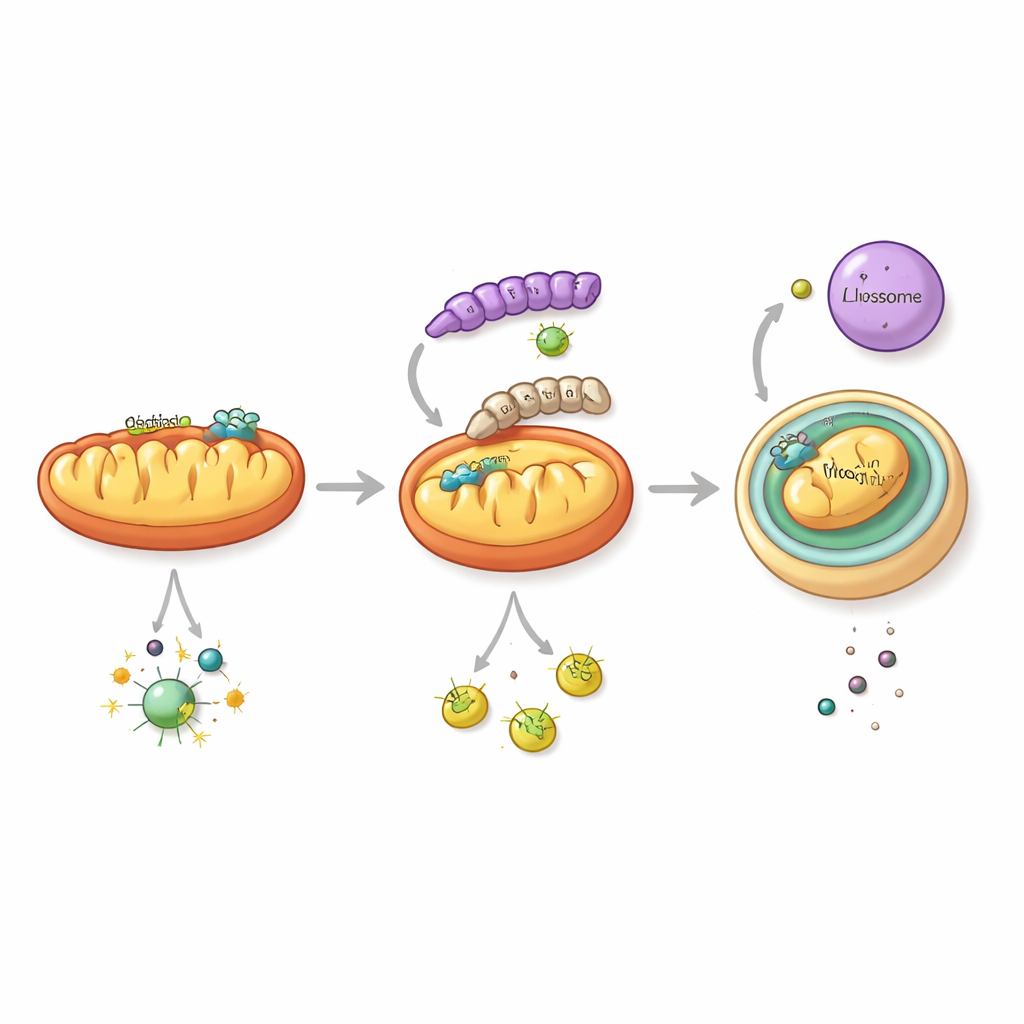
Un échange moléculaire unique au fort impact
Qu’est-ce qui rend la NS1 moderne si efficace pour détourner la mitophagie ? En analysant des milliers de séquences virales, les scientifiques ont identifié un changement récurrent en un point précis de la NS1 : l’acide aminé en position 247. Dans les souches anciennes, cette position est occupée par la phénylalanine, mais au cours des deux dernières décennies elle a été largement remplacée par la leucine. La modélisation structurelle et des tests biochimiques ont montré que cette leucine permet à NS1 de se lier plus fortement à LC3B, un marqueur clé des membranes formant les autophagosomes, et à TUFM, une protéine mitochondriale qui participe à l’organisation de la mitophagie. Ensemble, ces interactions amènent NS1 sur les mitochondries et dans les autophagosomes en formation, favorisant l’élimination sélective des mitochondries porteuses de MAVS. Lorsque les chercheurs ont génétiquement modifié un virus récent pour revenir à l’ancien acide aminé (leucine ramenée à phénylalanine), le virus altéré induisait moins de mitophagie, préservait davantage MAVS, déclenchait des réponses en interférons plus fortes et causait une maladie plus légère chez la souris.
Ce que cela signifie pour les saisons grippales à venir
Ce travail révèle que le succès à long terme de la grippe B chez l’humain ne tient pas seulement à des changements de ses protéines de surface qui lui permettent d’échapper aux anticorps, mais aussi à des ajustements subtils de sa capacité à réduire au silence nos premières défenses antivirales. Une substitution d’un seul acide aminé dans NS1 a donné aux virus récents un moyen puissant de démanteler la machinerie d’alerte cellulaire en redirigeant les mitochondries vers la voie d’élimination cellulaire. Pour le grand public, le message est que les virus peuvent devenir plus efficaces non seulement pour nous infecter, mais aussi pour se cacher de nos systèmes immunitaires de façons de plus en plus sophistiquées. Pour les chercheurs et les responsables de santé publique, surveiller de tels changements adaptatifs dans des protéines virales internes comme NS1 peut être aussi important que suivre les mutations des protéines de surface pour prévoir les menaces grippales futures et concevoir de meilleurs vaccins et traitements.
Citation: Jiao, P., Jia, X., Bai, X. et al. A single mutation in nonstructural protein 1 is critical for the adaptive evolution of influenza B virus. Nat Commun 17, 3353 (2026). https://doi.org/10.1038/s41467-026-70211-x
Mots-clés: virus grippal B, immunité innée, évolution virale, autophagie et mitophagie, mutation de la protéine NS1