Clear Sky Science · it
Una singola mutazione nella proteina non strutturale 1 è cruciale per l’evoluzione adattativa del virus dell’influenza B
Perché questa storia sull’influenza conta
L’influenza B è spesso considerata la “cugina più mite” dei più noti virus influenzali di tipo A, eppure provoca in modo silenzioso una quota consistente dei casi stagionali, soprattutto nei bambini. Questo studio pone una domanda apparentemente semplice ma dalle grandi implicazioni: come si è modificata l’influenza B nel tempo per diventare più adatta a vivere negli esseri umani? Gli autori rintracciano quel cambiamento fino a un singolo aminoacido in una proteina virale e mostrano come quella piccola modifica aiuti il virus a eludere uno dei primi sistemi d’allarme delle nostre cellule.
Uno sguardo ravvicinato a un disturbatore silenzioso
I virus dell’influenza B circolano nell’uomo da almeno 80 anni e oggi si raggruppano in due famiglie principali, chiamate Yamagata e Victoria. Studi epidemiologici mostrano che in alcune stagioni l’influenza B può causare fino alla metà di tutte le infezioni influenzali e una frazione rilevante dei costi ospedalieri, in particolare tra i bambini in età scolare. Eppure, rispetto all’influenza A, sappiamo molto meno su come l’influenza B si adatti al corpo umano. Lavori precedenti avevano suggerito che una proteina virale, chiamata NS1, evolve rapidamente e potrebbe aiutare il virus a sfuggire alle nostre difese innate, ma i cambiamenti esatti rilevanti non erano noti.
I virus più recenti sovvertono le nostre difese precoci
I ricercatori hanno confrontato ceppi di influenza B più vecchi, inclusi un virus classico del 1940 e un isolato del 1988, con un ceppo recente del 2018. In cellule polmonari umane e nei topi, il virus del 2018 si è replicato a livelli più elevati, ha causato maggior danno polmonare e ha indotto una minore produzione di interferoni — molecole che fanno da segnali antivirali a risposta rapida — e di geni stimolati dagli interferoni. I topi infettati hanno perso più peso, hanno avuto tassi di mortalità più alti e hanno mostrato lesioni polmonari più gravi quando esposti al ceppo moderno. Queste osservazioni indicano un quadro chiaro: i virus di influenza B recenti sono diventati migliori nel sopprimere il sistema d’allarme precoce dell’ospite, concedendosi più tempo e spazio per moltiplicarsi.
Il trucco nascosto di pulizia all’interno delle cellule
Per capire come ciò avvenga, il team si è concentrato su NS1, una proteina virale multifunzionale già nota per interferire con la segnalazione immunitaria. Hanno scoperto che l’NS1 del ceppo 2018 possiede una capacità speciale: innesca una forma di “autopulizia” cellulare diretta ai mitocondri, le strutture produttrici di energia che fungono anche da centri per la segnalazione antivirale. Questa via, chiamata mitofagia, incapsula mitocondri danneggiati in sacche a doppia membrana che si fondono con compartimenti digestivi. Quando è presente l’NS1 della variante recente, provoca l’inclusione di proteine mitocondriali chiave, incluso MAVS — un relè centrale nella via di allarme dell’interferone — in questo percorso di smaltimento e la loro degradazione. Con la riduzione dei livelli di MAVS, la capacità della cellula di inviare segnali interferonici antivirali crolla, mentre il virus si replica più efficacemente.
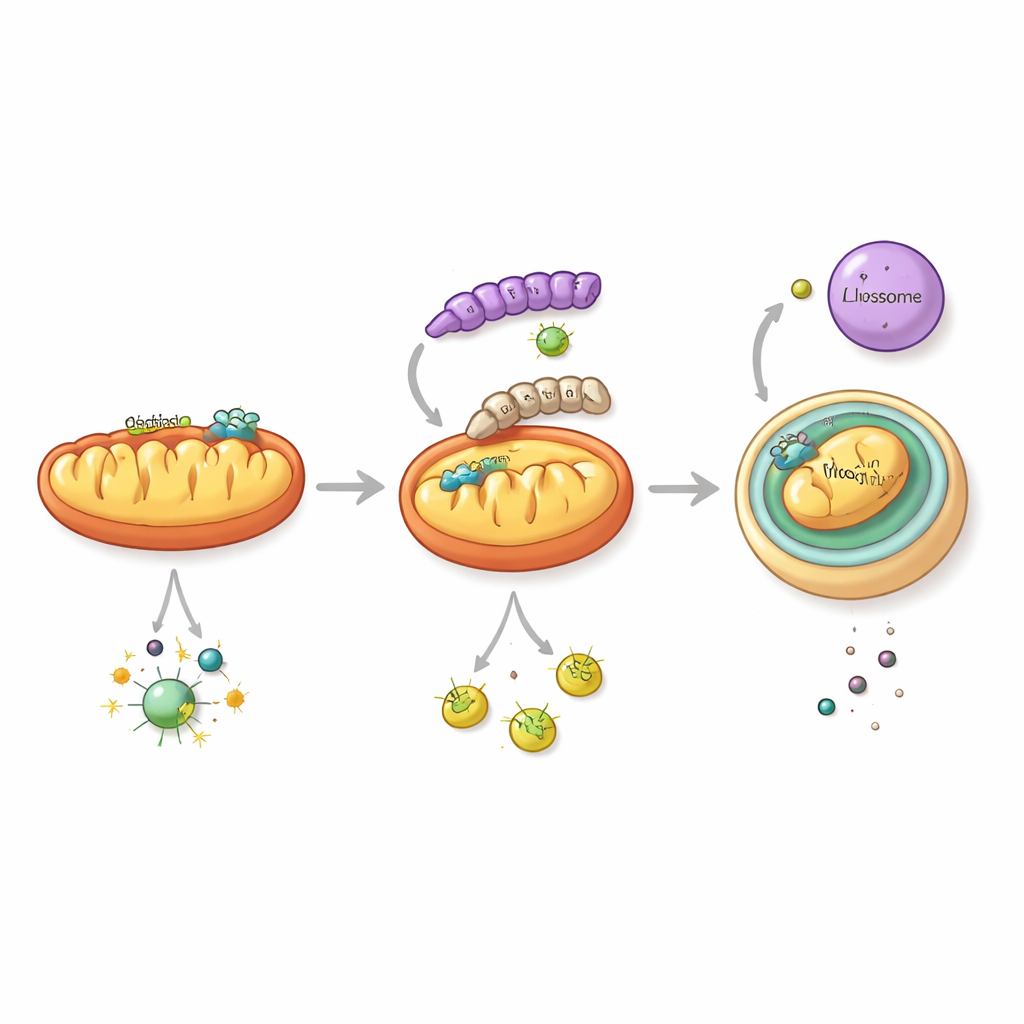
Un singolo scambio molecolare con grande impatto
Cosa rende l’NS1 moderno così efficace nello sfruttare la mitofagia? Analizzando migliaia di sequenze virali, gli scienziati hanno individuato un cambiamento ricorrente in un punto specifico di NS1: l’aminoacido alla posizione 247. Nei ceppi più vecchi questa posizione è occupata da fenilalanina, ma negli ultimi due decenni è stata in gran parte sostituita dalla leucina. Modellizzazione strutturale e test biochimici hanno mostrato che questa leucina permette a NS1 di legarsi più strettamente a LC3B, un marcatore chiave sulle membrane che formano gli autofagosomi, e a TUFM, una proteina mitocondriale che aiuta a organizzare la mitofagia. Insieme, queste interazioni portano NS1 sui mitocondri e negli autofagosomi in formazione, promuovendo la rimozione selettiva dei mitocondri che contengono MAVS. Quando i ricercatori hanno ingegnerizzato un virus recente per «tornare indietro» e ripristinare il vecchio aminoacido (leucina sostituita da fenilalanina), il virus modificato ha indotto meno mitofagia, ha preservato più MAVS, ha scatenato risposte interferoniche più forti e ha causato una malattia più lieve nei topi.
Cosa significa per le future stagioni influenzali
Questo lavoro rivela che il successo a lungo termine dell’influenza B nell’uomo non riguarda solo cambiamenti nelle sue proteine di superficie che la aiutano a sfuggire agli anticorpi, ma anche un raffinamento sottile della sua capacità di silenziare le nostre difese antivirali più precoci. Una singola sostituzione di un aminoacido in NS1 ha fornito ai virus recenti un modo potente per smantellare il meccanismo d’allarme cellulare reindirizzando i mitocondri verso la via di smaltimento cellulare. Per il grande pubblico, il messaggio è che i virus possono diventare più abili non solo nell’infettarci, ma nel nascondersi dal nostro sistema immunitario in modi sempre più sofisticati. Per ricercatori e responsabili della sanità pubblica, monitorare tali cambiamenti adattativi in proteine virali interne come NS1 potrebbe essere importante quanto tracciare le mutazioni nelle proteine di superficie quando si prevedono le minacce influenzali future e si progettano vaccini e terapie migliori.
Citazione: Jiao, P., Jia, X., Bai, X. et al. A single mutation in nonstructural protein 1 is critical for the adaptive evolution of influenza B virus. Nat Commun 17, 3353 (2026). https://doi.org/10.1038/s41467-026-70211-x
Parole chiave: virus dell’influenza B, immunità innata, evoluzione virale, autofagia e mitofagia, mutazione della proteina NS1