Clear Sky Science · de
Eine einzelne Mutation im nichtstrukturellen Protein 1 ist entscheidend für die adaptive Evolution des Influenza-B-Virus
Warum diese Grippegeschichte wichtig ist
Influenza B gilt oft als der „mildere Verwandte“ der bekannteren Influenza-A-Viren, verursacht aber dennoch einen erheblichen Anteil der saisonalen Grippefälle, besonders bei Kindern. Diese Studie stellt eine auf den ersten Blick einfache, aber weitreichende Frage: Wie hat sich Influenza B im Lauf der Zeit verändert, um besser im Menschen zu überleben? Die Autoren verfolgen diese Veränderung bis zu einer einzelnen Aminosäure in einem viralen Protein zurück und zeigen, wie diese kleine Änderung dem Virus hilft, eines der frühesten Alarmsysteme unserer Zellen zu umgehen.
Ein genauerer Blick auf einen leisen Übeltäter
Influenza-B-Viren zirkulieren beim Menschen seit mindestens 80 Jahren und gehören heute zu zwei Hauptlinien, genannt Yamagata und Victoria. Epidemiologische Studien zeigen, dass Influenza B in manchen Saisons bis zur Hälfte aller Grippeinfektionen und einen beachtlichen Anteil der Krankenhauskosten verursachen kann, insbesondere bei Schulkindern. Im Vergleich zu Influenza A wissen wir jedoch deutlich weniger darüber, wie sich Influenza B an den menschlichen Körper anpasst. Frühere Arbeiten deuteten an, dass ein virales Protein namens NS1 sich schnell entwickelt und dem Virus helfen könnte, die angeborene Immunabwehr zu umgehen, doch welche genauen Veränderungen relevant sind, war bislang unklar.
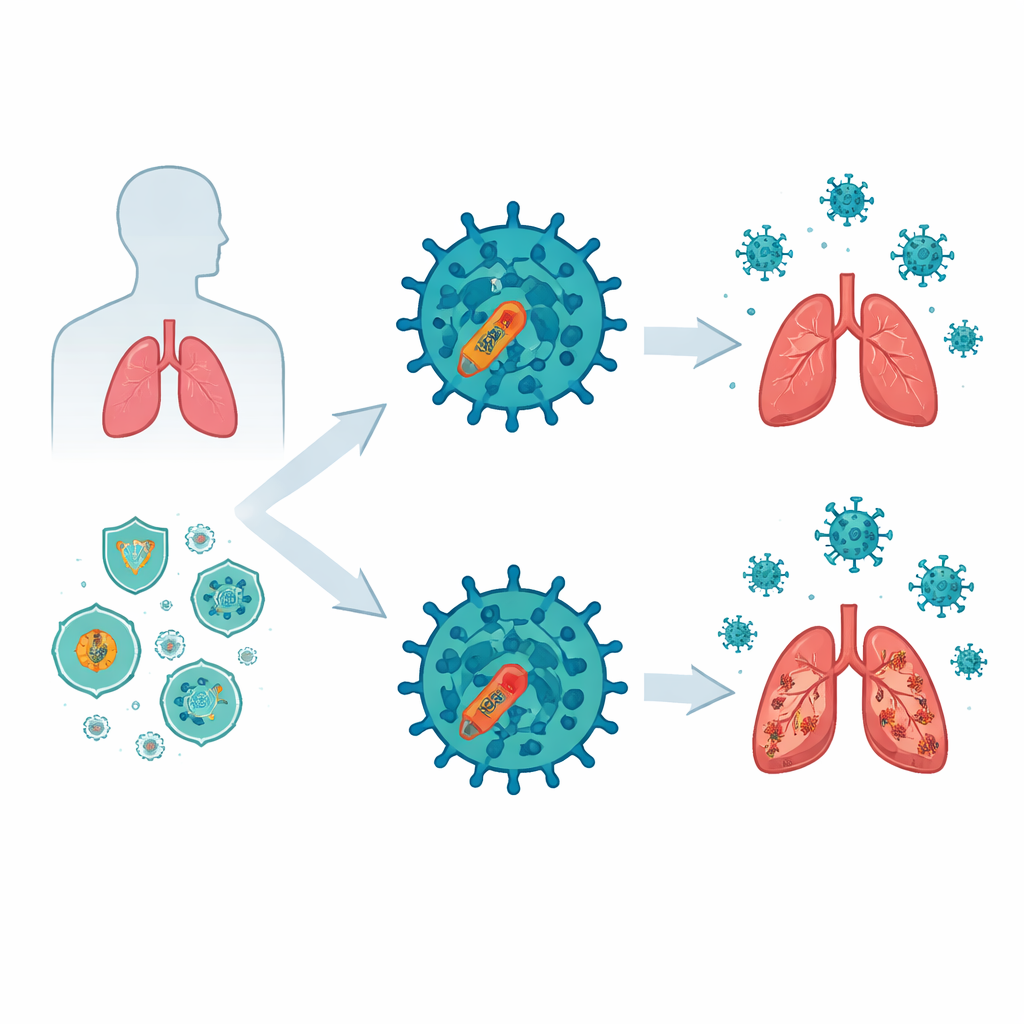
Neuere Viren überlisten unsere frühen Abwehrreaktionen
Die Forschenden verglichen ältere Influenza-B-Stämme, darunter ein klassisches Virus von 1940 und einen Isolat aus 1988, mit einem aktuellen Stamm von 2018. In menschlichen Lungenzellen und in Mäusen replizierte das 2018-Virus stärker, verursachte mehr Lungengewebe-Schäden und löste eine geringere Produktion von Interferonen—Molekülen, die als schnelle antivirale Alarmsignale fungieren—sowie interferon-stimulierten Genen aus. Infizierte Mäuse verloren mehr Gewicht, wiesen höhere Sterblichkeitsraten auf und zeigten bei Exposition gegenüber dem modernen Stamm schwerere Lungenschäden. Diese Beobachtungen zeigten ein klares Muster: neuere Influenza-B-Viren sind besser darin geworden, das frühe Alarmsystem des Wirts zu unterdrücken und sich so mehr Zeit und Raum zur Vermehrung zu verschaffen.
Der verborgene Aufräumtrick in den Zellen
Um zu verstehen, wie das geschieht, konzentrierte sich das Team auf NS1, ein multifunktionelles virales Protein, das bereits dafür bekannt ist, in die Immun-Signalwege einzugreifen. Sie entdeckten, dass das NS1 des 2018-Stamms eine besondere Fähigkeit besitzt: es löst eine Form der zellulären „Selbstreinigung“ aus, die gezielt Mitochondrien betrifft—die energieerzeugenden Strukturen, die zugleich Knotenpunkte für antivirales Signaling sind. Dieser Weg, Mitophagie genannt, verpackt beschädigte Mitochondrien in doppelmembranige Hüllen, die mit Verdauungskompartimenten verschmelzen. Ist das NS1 des neueren Stamms vorhanden, führt es dazu, dass wichtige mitochondriale Proteine, darunter MAVS—ein zentraler Relay-Mechanismus im Interferon-Alarmweg—in diese Entsorgungsroute geschleust und abgebaut werden. Sinkt der MAVS-Spiegel, bricht die Fähigkeit der Zelle zusammen, antivirale Interferon-Signale auszusenden, während das Virus effizienter repliziert.
Ein einzelner molekularer Tausch mit großer Wirkung
Was macht das moderne NS1 so geschickt darin, die Mitophagie zu kapern? Durch Analyse von Tausenden von Virussequenzen identifizierten die Wissenschaftler eine wiederkehrende Veränderung an einer spezifischen Stelle in NS1: Aminosäure 247. Bei älteren Stämmen ist diese Position mit Phenylalanin besetzt, in den letzten zwei Jahrzehnten wurde sie jedoch überwiegend durch Leucin ersetzt. Strukturmodellierung und biochemische Tests zeigten, dass dieses Leucin NS1 erlaubt, stärker an LC3B zu binden, einen wichtigen Marker auf den Membranen, die Autophagosomen bilden, sowie an TUFM, ein mitochondriales Protein, das die Mitophagie mitorganisiert. Zusammen bringen diese Interaktionen NS1 auf die Mitochondrien und in die entstehenden Autophagosomen und fördern so die selektive Entfernung von Mitochondrien, die MAVS tragen. Als die Forscher ein aktuelles Virus so veränderten, dass es zur alten Aminosäure zurückkehrte (Leucin zurück zu Phenylalanin), verursachte das veränderte Virus weniger Mitophagie, schonte mehr MAVS, löste stärkere Interferon-Antworten aus und führte bei Mäusen zu milderen Erkrankungen.
Was das für kommende Grippesaisons bedeutet
Diese Arbeit zeigt, dass der langfristige Erfolg von Influenza B beim Menschen nicht nur mit Veränderungen seiner Oberflächenproteine zusammenhängt, die dem Entgehen von Antikörpern dienen, sondern auch mit feiner Abstimmung seiner Fähigkeit, unsere frühesten antiviralen Abwehrmechanismen zum Schweigen zu bringen. Eine einzige Aminosäure-Substitution in NS1 hat neueren Viren eine mächtige Möglichkeit verschafft, die Alarmmaschinerie der Zelle zu demontieren, indem sie Mitochondrien in den zellulären Müllweg umlenken. Für die Öffentlichkeit ist die Botschaft, dass Viren nicht nur besser darin werden können, uns zu infizieren, sondern auch darin, sich immer raffinierteren Methoden zu bedienen, um dem Immunsystem zu entgehen. Für Forschende und Gesundheitsbehörden könnte die Überwachung solcher adaptiven Veränderungen in internen viralen Proteinen wie NS1 ebenso wichtig sein wie das Nachverfolgen von Mutationen in Oberflächenproteinen, wenn es darum geht, zukünftige Grippegefahren vorherzusagen und bessere Impfstoffe und Therapien zu entwickeln.
Zitation: Jiao, P., Jia, X., Bai, X. et al. A single mutation in nonstructural protein 1 is critical for the adaptive evolution of influenza B virus. Nat Commun 17, 3353 (2026). https://doi.org/10.1038/s41467-026-70211-x
Schlüsselwörter: Influenza-B-Virus, angeborene Immunität, virale Evolution, Autophagie und Mitophagie, NS1-Protein-Mutation