Clear Sky Science · sv
Identifiering och strukturell karaktärisering av antraxtoxinsreceptorn 2 som Clostridium perfringens NetF‑receptor
Varför detta toxin spelar roll för människor och djur
Allvarliga tarminfektioner hos hundar, hästar och boskap kan komma plötsligt, ge blodig diarré och ibland vara dödliga. En vanlig orsak är bakterien Clostridium perfringens, som skadar celler genom att skapa hål i dem med kraftfulla proteintoxiner. Denna studie visar på molekylär nivå hur ett sådant toxin, kallat NetF, hittar och angriper specifika djurceller. Arbetet förklarar inte bara gåtfulla sjukdomsutbrott hos sällskapsdjur och lantbruksdjur, utan blottlägger också allmänna principer för hur porbildande toxiner fäster vid våra celler — ett steg som kan bli måltavla för framtida terapier.
En bakteriell väpnad med borr
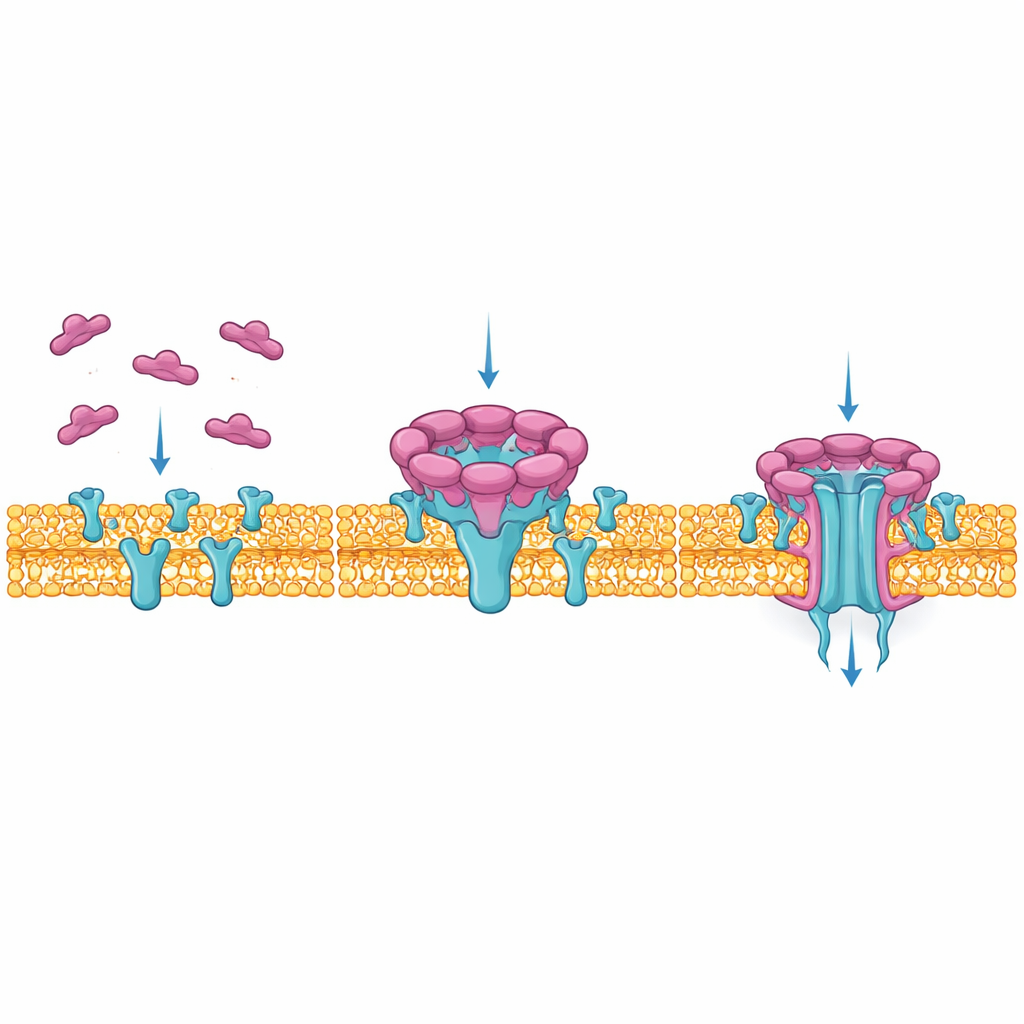
NetF tillhör en stor familj av ”porbildande” toxiner som bakterier släpper ut som lösliga enheter. När de kommer i kontakt med en lämplig cell monterar dessa enheter ihop sig till ringar som tränger in i cellmembranet och bildar kanaler. Genom dessa kanaler läcker livsviktiga molekyler ut och cellen kollapsar. Även om liknande toxiner från Clostridium perfringens är kända för att orsaka dödliga tarmsjukdomar hos grisar, fjäderfä och människor, var väldigt lite känt om hur NetF väljer sina målceller eller hur dess slutliga por ser ut i atomär detalj.
Att hitta toxinets dockningshandtag
Forskarna frågade först varför vissa celltyper från människor, hundar, hästar och nötkreatur dödas av NetF medan andra förblir opåverkade. Genom att jämföra genaktivitet i känsliga och resistenta celler, och genom att upprepade gånger utsätta celler för NetF tills sällsynta överlevare tog över, fann de att resistenta celler konsekvent producerade mycket mindre av ett ytlprotein kallat ANTXR2. Denna molekyl var redan känd som huvudreceptorn för antraxtoxin. När teamet slog ut ANTXR2 med CRISPR‑genredigering blev celler motståndskraftiga mot NetF. När de tillsatte extra mänsklig, hundlig, hästlig eller boskaps‑ANTXR2 blev tidigare resistenta celler mycket känsliga, vilket bekräftar att NetF förlitar sig på ANTXR2 som sitt dockningshandtag över flera djurslag.
Att se poren montera sig i nästan atomär skala
För att exakt se hur NetF bygger sin dödliga kanal använde författarna kryoelektronmikroskopi, som avbildar blixtfrusna molekyler med mycket hög upplösning. De återskapade toxinets interaktion med artificiella membran och fann två huvudstadier: en ”pre‑pore”, där nio NetF‑enheter ligger på membranytan, och en slutlig por som oftast byggs av åtta enheter som har pressat en lång, tätt packad proteinbarrel genom membranet. Jämförelse av dessa stadier visade hur en flexibel loop i varje NetF‑molekyl svänger ned och omstrukturerar sig till en 50 ångström lång barrel som matchar membranets tjocklek och skapar en smal, vattenfylld tunnel genom vilken joner och små molekyler kan passera.
Hur NetF greppar både receptor och membran
Teamet löste därefter strukturen för NetF:s por bunden till hela den yttre delen av ANTXR2. Till skillnad från antraxtoxin, som tar tag i en metallbindande plats längst ut på ANTXR2, klämmer NetF sig fast på sidan av receptorn och kontaktar två olika regioner samtidigt. Detta sidofäste placerar toxinet nära membranet och låter delar av NetF:s ”rim” och ”stam” tränga ner i närliggande lipider och kolesterol. Gränsytan är ovanligt rik på tyrosinrester, vilka stabiliserar både receptorbindningen och membranankaret. Subtila sekvensskillnader i receptorernas nedre region, särskilt hos möss, försvagar denna passform och hjälper till att förklara varför musceller naturligt är mer motståndskraftiga mot NetF än celler från andra däggdjur.
Vad dessa fynd betyder för sjukdom
Tillsammans visar resultaten att NetF bara dödar celler när det kan fästa ordentligt vid ANTXR2 och samtidigt engagera omgivande membranlipider för att driva inporingen. Denna dubbla igenkänning förklarar dess starka aktivitet hos hundar och föl, där ANTXR2‑bärande celler i tarmen är primära mål, och dess svagare effekt hos möss. Mer generellt avslöjar studien en återkommande strategi bland porbildande toxiner: att binda nära membranet via specifika receptorer som fungerar som ställningar för porens montering. Genom att kartlägga de exakta kontaktpunkterna mellan NetF och ANTXR2 öppnar arbetet dörren för att utforma molekyler som kan blockera interaktionen och potentiellt skydda utsatta djur från förödande tarmsjukdomar.
Citering: Wang, C., Cattalani, F., Iacovache, I. et al. Identification and structural characterization of anthrax toxin receptor 2 as the Clostridium perfringens NetF receptor. Nat Commun 17, 2788 (2026). https://doi.org/10.1038/s41467-026-69526-6
Nyckelord: porbildande toxin, Clostridium perfringens, NetF, ANTXR2‑receptor, bakteriell patogenes