Clear Sky Science · de
Identifizierung und strukturelle Charakterisierung des Anthrax‑Toxin‑Rezeptors 2 als Rezeptor von Clostridium perfringens NetF
Warum dieses Toxin für Menschen und Tiere wichtig ist
Schwere Darminfektionen bei Hunden, Pferden und Nutztieren können plötzlich auftreten, blutigen Durchfall verursachen und mitunter tödlich verlaufen. Häufig verantwortlich ist das Bakterium Clostridium perfringens, das Zellen durch das Einbringen von Löchern mit kraftvollen Proteintoxinen schädigt. Diese Studie zeigt auf molekularer Ebene, wie ein solches Toxin namens NetF bestimmte tierische Zellen erkennt und angreift. Die Arbeit erklärt nicht nur rätselhafte Krankheitsausbrüche bei Haustieren und Nutztieren, sondern legt auch allgemeine Prinzipien offen, wie porenbildende Toxine an unsere Zellen andocken — ein Schritt, der künftig therapeutisch angesteuert werden könnte.
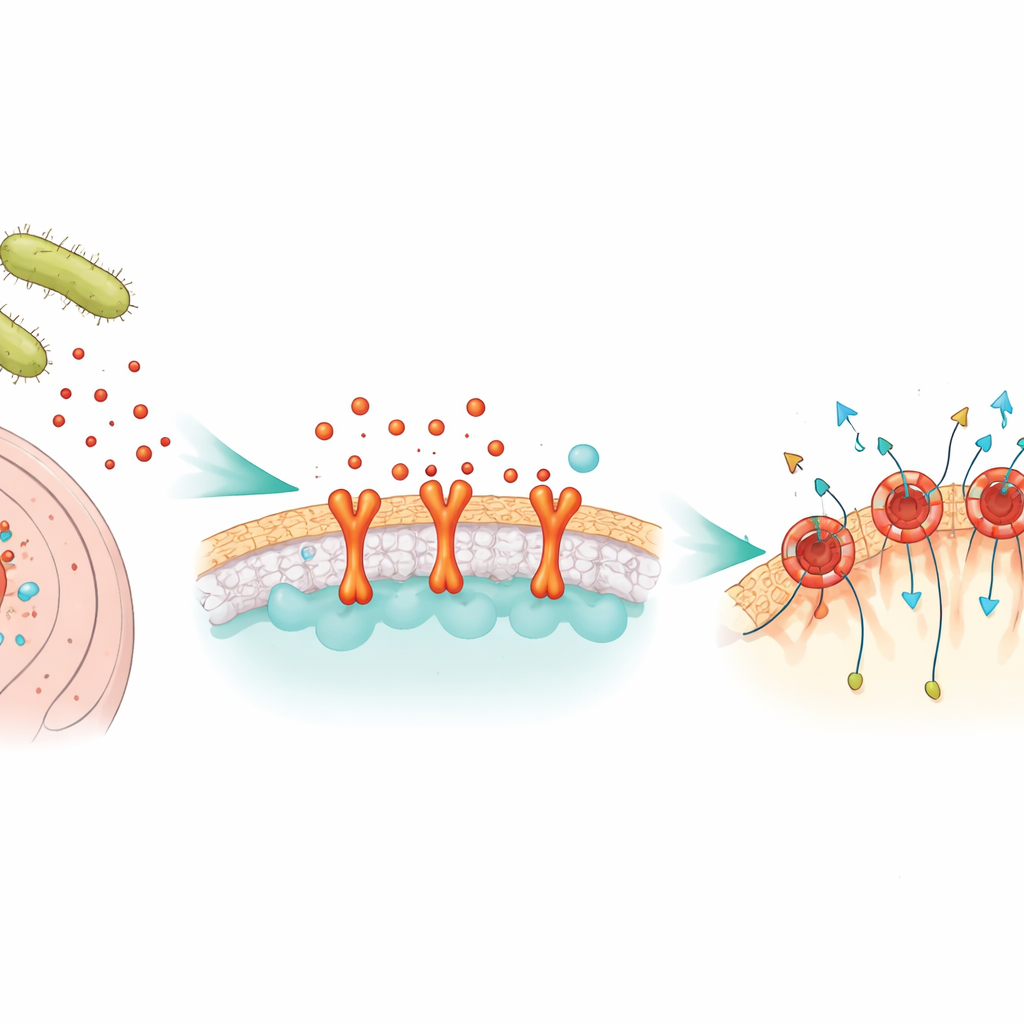
Eine bakterielle Waffe, die Löcher bohrt
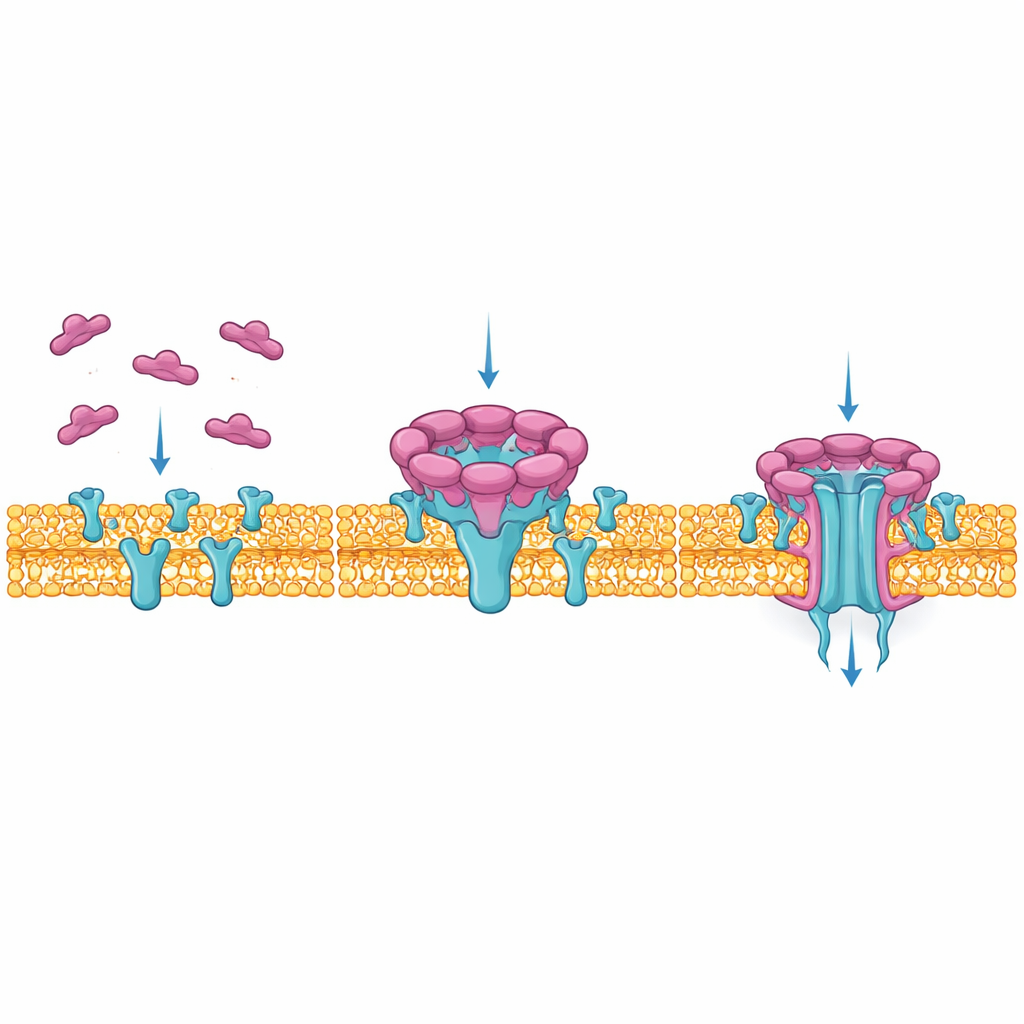
NetF gehört zu einer großen Familie von „porenbildenden“ Toxinen, die Bakterien als lösliche Einzelmoleküle freisetzen. Sobald sie eine geeignete Zelle erreichen, fügen sich diese Einheiten zu Ringen zusammen, die in die Zellmembran eindringen und Kanäle bilden. Durch diese Kanäle entweichen lebenswichtige Moleküle und die Zelle bricht zusammen. Obwohl ähnliche Toxine von Clostridium perfringens dafür bekannt sind, bei Schweinen, Geflügel und Menschen tödliche Darmerkrankungen zu verursachen, war bislang nur wenig darüber bekannt, wie NetF seine Opfer auswählt oder wie die endgültige Pore auf atomarer Ebene aussieht.
Den Andockgriff des Toxins finden
Die Forschenden fragten zunächst, warum bestimmte Zelltypen von Menschen, Hunden, Pferden und Rindern durch NetF getötet werden, andere aber unbeschadet bleiben. Durch den Vergleich der Genaktivität in empfindlichen und resistenten Zellen und durch wiederholte Exposition gegenüber NetF, bis seltene Überlebende dominierten, stellten sie fest, dass resistente Zellen konsequent deutlich weniger eines Oberflächenproteins namens ANTXR2 produzierten. Dieses Molekül war bereits als Hauptrezeptor für das Anthrax‑Toxin bekannt. Als das Team ANTXR2 mittels CRISPR‑Gentechnik ausschaltete, wurden Zellen resistent gegen NetF. Als sie zusätzlich menschliches, hunde‑, pferde‑ oder rinds‑ANTXR2 einfügten, wurden zuvor resistente Zellen hochgradig empfindlich, was bestätigte, dass NetF bei mehreren Tierarten auf ANTXR2 als Andockgriff angewiesen ist.
Beobachtung des Porenaufbaus im nahezu atomaren Maßstab
Um genau zu sehen, wie NetF seinen tödlichen Kanal aufbaut, nutzten die Autorinnen und Autoren kryo‑Elektronenmikroskopie, die eingefrorene Moleküle in sehr hoher Auflösung abbildet. Sie rekonstruierten die Interaktion des Toxins mit künstlichen Membranen und fanden zwei Hauptstadien: ein „Prä‑Pore“, in dem neun NetF‑Einheiten auf der Membranoberfläche sitzen, und eine Endpore, die meist aus acht Einheiten besteht, die ein langes, dicht gepacktes Proteinbarrel durch die Membran schieben. Der Vergleich dieser Stadien zeigte, wie eine flexible Schleife in jedem NetF‑Molekül herunterschwingt und sich in ein 50‑Ångström‑langes Barrel umformt, das zur Dicke der Membran passt und einen engen, wassergefüllten Tunnel schafft, durch den Ionen und kleine Moleküle passieren können.
Wie NetF sowohl Rezeptor als auch Membran greift
Das Team löste anschließend die Struktur der an den gesamten externen Teil von ANTXR2 gebundenen NetF‑Pore. Anders als das Anthrax‑Toxin, das eine Metall‑Bindestelle an der Spitze von ANTXR2 ergreift, klemmt NetF seitlich an den Rezeptor und berührt dabei zwei verschiedene Bereiche gleichzeitig. Diese Seitenumarmung positioniert das Toxin dicht an der Membran und ermöglicht es Teilen von NetF‑„Rand“ und „Stiel“, in benachbarte Lipide und Cholesterin einzudringen. Die Kontaktfläche ist ungewöhnlich reich an Tyrosin‑Resten, die sowohl die Rezeptorbindung als auch die Membranverankerung stabilisieren. Subtile Sequenzunterschiede im unteren Bereich des Rezeptors, insbesondere bei Mäusen, schwächen diese Passung und helfen zu erklären, warum Maus‑Zellen natürlicherweise resistenter gegen NetF sind als Zellen anderer Säugetiere.
Was diese Erkenntnisse für Krankheiten bedeuten
Insgesamt zeigen die Ergebnisse, dass NetF Zellen nur dann tötet, wenn es sich fest an ANTXR2 anheften kann und gleichzeitig umliegende Membranlipide zur Förderung der Poreninsertion einbezieht. Diese doppelte Erkennung erklärt die starke Aktivität bei Hunden und Fohlen, wo ANTXR2‑tragende Zellen im Darm besonders verwundbar sind, und die schwächere Wirkung bei Mäusen. Allgemeiner offenbart die Studie eine wiederkehrende Strategie porenbildender Toxine: die Bindung nahe an der Membran über spezifische Rezeptoren, die als Gerüst für die Porenassemblierung dienen. Durch die Kartierung der exakten Kontaktpunkte zwischen NetF und ANTXR2 ebnet diese Arbeit den Weg zur Entwicklung von Molekülen, die die Interaktion blockieren könnten und damit potenziell gefährdete Tiere vor verheerenden Darmerkrankungen schützen.
Zitation: Wang, C., Cattalani, F., Iacovache, I. et al. Identification and structural characterization of anthrax toxin receptor 2 as the Clostridium perfringens NetF receptor. Nat Commun 17, 2788 (2026). https://doi.org/10.1038/s41467-026-69526-6
Schlüsselwörter: porenbildendes Toxin, Clostridium perfringens, NetF, ANTXR2‑Rezeptor, bakterielle Pathogenese