Clear Sky Science · es
Identificación y caracterización estructural del receptor de la toxina del ántrax 2 como el receptor de NetF de Clostridium perfringens
Por qué esta toxina importa para personas y animales
Las infecciones intestinales graves en perros, caballos y ganado pueden aparecer de forma súbita, causando diarrea con sangre y en ocasiones la muerte. Un culpable frecuente es la bacteria Clostridium perfringens, que daña las células abriéndoles agujeros con potentes toxinas proteicas. Este estudio revela, con detalle molecular, cómo una de esas toxinas, llamada NetF, localiza y ataca a células animales específicas. El trabajo no solo aclara brotes de enfermedad en mascotas y animales de granja que resultaban enigmáticos, sino que también descubre reglas generales sobre cómo las toxinas formadoras de poros se enganchan a nuestras células, un paso que podría ser blanco de futuras terapias.
Un arma bacteriana que perfora
NetF pertenece a una amplia familia de toxinas “formadoras de poros” que las bacterias liberan como unidades solubles individuales. Una vez que contactan una célula adecuada, estas unidades se ensamblan en anillos que se insertan en la membrana celular y forman canales. A través de esos canales, moléculas vitales se escapan y la célula colapsa. Aunque se sabe que toxinas similares de Clostridium perfringens causan enfermedades intestinales mortales en cerdos, aves y personas, se conocía muy poco sobre cómo NetF elige a sus víctimas o cómo es su poro final a escala atómica.
Encontrando el punto de anclaje de la toxina
Los investigadores preguntaron primero por qué algunos tipos celulares de humanos, perros, caballos y bovinos son muertos por NetF mientras otros quedan indemnes. Al comparar la actividad génica en células sensibles y resistentes, y al exponer repetidamente células a NetF hasta que sobrevivientes raros dominaron, hallaron que las células resistentes producían consistentemente mucho menos de una proteína de superficie llamada ANTXR2. Esta molécula ya era famosa como el receptor principal de la toxina del ántrax. Cuando el equipo eliminó ANTXR2 mediante edición genética CRISPR, las células se volvieron resistentes a NetF. Cuando añadieron ANTXR2 humana, canina, equina o bovina adicional, células previamente resistentes se volvieron altamente sensibles, confirmando que NetF depende de ANTXR2 como su punto de anclaje en varias especies animales.
Observando el ensamblaje del poro a escala casi atómica
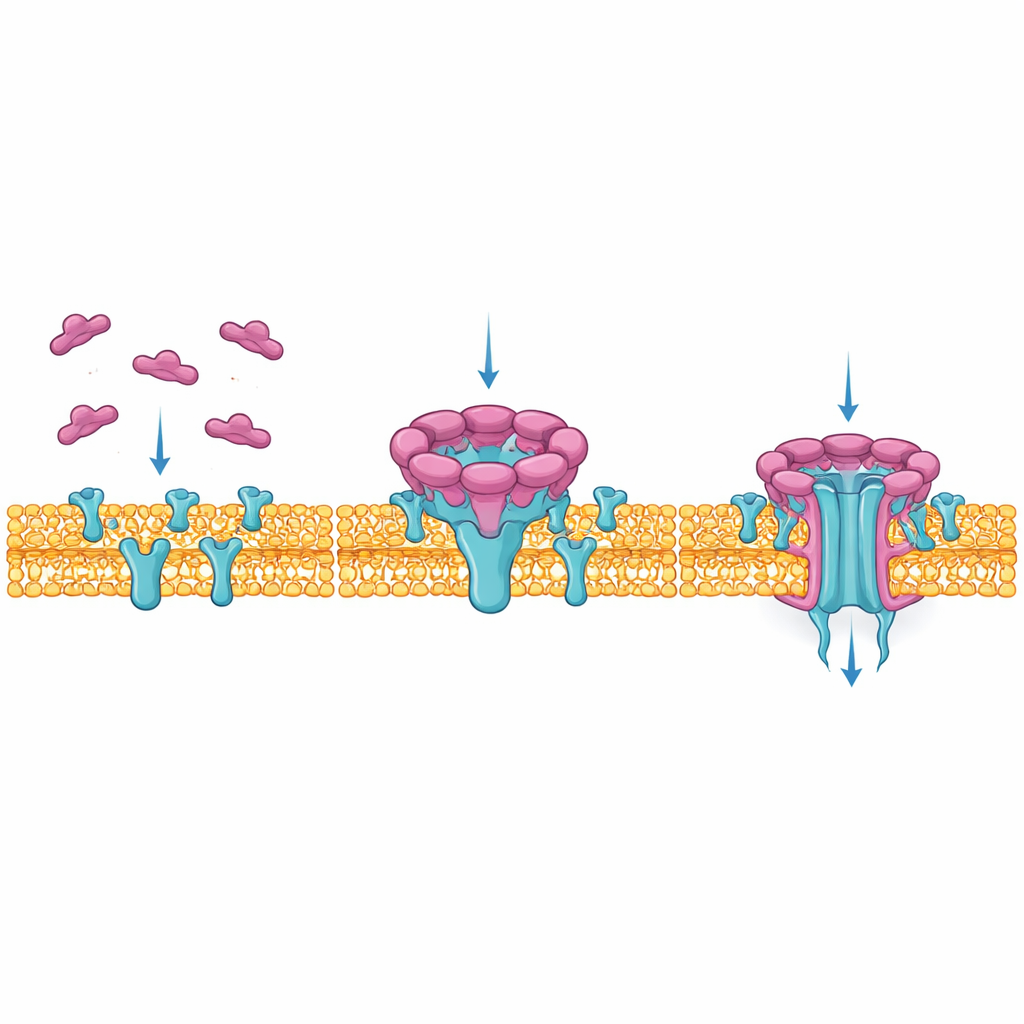
Para ver con precisión cómo NetF construye su canal letal, los autores usaron crio‑microscopía electrónica, que imagen moléculas congeladas al instante a muy alta resolución. Recrearon la interacción de la toxina con membranas artificiales y encontraron dos etapas principales: un “pre‑poro”, donde nueve unidades de NetF se disponen sobre la superficie de la membrana, y un poro final, con más frecuencia formado por ocho unidades que han empujado un largo y compactado barril de proteína a través de la membrana. Comparar estas etapas mostró cómo un bucle flexible en cada molécula de NetF se pliega hacia abajo y se reconfigura en un barril de 50 angstroms de longitud que coincide con el espesor de la membrana, creando un túnel estrecho lleno de agua por el que pueden pasar iones y pequeñas moléculas.
Cómo NetF se agarra tanto al receptor como a la membrana
El equipo resolvió posteriormente la estructura del poro de NetF unido a la porción exterior completa de ANTXR2. A diferencia de la toxina del ántrax, que se fija en un sitio de unión a metales en la punta de ANTXR2, NetF se sujeta al lateral del receptor, contactando dos regiones diferentes a la vez. Este abrazo lateral posiciona la toxina próxima a la membrana y permite que partes del “borde” y del “tallo” de NetF se incrusten en los lípidos y el colesterol circundantes. La interfaz es inusualmente rica en residuos de tirosina, que ayudan a estabilizar tanto la unión al receptor como el anclaje a la membrana. Diferencias sutiles en la secuencia de la región inferior del receptor, especialmente en ratones, debilitan este encaje y ayudan a explicar por qué las células de ratón son de forma natural más resistentes a NetF que las células de otros mamíferos.
Qué significan estos hallazgos para la enfermedad
En conjunto, los resultados muestran que NetF mata células solo cuando puede adherirse firmemente a ANTXR2 y, al mismo tiempo, interactuar con lípidos de la membrana circundante para impulsar la inserción del poro. Este reconocimiento dual explica su fuerte actividad en perros y potros, donde las células intestinales que expresan ANTXR2 son objetivos primarios, y su acción más débil en ratones. Más en general, el estudio revela una estrategia recurrente entre las toxinas formadoras de poros: unirse cerca de la membrana a través de receptores específicos que actúan como andamios para el ensamblaje del poro. Al mapear los puntos de contacto exactos entre NetF y ANTXR2, este trabajo abre la puerta al diseño de moléculas que podrían bloquear la interacción, protegiendo potencialmente a animales vulnerables de devastadoras enfermedades intestinales.
Cita: Wang, C., Cattalani, F., Iacovache, I. et al. Identification and structural characterization of anthrax toxin receptor 2 as the Clostridium perfringens NetF receptor. Nat Commun 17, 2788 (2026). https://doi.org/10.1038/s41467-026-69526-6
Palabras clave: toxina formadora de poros, Clostridium perfringens, NetF, receptor ANTXR2, patogénesis bacteriana