Clear Sky Science · it
Identificazione e caratterizzazione strutturale del recettore dell'antitossina dell'antrace 2 come recettore di Clostridium perfringens NetF
Perché questa tossina è importante per persone e animali
Le gravi infezioni intestinali in cani, cavalli e bestiame possono manifestarsi all'improvviso, provocando diarrea sanguinolenta e talvolta la morte. Un colpevole comune è il batterio Clostridium perfringens, che danneggia le cellule praticando fori nella loro membrana con potenti proteine tossiche. Questo studio rivela, a livello molecolare, come una di queste tossine, chiamata NetF, individua e attacca cellule animali specifiche. Il lavoro non solo spiega focolai di malattia altrimenti inspiegabili in animali domestici e da allevamento, ma mette anche in luce regole generali su come le tossine formanti pori si agganciano alle nostre cellule, un passaggio che potrebbe essere bersaglio di terapie future.
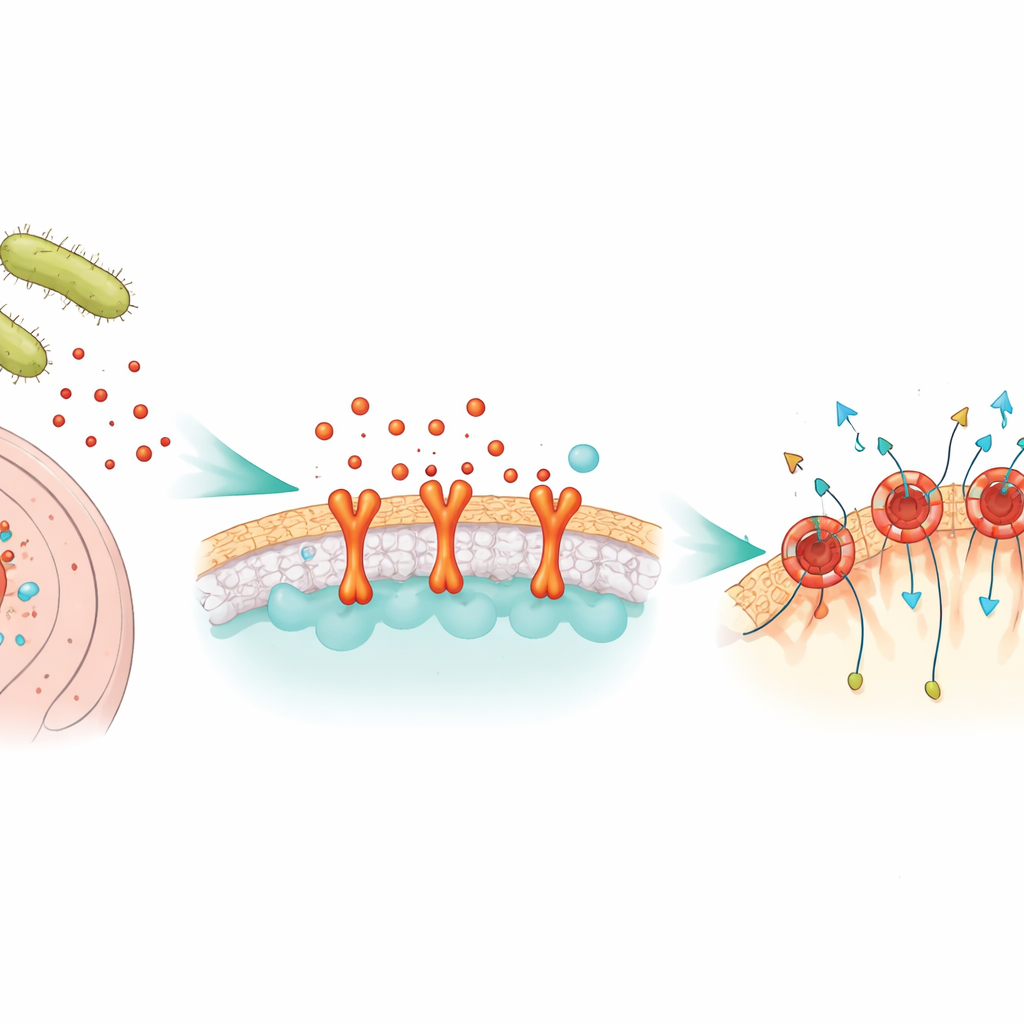
Un’arma batterica che perfora le membrane
NetF appartiene a una grande famiglia di tossine “formanti pori” che i batteri rilasciano come unità solubili monomeriche. Una volta che incontrano una cellula adatta, queste unità si assemblano in anelli che si inseriscono nella membrana cellulare formando canali. Attraverso questi canali fuoriescono molecole vitali e la cellula collassa. Sebbene tossine simili di Clostridium perfringens siano note per causare malattie intestinali letali in suini, pollame e persone, si sapeva molto poco su come NetF scelga le sue vittime o quale sia l’aspetto finale del suo poro a livello atomico.
Trovare l’impugnatura a cui si aggancia la tossina
Gli autori hanno innanzitutto chiesto perché alcuni tipi cellulari di esseri umani, cani, cavalli e bovini vengano uccisi da NetF mentre altri rimangono indenni. Confrontando l’attività genica in cellule sensibili e resistenti e esponendo ripetutamente cellule a NetF finché non sopravvissero rari resistenti, hanno scoperto che le cellule resistenti producevano costantemente molto meno di una proteina di superficie chiamata ANTXR2. Questa molecola era già nota come recettore principale della tossina dell’antrace. Quando il gruppo ha eliminato ANTXR2 usando l’editing genetico CRISPR, le cellule sono diventate resistenti a NetF. Quando hanno aggiunto copie extra di ANTXR2 umana, canina, equina o bovina, cellule precedentemente resistenti sono diventate altamente sensibili, confermando che NetF si affida ad ANTXR2 come impugnatura di aggancio in diverse specie animali.
Osservare l’assemblaggio del poro a scala quasi atomica
Per vedere con precisione come NetF costruisce il suo canale letale, gli autori hanno usato la criomicroscopia elettronica, che immortala molecole congelate a risoluzione molto elevata. Hanno ricreato l’interazione della tossina con membrane artificiali e trovato due stadi principali: un “pre‑poro”, dove nove unità di NetF si dispongono sulla superficie della membrana, e un poro finale, spesso composto da otto unità che hanno fatto penetrare nella membrana un lungo e compatto barrel proteico. Il confronto tra questi stadi ha mostrato come un anello flessibile in ciascuna molecola di NetF si abbassi e si riorganizzi in un barile lungo circa 50 ångström che corrisponde allo spessore della membrana, creando un tunnel stretto, riempito d’acqua, attraverso il quale ioni e piccole molecole possono passare.
Come NetF afferra sia il recettore sia la membrana
Il gruppo ha quindi risolto la struttura del poro di NetF legato all’intera porzione esterna di ANTXR2. A differenza della tossina dell’antrace, che si lega a un sito di legame per metalli sulla punta di ANTXR2, NetF si ancora al lato del recettore, toccando contemporaneamente due regioni diverse. Questa presa laterale posiziona la tossina vicino alla membrana e permette a parti della “corona” e dello “stelo” di NetF di scavare nei lipidi e nel colesterolo circostanti. L’interfaccia è insolitamente ricca di residui di tirosina, che contribuiscono a stabilizzare sia il legame con il recettore sia l’ancoraggio alla membrana. Sottili differenze di sequenza nella regione inferiore del recettore, in particolare nei topi, indeboliscono questo adattamento e aiutano a spiegare perché le cellule murine sono naturalmente più resistenti a NetF rispetto a quelle di altri mammiferi.
Implicazioni di questi risultati per la malattia
Complessivamente, i risultati mostrano che NetF uccide le cellule solo quando può aggrapparsi saldamente ad ANTXR2 e contemporaneamente interagire con i lipidi della membrana circostante per favorire l’inserimento del poro. Questo doppio riconoscimento spiega la sua forte attività in cani e puledri, dove le cellule intestinali che esprimono ANTXR2 sono bersagli principali, e la sua azione più debole nei topi. Più in generale, lo studio rivela una strategia ricorrente tra le tossine formanti pori: legarsi vicino alla membrana tramite recettori specifici che fungono da impalcatura per l’assemblaggio del poro. Mappando i punti di contatto esatti tra NetF e ANTXR2, questo lavoro apre la strada alla progettazione di molecole in grado di bloccare l’interazione, proteggendo potenzialmente gli animali vulnerabili da devastanti malattie intestinali.
Citazione: Wang, C., Cattalani, F., Iacovache, I. et al. Identification and structural characterization of anthrax toxin receptor 2 as the Clostridium perfringens NetF receptor. Nat Commun 17, 2788 (2026). https://doi.org/10.1038/s41467-026-69526-6
Parole chiave: tossina formante pori, Clostridium perfringens, NetF, recettore ANTXR2, patogenesi batterica