Clear Sky Science · fr
Identification et caractérisation structurale du récepteur de la toxine du charbon 2 comme récepteur de NetF de Clostridium perfringens
Pourquoi cette toxine importe pour les humains et les animaux
Des infections intestinales graves chez les chiens, les chevaux et le bétail peuvent survenir brusquement, provoquant des diarrhées sanglantes et parfois la mort. Un coupable fréquent est la bactérie Clostridium perfringens, qui endommage les cellules en leur perforant la membrane grâce à de puissantes toxines protéiques. Cette étude révèle, en détail moléculaire, comment l’une de ces toxines, appelée NetF, repère et attaque des cellules animales spécifiques. Ce travail explique non seulement des flambées de maladie énigmatiques chez les animaux de compagnie et d’élevage, mais met aussi en lumière des règles générales sur la façon dont les toxines formant des pores s’attachent à nos cellules, une étape qui pourrait être ciblée par des thérapies futures.
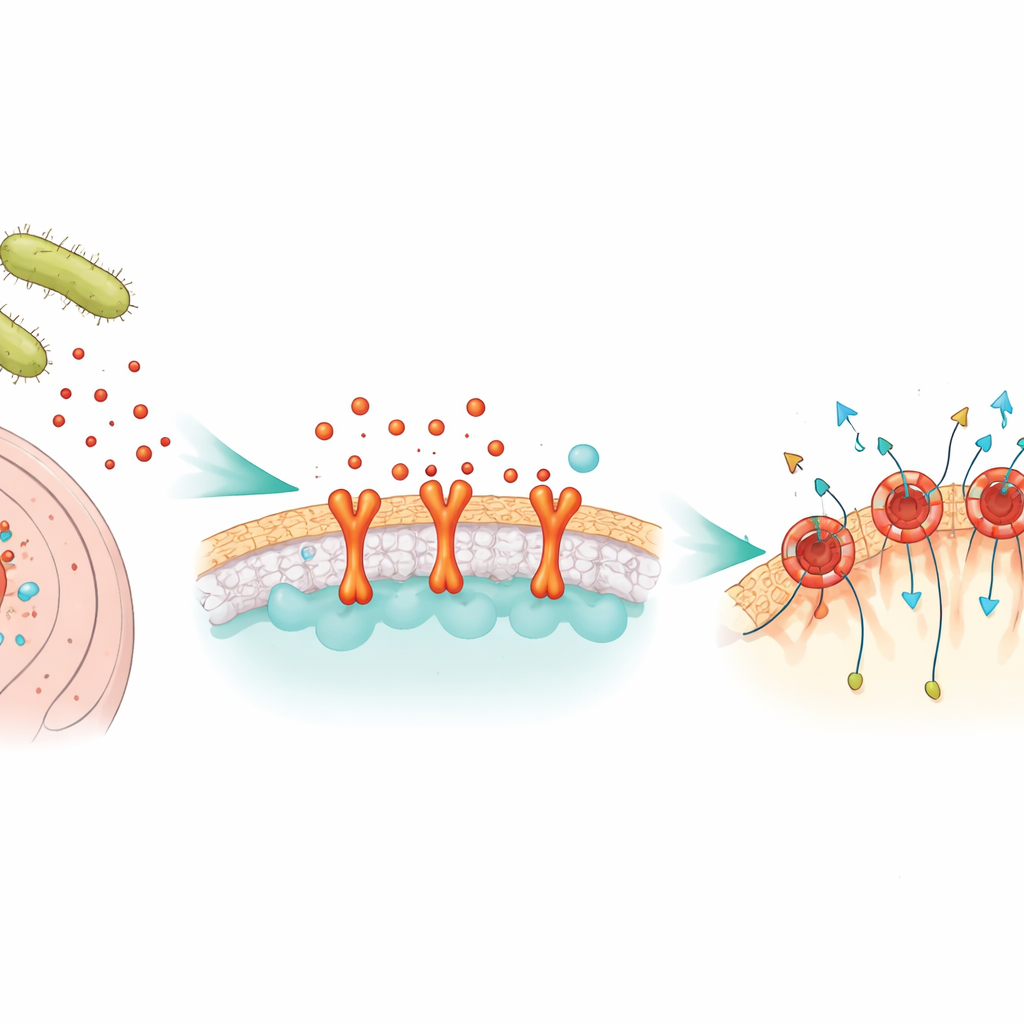
Une arme bactérienne qui fore des trous
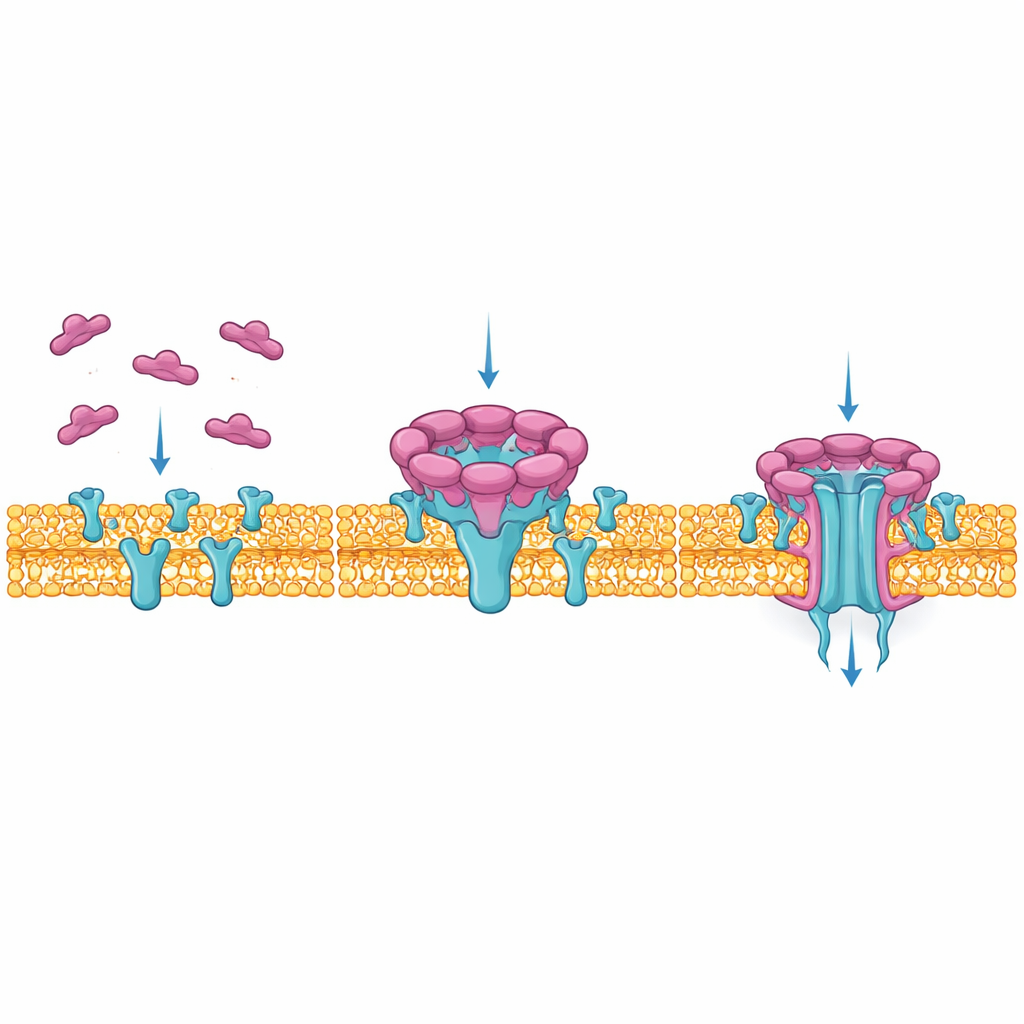
NetF appartient à une vaste famille de toxines « formant des pores » que les bactéries libèrent sous forme d’unités solubles monomériques. Une fois qu’elles rencontrent une cellule compatible, ces unités s’assemblent en anneaux qui s’insèrent dans la membrane cellulaire et forment des canaux. Par ces canaux, des molécules vitales s’échappent et la cellule s’effondre. Bien que des toxines similaires issues de Clostridium perfringens soient reconnues pour provoquer des maladies intestinales mortelles chez les porcs, la volaille et les humains, on savait très peu de choses sur la façon dont NetF choisit ses victimes ni sur l’apparence atomique de son pore final.
Repérer la poignée d’amarrage de la toxine
Les chercheurs ont d’abord cherché à comprendre pourquoi certains types cellulaires d’humains, de chiens, de chevaux et de bovins sont tués par NetF tandis que d’autres restent indemnes. En comparant l’activité génique des cellules sensibles et résistantes, et en exposant à plusieurs reprises des cellules à NetF jusqu’à ce que de rares survivants prennent le dessus, ils ont constaté que les cellules résistantes produisaient systématiquement beaucoup moins d’une protéine de surface appelée ANTXR2. Cette molécule était déjà connue comme étant le récepteur principal de la toxine du charbon. Lorsque l’équipe a inactivé ANTXR2 par édition génomique CRISPR, les cellules sont devenues résistantes à NetF. Lorsqu’ils ont ajouté des copies supplémentaires d’ANTXR2 humaines, canines, équines ou bovines, des cellules auparavant résistantes sont devenues fortement sensibles, confirmant que NetF s’appuie sur ANTXR2 comme poignée d’amarrage chez plusieurs espèces animales.
Observer l’assemblage du pore à l’échelle quasi atomique
Pour voir précisément comment NetF construit son canal mortel, les auteurs ont utilisé la cryo‑microscopie électronique, qui image des molécules vitrifiées à très haute résolution. Ils ont reconstitué l’interaction de la toxine avec des membranes artificielles et identifié deux étapes principales : un « pré‑pore », où neuf unités de NetF sont posées à la surface de la membrane, et un pore final, le plus souvent composé de huit unités qui ont projeté un long barrel protéique étroitement empaqueté à travers la membrane. La comparaison de ces étapes montre comment une boucle flexible de chaque molécule de NetF bascule et se repli pour former un barrel d’environ 50 angström de long qui correspond à l’épaisseur de la membrane, créant un tunnel étroit rempli d’eau par lequel ions et petites molécules peuvent passer.
Comment NetF agrippe à la fois le récepteur et la membrane
L’équipe a ensuite résolu la structure du pore de NetF lié à la portion externe entière d’ANTXR2. Contrairement à la toxine du charbon, qui saisit un site de liaison au métal à l’extrémité d’ANTXR2, NetF s’accroche sur le côté du récepteur, en contact avec deux régions distinctes à la fois. Cette étreinte latérale positionne la toxine près de la membrane et permet à des parties du « rebord » et de la « tige » de NetF de s’enfoncer dans les lipides et le cholestérol voisins. L’interface est exceptionnellement riche en résidus de tyrosine, qui contribuent à stabiliser à la fois la liaison au récepteur et l’ancrage membranaire. De subtiles différences de séquence dans la région inférieure du récepteur, notamment chez la souris, affaiblissent cet ajustement et aident à expliquer pourquoi les cellules de souris sont naturellement plus résistantes à NetF que celles d’autres mammifères.
Ce que ces découvertes signifient pour la maladie
Globalement, les résultats montrent que NetF tue les cellules uniquement lorsqu’il peut s’ancrer fermement sur ANTXR2 tout en engageant simultanément les lipides membranaires environnants pour favoriser l’insertion du pore. Cette reconnaissance double explique sa forte activité chez les chiens et les poulains, où les cellules porteuses d’ANTXR2 dans l’intestin sont des cibles privilégiées, et sa moindre action chez la souris. Plus généralement, l’étude révèle une stratégie récurrente chez les toxines formant des pores : se lier près de la membrane via des récepteurs spécifiques qui servent de supports à l’assemblage du pore. En cartographiant les points de contact exacts entre NetF et ANTXR2, ce travail ouvre la voie à la conception de molécules capables de bloquer cette interaction, protégeant potentiellement les animaux vulnérables contre des maladies intestinales dévastatrices.
Citation: Wang, C., Cattalani, F., Iacovache, I. et al. Identification and structural characterization of anthrax toxin receptor 2 as the Clostridium perfringens NetF receptor. Nat Commun 17, 2788 (2026). https://doi.org/10.1038/s41467-026-69526-6
Mots-clés: toxine formant un pore, Clostridium perfringens, NetF, récepteur ANTXR2, pathogenèse bactérienne