Clear Sky Science · sv
Histidinrika coiled-coils främjar zinkberoende självmontering och härdning av porösa mussel-lim
Hur musslor tillverkar superlim under vatten
Musslor fäster vid vågbankade klippor med ett naturligt lim som forskare har försökt efterlikna i årtionden. Denna studie visar att en länge förbisedd ingrediens — snarare än den vanliga kemiska stjärnan — tyst utför mycket av det tunga arbetet. Genom att avslöja hur ett speciellt protein och metallen zink hjälper musslor att bygga ett starkt, svampliknande lim öppnar forskningen nya vägar till mildare, mer hållbara adhesiver för medicin, teknik och vardagliga våta ytor.
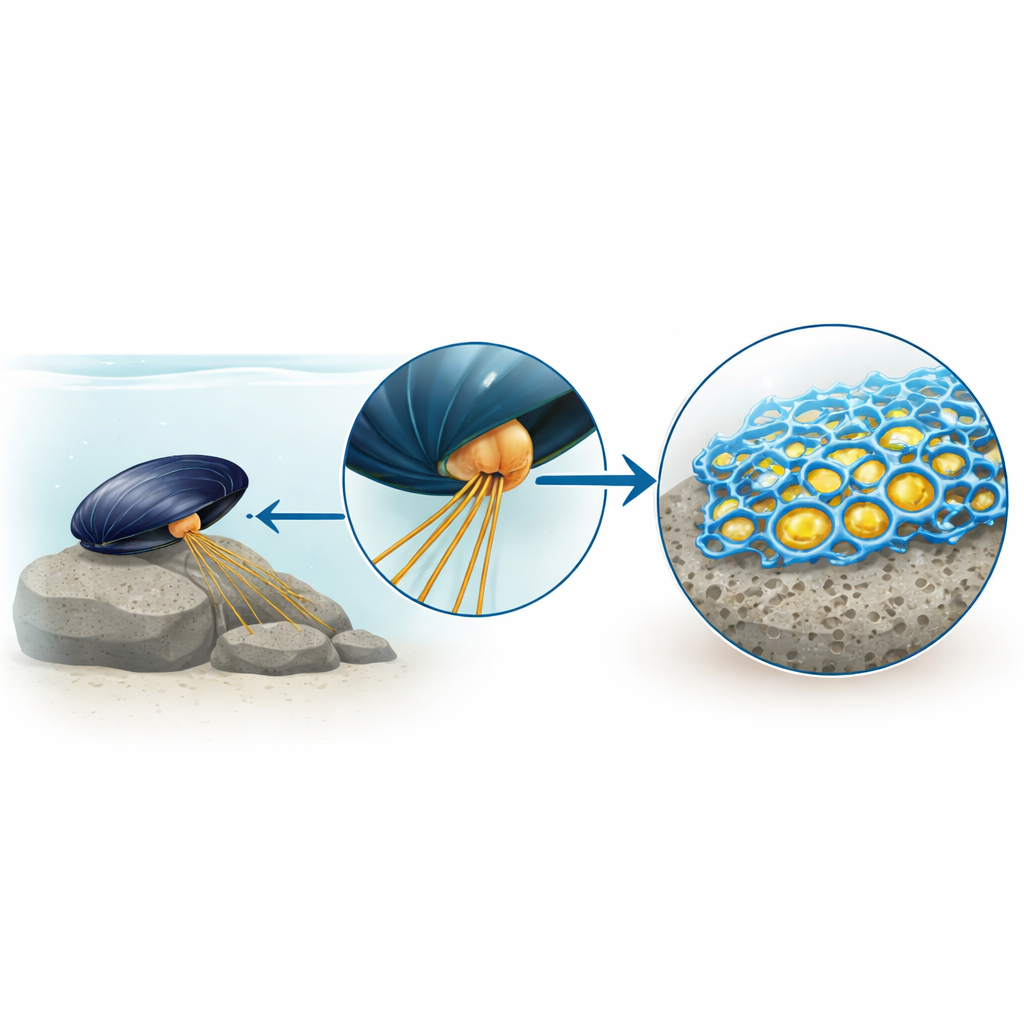
Från kladdigt mysterium till ny limhjälte
I åratal har berättelsen om mussellim kretsat kring en modifierad byggsten kallad DOPA, som fäster starkt vid ytor och metaller. Syntetiska material inspirerade av DOPA har imponerat, men når ändå inte upp till det verkliga mussellimet. Författarna misstänkte att andra, outredda proteiner inne i musslans limproducerande körtlar kunde vara saknade pusselbitar. Genom att isolera små, limfyllda blåsor från musselfoten och iaktta hur de spricker och stelnar fann de att en delmängd av proteiner bildade ett fast skelett med en porös, skumliknande struktur, medan de välkända DOPA‑rika proteinerna förblev mestadels som en vätska i porerna.
Upptäckt av ett dolt strukturellt protein
När teamet löste upp bara den fasta delen av detta miniatyrlim och analyserade dess innehåll framträdde ett enda dominerande protein. De döpte det till mefp-12 och upptäckte att det är rikt på aminosyran histidin och bevarat över flera musselarter, vilket tyder på att det är viktigt för överlevnad. Avbildning av musselfotens vävnad visade att celler i den limproducerande körteln särskilt tillverkar detta protein för plattan — den tillplattade dyna som förankrar musslan i stenen. Datorbaserade strukturförutsägelser indikerade att mefp-12 har ett långt centralt segment som föredrar att bilda rep‑liknande buntar kända som coiled coils, och flera kompakta domäner som liknar metallbindande ”zinkfinger”‑regioner, vilket alla antyder att metalljoner, särskilt zink, kan vara avgörande för dess beteende.
Hur zink och pH förvandlar flytande droppar till fast skum
För att testa denna idé på ett enkelt sätt tillverkade forskarna en 30‑aminosyrasekvens från mefp-12:s centrala region. I saltvatten under lätt sura förhållanden — liknande lagringsmiljön inne i musselfoten — samlades denna korta bit till flytande droppar när zink var närvarande, men inte med andra metaller som koppar eller nickel. Att höja pH mot havsvattnets nivå utlöste en slående förvandling: dropparna sammansmälte, spreds på ytor och ”härdade” sedan till ett stelt, öppencelligt poröst material som under mikroskop liknade naturligt mussellim. Spektroskopi och kärnmagnetisk resonansmätning visade att under denna övergång skiftar proteinbitarna från ett löst, oordnat tillstånd till mer ordnade spiralformer som packar ihop sig, medan histidinsidokedjor bildar tåliga broar till zinkjoner. Dessa metallbryggor låser de coiled strukturerna i ett stabilt, men reversibelt, nätverk.

Ett tåligt, återvinningsbart nätverk byggt för vågor
Författarna föreslår en ny bild av hur mussellim bildas. Inne i foten förvaras mefp-12 i sura, zinkhaltiga droppar tillsammans med andra limproteiner. När sekretet frigörs i det högre pH‑värdet i havsvattnet börjar histidiner på mefp-12 binda zink, vilket driver proteinet att omorganisera sig till coiled‑buntar som kopplas samman till ett poröst ramverk. DOPA‑rika adhesiva proteiner förblir som en mer flytande fas i porerna, redo att våta och åter‑våta ytor. Senare stärker andra metaller som järn och vanadin de DOPA‑innehållande komponenterna och skapar ett sammanlåsande dubbelnät. Histidin–zinkramverket fungerar sannolikt som en uppoffrande, men återhämtbar, stötupptagare som hjälper plattan att dissipera energi från krossande vågor samtidigt som fästförmågan bibehålls över lång tid.
Vad detta betyder för framtida våta lim
Genom att flytta fokus från enbart DOPA till ett partnerskap mellan histidinrika proteiner och zink skriver denna studie om reglerna för mussellim. Den visar att instruktionerna för att bilda ett självmonterande, poröst fast material är kodade direkt i mefp-12‑sekvensen, aktiverade enkelt av salt, metalljoner och en pH‑förändring. Dessa insikter antyder nya designprinciper för konstgjorda adhesiver och mjuka material: använd kontrollerad fasskillnad, metall–protein‑broar och skumliknande arkitekturer för att skapa lim och geler som härdar i våta förhållanden, absorberar skador och potentiellt självläker, utan att förlita sig enbart på en enda mycket reaktiv kemisk grupp.
Citering: Rivard, M.D., Poulhazan, A., Renner-Rao, M.J. et al. Histidine-rich coiled-coils promote zinc-dependent self-assembly and curing of porous mussel glues. Nat Commun 17, 2809 (2026). https://doi.org/10.1038/s41467-026-69504-y
Nyckelord: musseladhesion, bioinspirerat lim, proteinsjälvmontering, metallkoordinerade material, våta adhesives